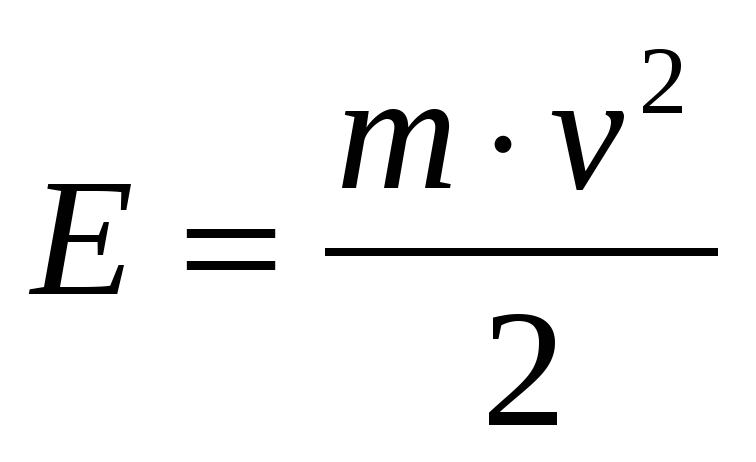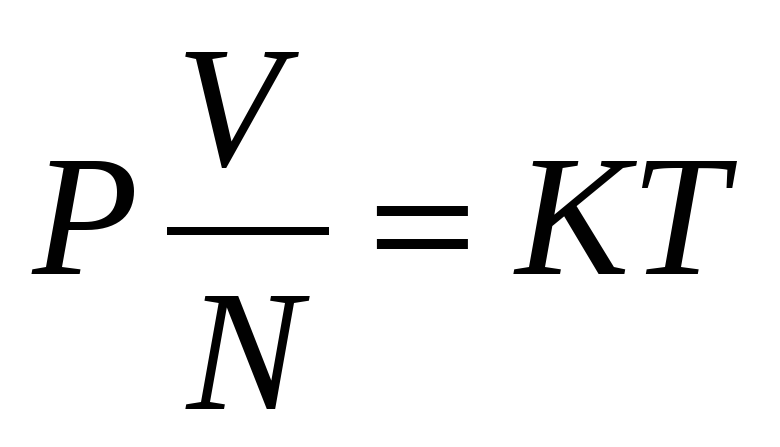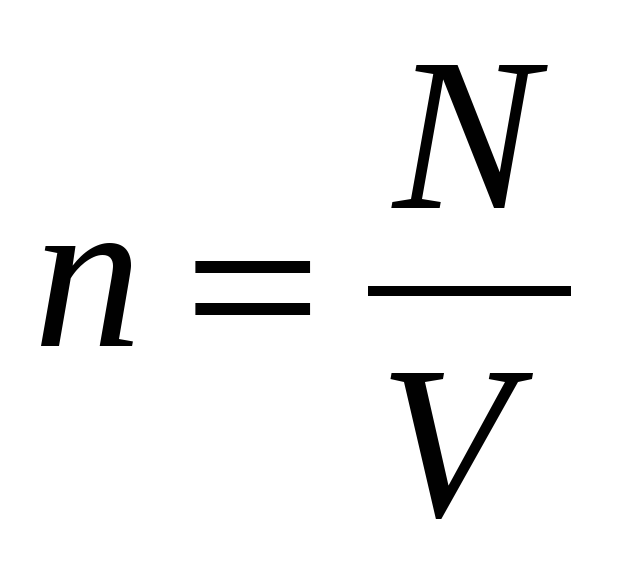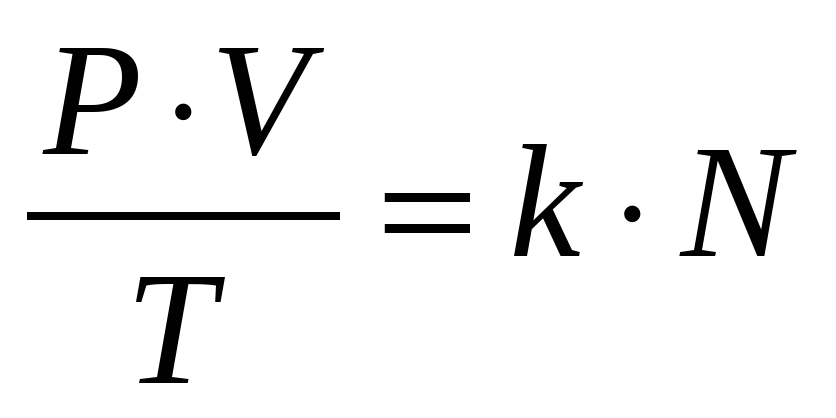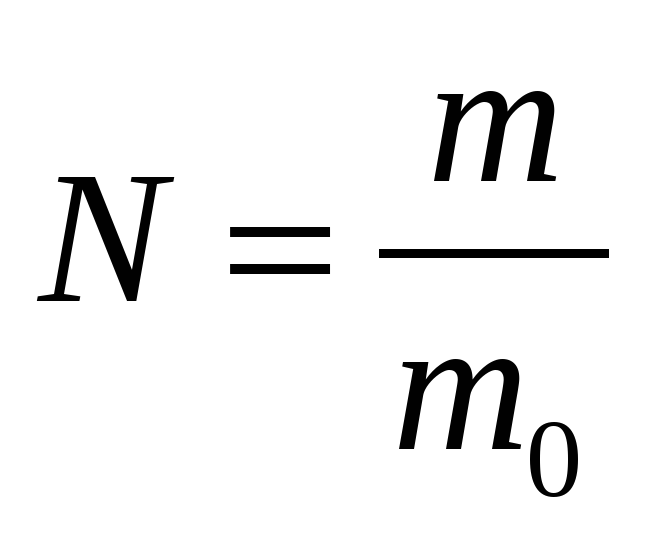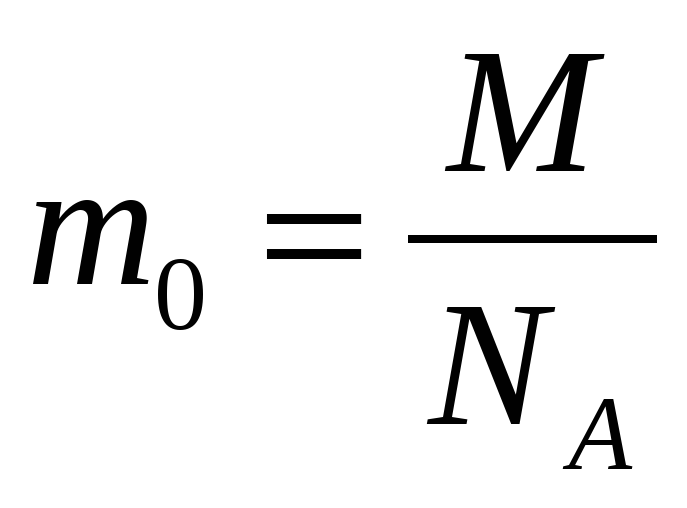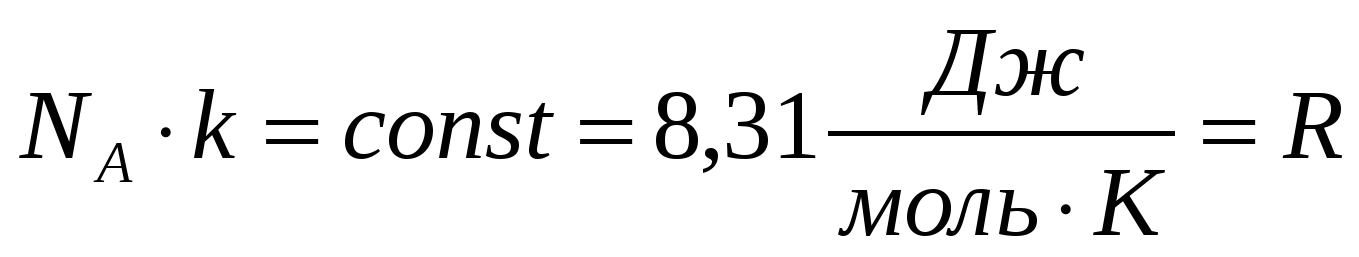Конспект по физике. Модуль 2. Идеальный газ
Конспект по физике. Модуль 2. Идеальный газ
Просмотр содержимого документа
«Конспект по физике. Модуль 2. Идеальный газ»
7 Идеальный газ
Идеальный газ — это газ, в котором можно пренебречь взаимодействием между молекулами.
Эта модель вводится для того, чтобы упростить вывод основного уравнения МКТ.
Будем учитывать только кинетическую энергию частиц, пренебрегая энергией их взаимодействия.
В реальных газах силы отталкивания возникают при столкновении частиц на очень короткое время, и большую часть времени молекулы газа движутся как свободные частицы.
О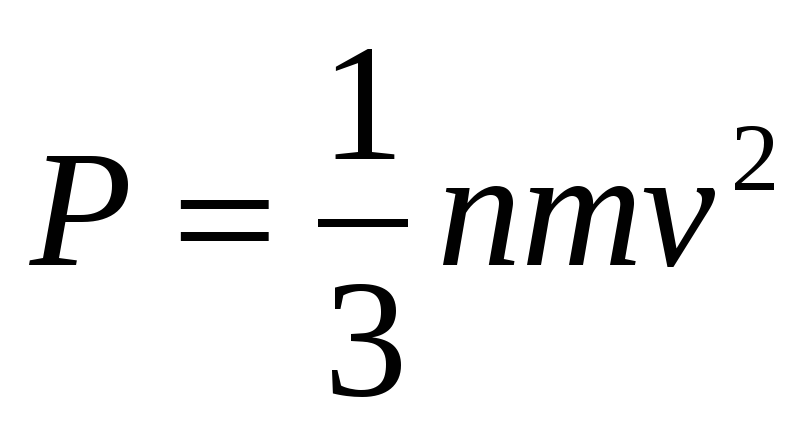
которое может быть измерено манометром, — с микроскопическими величинами, характеризующими молекулы, и является как бы мостом между макромиром и микромиром.
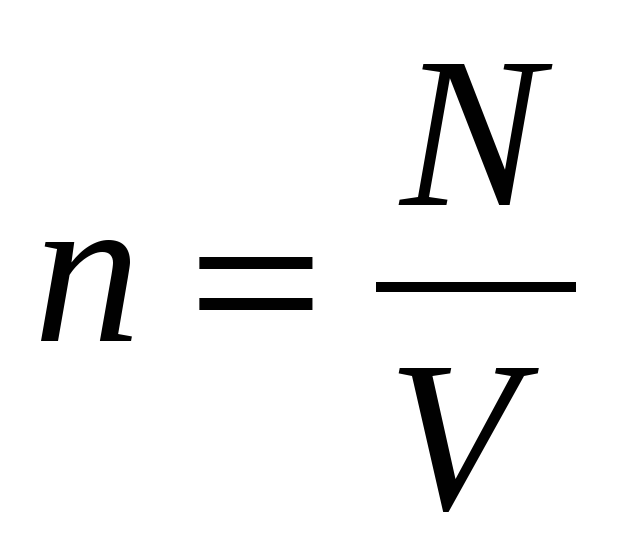
Р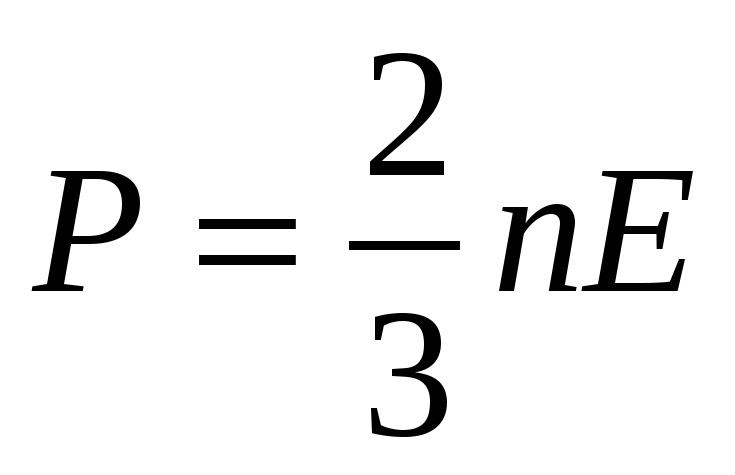
— средняя кинетическая энергия молекул
t = -273 0 – абсолютный нуль температуры – это температура, при которой останавливается поступательное движение молекул, движение электронов в атомах нельзя остановить ни при какой температуре, следовательно движение – неотъемлемое свойство материи.
Т = t + 273 t = 25 0 T = 25 + 273 = 298 К t = -17 0 T =-17 + 273 = 256 К
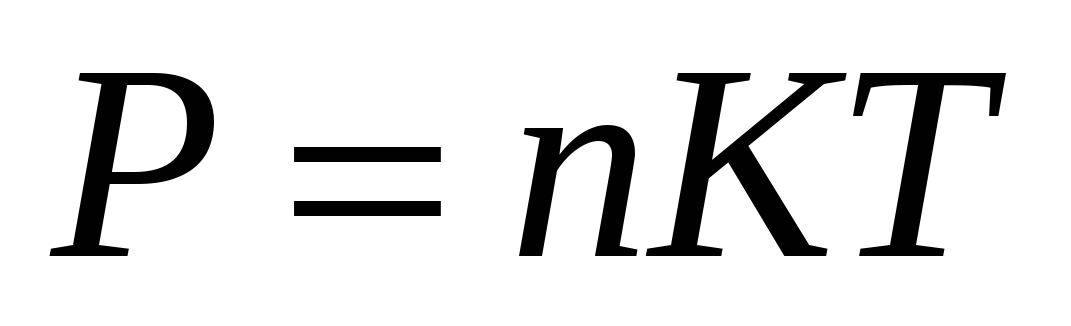
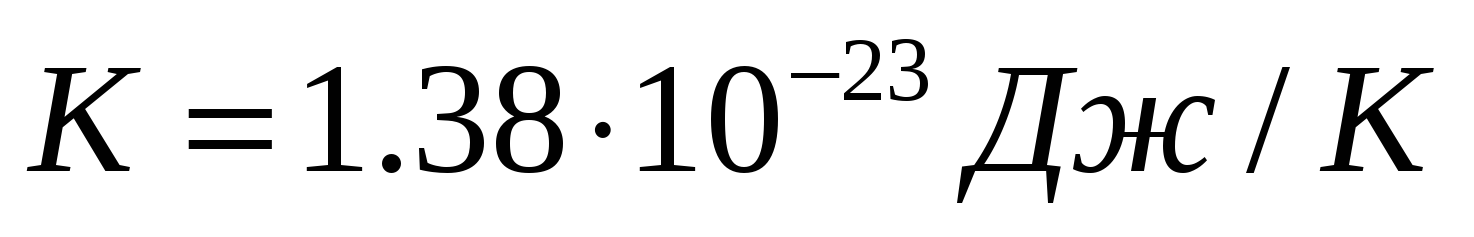
Постоянная Больцмана показывает, что на 1 0 или на
1 К приходится энергия 1,38 *10 -23 Дж. Таким образом, при нагревании вещества на 1 0 или на 1 К надо затратить 1,38 *10 -23 Дж энергии.
М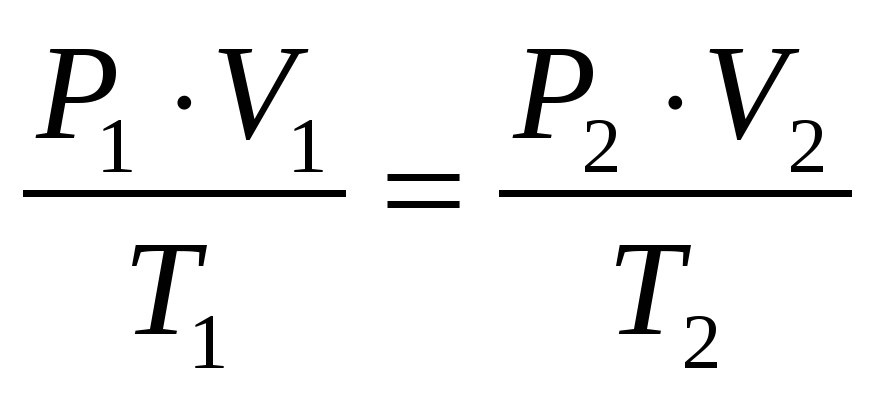
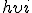
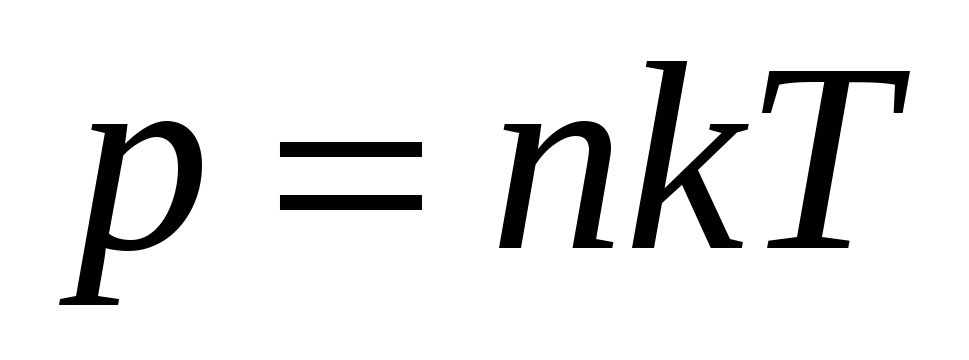
где Р – давление, V –объем, Т – термодинамическая температура, 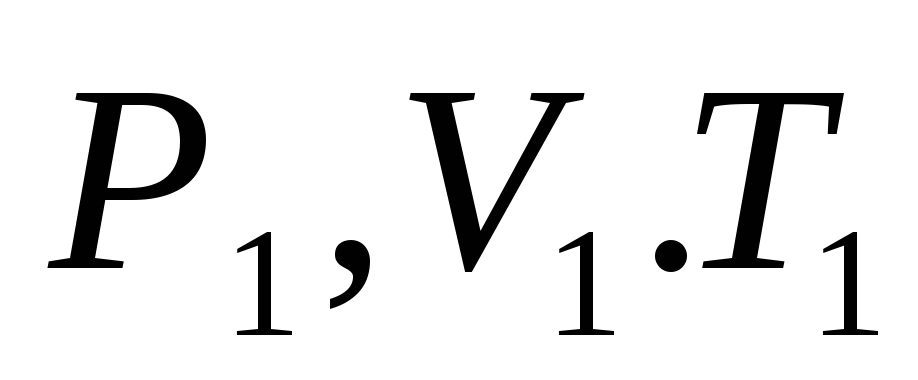
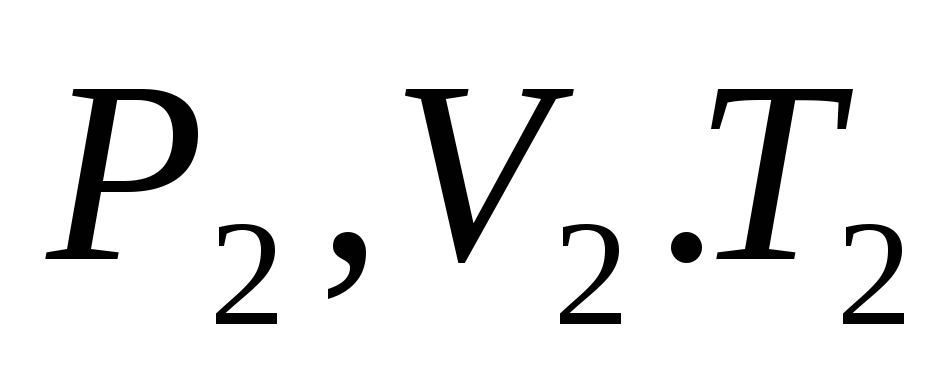
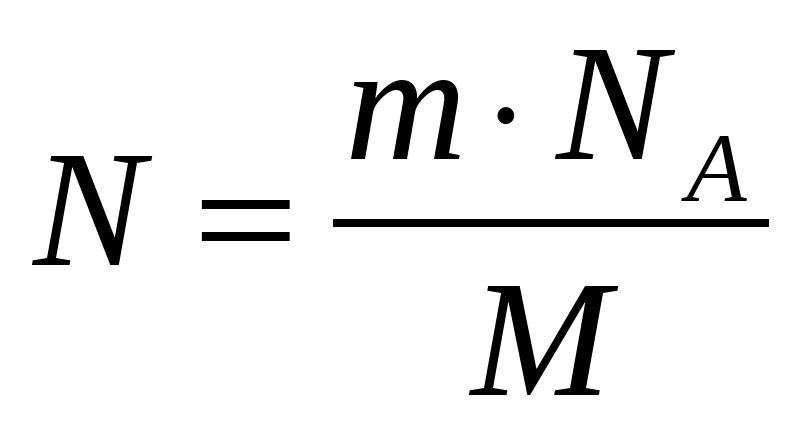
R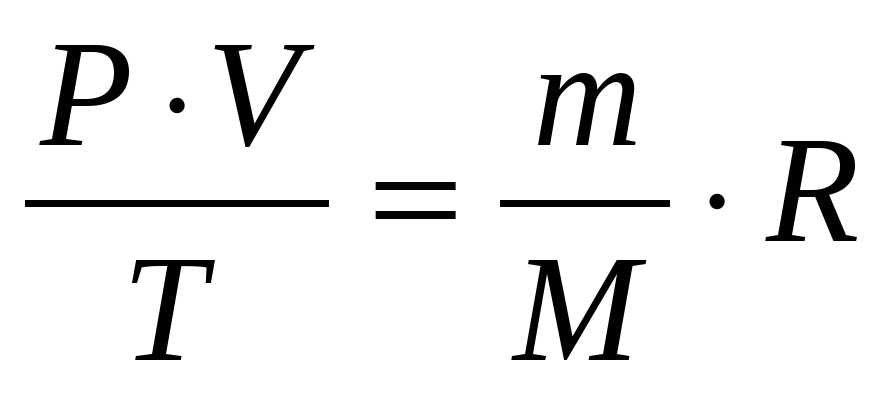
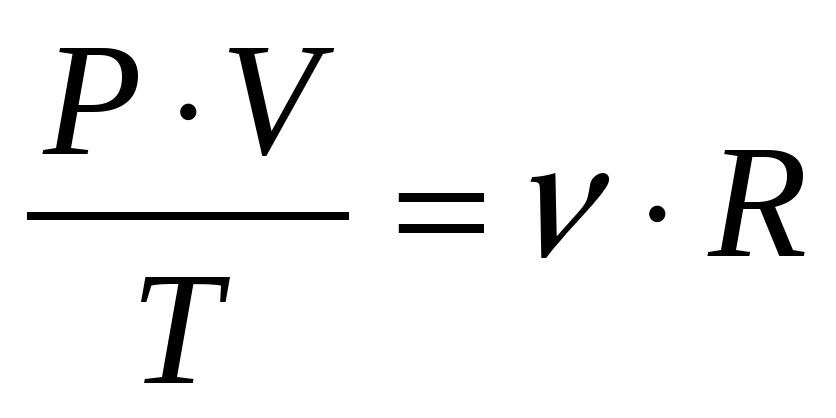
Физика. 10 класс
Конспект урока
Физика, 10 класс
Урок 20. Уравнение состояния идеального газа. Газовые законы
Перечень вопросов, рассматриваемых на уроке:
1) уравнение состояния идеального газа и уравнение Менделеева — Клапейрона;
2) закон Дальтона, парциальное давление, закон Авогадро;
3) газовые законы и границы их применимости;
4) графики изохорного, изобарного и изотермического процесса;
5) определение по графикам характера процессов и макропараметров идеального газа;
6) применение модели идеального газа для описания поведения реальных газов.
Глоссарий по теме
Уравнение, связывающее три макроскопических параметра давление, объём и температура, называют уравнением состояния идеального газа.
Парциальное давление – давление отдельно взятого компонента газовой смеси, равно давлению, которое он будет оказывать, если занимает весь объем при той же температуре.
Количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называют газовыми законами (изопроцессами).
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют изотермическим.
Процесс изменения состояния термодинамической системы макроскопических тел при постоянном давлении называют изобарным.
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
Основная и дополнительная литература по теме урока:
Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. Физика. 10 класс. Учебник для общеобразовательных организаций М.: Просвещение, 2017. – С. 209 – 218.
Рымкевич А.П. Сборник задач по физике. 10-11 класс. — М.: Дрофа, 2009.
Открытые электронные ресурсы по теме урока:
Теоретический материал для самостоятельного изучения
Уравнение Клапейрона при m = const: отношение произведения давления и объёма к температуре есть величина постоянная для постоянной массы газа:
Если изменяется какой-либо макроскопический параметр газа постоянной массы, то два других параметра изменятся таким образом, чтобы указанное соотношение осталось постоянным.
Отношение произведения давления и объёма к температуре равно универсальной газовой постоянной для одного моля идеального газа.
Уравнение Менделеева при v = 1 моль
Произведение постоянной Больцмана и постоянной Авогадро называется универсальной газовой постоянной.

Уравнение состояния идеального газа получило название «уравнение Менделеева-Клапейрона».
Давление смеси химически невзаимодействующих газов равно сумме их парциальных давлений: закон Дальтона.
где pi– парциальное давление i-й компоненты смеси.
Парциальное давление – давление отдельно взятого компонента газовой смеси, равное давлению, которое он будет оказывать, если занимает весь объём при той же температуре.
Один моль любого газа при нормальных условиях занимает один и тот же объём равный:
V0=0,0224м 3 /моль=22,4дм 3 /моль.
Это утверждение называется законом Авогадро
Количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называют газовыми законами (изопроцессами).
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют изотермическим.
Для газа данной массы произведение давления на объём постоянна, если температура газа не меняется — закон Бойля – Мариотта.
Изотерма соответствующая более высокой температуре T1, лежит на графике выше изотермы, соответствующей более низкой температуре T2.
Если значения давления и температуры в различных точках объёма разные, то в этом случае газ находится в неравновесном состоянии.
Равновесное состояние — это состояние, при котором температура и давление во всех точках объёма одинаковы.
Процесс изменения состояния термодинамической системы макроскопических тел при постоянном давлении называют изобарным.
Для газа данной массы отношение объема к температуре постоянно, если давление не изменяется — закон Гей-Люссака.
Изобара соответствующая более высокому давлению p2 лежит на графике ниже изобары соответствующей более низкому давлению p1.
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
При данной массе газа отношение давление газа к температуре постоянно, если объем газа не изменяется — закон Шарля.
Изохора соответствующая большему объему V2 лежит ниже изохоры, соответствующей меньшему объему V1.
Примеры и разбор решения заданий
1. Установите соответствие между физическими величинами и приборами для их измерения. К каждой позиции первого столбца подберите нужную позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
Конспект урока: «Идеальный газ. Основное уравнение МКТ»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Физика 10 класс урок 27 12.12.17
Тема: Идеальный газ. Основное уравнение МКТ
сформировать представление о структуре и содержании новой физической теории;
организовать усвоение основных положений МКТ;
формирование умений описывать тепловые явления на молекулярно кинетических представлениях о строении вещества;
формировать мотивацию постановкой проблем и познавательных задач, раскрытием связи опыта и теории;
формировать умение анализировать факты при наблюдении явлений;
способствовать воспитанию познавательного интереса к физике, материалистического мировоззрения учащихся.
Организационный момент урока.
Постановка цели урока.
Мы с вами продолжаем изучение основ молекулярно- кинетической теории. На предыдущем уроке мы рассмотрели основные положения МКТ. Сегодня на уроке необходимо на основе МКТ установить количественную зависимость давления газа от массы одной молекулы и среднего квадрата скорости ее движения. Поэтому тема урока: «Идеальный газ. Основное уравнение МКТ»
Актуализация знаний.
Что такое молекулярно-кинетическая теория? Сформулируйте ее основные положения.
Какие наблюдения и эксперименты подтверждают основные положения молекулярно-кинетической теории?
Что называют броуновским движением? Каковы его особенности?
О чем свидетельствует броуновское движение?
Что называют диффузией? Приведите примеры диффузии в газах, жидкостях и твердых телах.
От чего зависит скорость диффузии? О чем свидетельствует явление диффузии?
Изучение нового материала.
1. Макроскопические параметры. Идеальный газ.
Состояние газа (так же как жидкости и твердого тела) может быть описано и без рассмотрения молекулярного строения вещества. Это делают с помощью макроскопических величин, совокупность которых однозначно определяет состояние системы. Такие величины называют параметрами состояния (или термодинамическими параметрами). Параметрами состояния любой системы являются ее объем, давление и температура. Если в каком-либо процессе изменяется хотя бы один из параметров состояния системы, то и само состояние системы становится другим.
Величины, характеризующие состояние макроскопических тел без учета их внутреннего строения называются макроскопическими параметрами.
Идеальный газ – это модель реального газа, которая обладает следующими свойствами:
Молекулы пренебрежимо малы по сравнению со средним расстоянием между ними.
Молекулы ведут себя подобно маленьким твердым шарикам: они упруго сталкиваются между собой и со стенками сосуда, никаких других взаимодействий между ними нет.
Молекулы находятся в непрекращающемся хаотическом движении.
Все газы при не слишком высоких давлениях и при не слишком низких температурах близки по своим свойствам к идеальному газу. При высоких давлениях молекулы газа настолько сближаются, что пренебрегать их собственными размерами нельзя. При понижении температуры кинетическая энергия молекул уменьшается и становится сравнимой с их потенциальной энергией, следовательно, при низких температурах пренебрегать потенциальной энергией нельзя.
При высоких давлениях и низких температурах газ не может считаться идеальным. Такой газ называют реальным. (Поведение реального газа описывается законами, отличающимися от законов идеального газа.)
2. Давление газа. Основное уравнение МКТ газа.
Давление газа определяется столкновением молекул газа со стенками сосуда.
В СИ за единицу давления принимают 1 Па.
Давление, при котором на площадь 1 м 2 действует сила давления в 1 Н, называется Паскалем.
1мм.рт.ст. = 133 Па
Одной из основных задач молекулярно-кинетической теории газа является установление количественных соотношений между макроскопическими параметрами, характеризующими состояние газа (давлением, температурой), и величинами, характеризующими хаотическое тепловое движение молекул газа (скоростью молекул, их кинетической энергией). Одним из таких соотношений является зависимость между давлением идеального газа и средней кинетической энергией поступательного движения его молекул. Эту зависимость называют основным уравнением молекулярно-кинетической теории идеального газа:

где р — давление газа; n — концентрация молекул газа (число его молекул в единичном объеме): m 0 — масса молекулы газа, 

Давление идеального газа пропорционально средней кинетической энергии поступательного движения молекул и концентрации молекул.
Это давление тем больше, чем больше средняя кинетическая энергия поступательного движения молекул.
Средней квадратической скоростью называют величину, равную корню квадратному из среднего арифметического значения квадратов скоростей N молекул газа:
Средней кинетической энергией поступательного движения молекул идеального газа называют величину

Из этой формулы видно, что средняя кинетическая энергия поступательного движения молекул газа пропорциональна абсолютной температуре.
10В этой формуле k=1,38 -23 Дж/К – постоянная Больцмана.
Давление газа зависит от концентрации молекул. Эта зависимость выражается формулой:
Давление газа не зависит от его природы, а определяется только концентрацией молекул и температурой газа.
Численное значение средней квадратичной скорости получим из формулы


При одинаковых давлениях и температурах концентрация молекул всех газов одинакова. В частности, при нормальных условиях
n = N л 10= 2,7 25 м- 3 .
Величину N л называют числом Лошмидта, оно равно количеству молекул идеального газа, содержащихся в 1 м 3 газа при нормальных условиях.
6.Закрепление материала:
А) Вопросы для фронтального опроса:
Что такое макроскопические параметры?
Какой газ называют идеальным? Что является моделью идеального газа?
При каких условиях газ по своим свойствам близок к идеальному? При каких условиях и почему газ не может считаться идеальным?
Что называют абсолютным нулем температуры? Каков физический смысл этого понятия с точки зрения молекулярно-кинетической теории?
Чему равно давление идеального газа на стенки камеры при абсолютном нуле температуры?
Б) Решение количественных задач:
Задача №1.
Найти концентрацию молекул кислорода, если его давление 0,2 МПа, а средняя квадратичная скорость молекул равна 700 м/с.
υ=700 м/с
M =32·10 — 3 кг/моль n=р/κТ
n=? n=3N а р /υ 2 М = 2,3·10 25 .
Подведение итогов урока.
8. Домашнее задание: § 63-65, упр. 11(10).
http://resh.edu.ru/subject/lesson/6292/conspect/
http://infourok.ru/konspekt-uroka-idealniy-gaz-osnovnoe-uravnenie-mkt-3077817.html