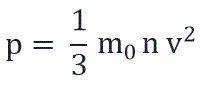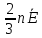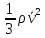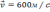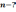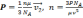Основное уравнение мкт идеального газа задачи егэ
Среднюю кинетическую энергию теплового движения молекул разреженного газа уменьшили в 2 раза и концентрацию молекул газа уменьшили в 2 раза. Чему равно отношение конечного давления к начальному?
Давление разреженного газа пропорционально произведению концентрации молекул газа и средней кинетической энергии теплового движения, например, для одноатомного газа:
При одновременном уменьшении средней кинетической энергии теплового движения в два раза и концентрации молекул в два раза давление разреженного газа уменьшится в 4 раза.
Концентрацию молекул одноатомного идеального газа уменьшили в 5 раз. Одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. Чему равно отношение конечного давления к начальному?
Давление одноатомного идеального газа пропорционально произведению концентрации молекул газа и средней энергии хаотического движения:
При увеличении средней энергии теплового движения в два раза и уменьшении концентрации молекул в пять раз конечное давление одноатомного идеального газа составит от начального.
Практическая работа по теме: Решение задач на применение основного уравнения МКТ
Цель: Научиться применять основное уравнение МКТ при решении задач.
Просмотр содержимого документа
«Практическая работа по теме: Решение задач на применение основного уравнения МКТ»
Практическая работа № 5
Решение задач на применение основного уравнения МКТ
Цель: Научиться применять основное уравнение МКТ при решении задач.
Физический смысл основного уравнения МКТ заключается в том, что давление идеального газа — это совокупность всех ударов молекул о стенки сосуда. Это уравнение можно выразить через концентрацию частиц, их среднюю скорость и массу одной частицы:
P =
P =
p – давление молекул газа на границы емкости,
m0 – масса одной молекулы,
n — концентрация молекул, число частиц N в единице объема V;
v 2 — средне квадратичная скорость молекул.
Как известно из законов динамики, кинетическая энергия любого тела или частицы. Заменив произведение массы каждой из частичек и квадрата их скорости в записанном нами уравнении, мы можем представить его в виде:
Также кинетическая энергия газовых молекул выражается формулой, что нередко используется в задачах. Здесь k – это постоянная Больцмана, устанавливающая связь между температурой и энергией. k=1,38•10 -23 Дж/К.
Основное уравнение МКТ лежит в основе термодинамики.
Средняя квадратичная скорость молекул азота 600 м/с. Если его давление 0,28 МПа, то концентрация молекул равна….
P = 0,28 МПа = 28*10 4 Па
Основное уравнение молекулярно-кинетической теории:
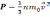
Зная число Авогадро, массу одной молекулы m0 выразим как:
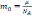
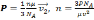
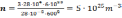
Ответ: 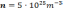
Задания для аудиторной работы
1.Найти температуру газа при давлении 100 кПа и концентрации молекул
2. Каково давление газа, если в каждом см³ его содержится 10 6 молекул, а температура 87°С?
3. В сосуде находится газ. Какое давление он производит на стенки сосуда, если масса газа 5 г, его объем 1 л, средняя квадратичная скорость молекул 500 м/с?
4. Определите давление водорода, если средняя квадратичная скорость его молекул 800 м/с, а его плотность 2.4 кг/м³.
5. Какова скорость теплового движения молекул, если при давлении 250 кПа газ массой 8 кг занимает объем 15 м³.
6. Определить число молекул водорода в 1 м³, если давление равно 200 мм РТ. Столба, а средняя квадратичная скорость его молекул равна 24000 м/с.
7. Определите среднюю квадратичную скорость молекул газа, плотность которого при давлении р = 50 кПа составляет ρ = 4.1·10‾² кг/м³.
8. Чему равны средняя квадратичная скорость и средняя энергия поступательного движения молекул азота, если 2.5 кг его, занимая объем 3.2 м³, производит давление 2.5·10 5 Па?
1. Определите температуру газа, если средняя кинетическая энергия поступательного движения его молекул равна 1.6·10‾ 19 Дж.
2. Сколько молекул газа находится в сосуде вместимостью 480 см³ при температуре 20°С и давлении 2.5·10 4 Па?
3. Определите давление азота в ампуле, если в 1м³ находится 3.5·10 14 молекул, средняя скорость теплового движения которых равна 490 м/с.
4. Определите концентрацию молекул водорода при давлении 100 кПа, если среднее значение скорости теплового движения молекул равно 450 м/с.
5. Средняя энергия молекулы идеального газа равна 6.4·10‾²¹ Дж. Давление газа 4 мПа. Найти число молекул газа в единице объема.
6. Чему равны средняя квадратичная скорость и средняя энергия поступательного движения молекул азота, если 2.5 кг его, занимая объем 3.2 м³, производит давление 2.5·10 5 Па?
7. Определить среднюю кинетическую энергию Ек поступательного движения молекул газа, находящегося под давлением 0.2 Па. Концентрация молекул газа равна 10 14 см‾³.
8. Определите среднюю квадратичную скорость молекул газа, плотность которого при давлении р = 50 кПа составляет ρ = 4.1·10‾² кг/м³.
Основное уравнение мкт идеального газа задачи егэ
Основное уравнение МКТ .
\(p\) — Давление газа
\(m_0\) — масса молекулы газа
\(n\) -концентрация молекул газа
\(\bar
Это уравнение связывает макроскопический параметр давление с микроскопическими параметрами: массой молекулы и среднеквадратичной скоростью молекул
макроскопические параметры это то что мы можем увидеть глазами или измерить прибором
Мы живем в макромире
Молекулы мы не можем пощупать, увидеть или измерить их скороть, они находятся в микромире
Попробуем преобразовать наше уравнение, используя формулу кинетической энергии:
\(p=\dfrac<1> <3>m_0 n \bar
это тоже основное уравнение МКТ
Другие формулы этой темы:
\(k\) — постоянная Больцмана
Эта формула связывает среднюю кинетическую энергию молекулы с температурой в градусах Кельвина
Задача 1.(Основное уравнение МКТ) .формула \(p= \dfrac<2> <3>n \bar < E_к>\)
Найти давление газа в баллоне, если концентрация молекул газа \(n=10^ <26>м^ <-1>\), а средняя кинетическая энергия молекул газа \(\bar< E_к>=3 \cdot 10^ <-21>Дж \)
Показать ответ Показать решение Видеорешение
Ответ: \( p= 200000Па \)
Запишем основное уравнение МКТ в преобразованном виде:
\(p= \dfrac<2> <3>\cdot 10^ <26>м^ <-1>3 \cdot 10^ <-21>Дж=2 \cdot 10^ <5>Па=200000Па\)
http://multiurok.ru/files/praktichieskaia-rabota-po-tiemie-rieshieniie-zad-1.html
http://kornev-school.ru/f10_basic_equation_of_molecular_kinetic_theory.html