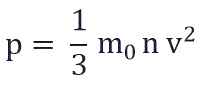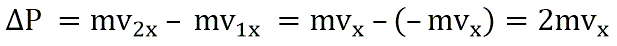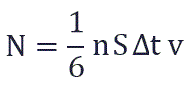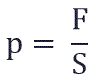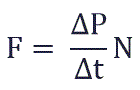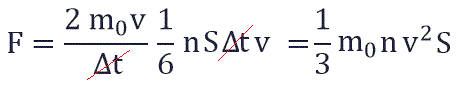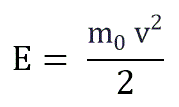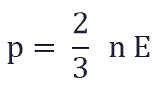Основное уравнение молекулярно-кинетической теории (МКТ) с выводом
В статье рассмотрена модель идеального газа, приведено основное уравнение молекулярно-кинетической теории и его вывод.
Чтобы объяснить свойства материи в газообразном состоянии, в физике применяется модель идеального газа. Идеальный газ — разреженный, состоящий из одного типа атомов газ, частицы которого не взаимодействуют между собой. Помимо основных положений МКТ эта модель предполагает, что:
- молекулы имеют пренебрежимо малый объем в сравнении с объемом емкости
- при сближении частиц друг с другом и с границами емкости имеют место силы отталкивания
Основное уравнение молекулярно-кинетической теории
Физический смысл основного уравнения МКТ заключается в том, что давление идеального газа — это совокупность всех ударов молекул о стенки сосуда. Это уравнение можно выразить через концентрацию частиц, их среднюю скорость и массу одной частицы:
p – давление молекул газа на границы емкости,
m0 – масса одной молекулы,
n — концентрация молекул, число частиц N в единице объема V;
v 2 — средне квадратичная скорость молекул.
Вывод основного уравнения МКТ
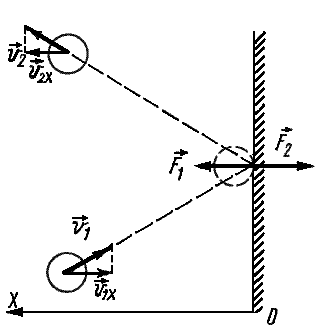
Частицы идеального газа при соударениях с границами емкости ведут себя как упругие тела. Такое взаимодействие описывается согласно законам механики. При соприкосновении частицы с границей емкости проекция vx скоростного вектора на ось ОХ, проходящую под прямым углом к границе сосуда, меняет свой знак на противоположный, но сохраняется неизменной по модулю:
Поэтому после соударения частицы с границей емкости проекция импульса молекулы на ось ОХ меняется с mv1x = –mvx на mv2x = mvx.
Изменение импульса молекулы ΔP равняется удвоенному произведению массы молекулы на ее скорость:
Поскольку в каждом из шести основных направлений декартовой системы координат (вверх, вниз, вперед, назад, вправо, влево) движется одна шестая часть частиц N/6. Тогда число частиц, которые сталкиваются с каждой стенкой за время Δt равно:
S – площадь этой стенки
n — концентрация частиц
Давление p равно отношению силы F к площади S, на которую действует эта сила:
Суммарная сила, с которой частицы давят на стенку равна отношению произведения числа этих частиц N и изменения импульса ΔP ко времени, в течение которого происходит давление:
Исходя из вышенаписанного получаем:
Если заменить среднее значение кинетической энергии поступательного движения молекул — E:
и подставить эту формулу в основное уравнение МКТ, получим давление идеального газа:
Давление идеального газа равняется двум третям средней кинетической энергии поступательного движения молекул на единицу объема. При решении задач реальный газ можно считать идеальным газом, если он одноатомный и можно пренебречь взаимодействием между частицами.
Понравилась статья, расскажите о ней друзьям:
Основное уравнение молекулярно-кинетической теории газов

Средняя оценка: 4.6
Всего получено оценок: 88.
Средняя оценка: 4.6
Всего получено оценок: 88.
Основное уравнение молекулярно-кинетической теории газов связывает макроскопический параметр газа — давление — с параметрами молекул. Рассмотрим кратко вывод этого уравнения.
Основные положения МКТ
Молекулярно-кинетическая теория (МКТ) описывает тепловые явления на основе положений о строении вещества. Таких положений три:
- все вещества состоит из мельчайших частиц-молекул;
- молекулы находятся в постоянном хаотическом движении;
- частицы могут взаимодействовать друг с другом.
В зависимости от скорости движения молекул и от вида их взаимодействий, вещества находятся в различном температурном и агрегатном состоянии.
Давление идеального газа
Одним из объектов, который хорошо описывается с помощью МКТ, является идеальный газ.
В идеальном газе молекулы представляют собой материальные точки, которые хаотически движутся в предоставленном объеме, сталкиваясь друг с другом и со стенками сосуда. Столкновения абсолютно упруги, и других взаимодействий между молекулами нет.

Учитывая основные положения МКТ газов, становится возможным связать величину давления с параметрами его молекул. В упрощенном виде ход рассуждений будет таким.
Для определения давления учтем, что, если средняя скорость молекулы равна $v_<ср>$, то импульс, переданный ею при абсолютно упругом ударе о стенку сосуда, равен:
Если концентрация молекул равна $n$, то количество ударов молекул о стенку сосуда площадью $S$ за время $t$ равно:
А полный импульс силы, подействовавший на стенку, равен:
Из двух последних формул найдем силу:
Поскольку в ударах о стенку сосуда участвовали лишь молекулы, имеющие составляющую скорости, перпендикулярную стенке и направленную в ее сторону, то в среднем импульс передавала только одна шестая молекул (в трехмерном пространстве молекулы могут двигаться в шести направлениях). Следовательно, среднее значение силы в шесть раз меньше полученного значения:
Поделив полученное значение силы на площадь, получим создаваемое ею давление:
Полученная формула — это и есть основное уравнение молекулярно-кинетической теории газов.
Иногда основное уравнение МКТ записывается с использованием средней кинетической энергии молекулы. Средняя кинетическая энергия равна:
Выражая среднеквадратичную скорость из этой формулы и подставляя ее в предыдущую, получим:
Давление идеального газа пропорционально концентрации и средней кинетической энергии молекулы.
Что мы узнали?
Основное уравнение молекулярно-кинетической теории идеального газа связывает макроскопический параметр газа — давление — с параметрами его молекул: с концентрацией, массой и средней скоростью. Поскольку масса и средняя скорость молекулы однозначно определяют среднюю энергию молекулы, основное уравнение МКТ можно записать с помощью средней энергии.
Основное уравнение молекулярно-кинетической теории (Ерюткин Е.С.)
Этот видеоурок доступен по абонементу
У вас уже есть абонемент? Войти
Как уже было сказано ранее, начиная с этого урока, мы приступаем к изучению только газов. На прошлом уроке мы дали представление о способах количественного описания некой порции вещества. Сейчас же мы начнём описывать газ со стороны его качественных характеристик (микро- и макропараметров). Мы сформулируем понятие об идеальном газе, опишем его параметры и введём соотношение, связывающее эти параметры (основное уравнение МКТ).
http://obrazovaka.ru/fizika/osnovnoe-uravnenie-molekulyarno-kineticheskoy-teorii-gazov.html
http://interneturok.ru/lesson/physics/10-klass/osnovy-molekulyarno-kineticheskoy-teorii/osnovnoe-uravnenie-molekulyarno-kineticheskoy-teorii-2