Научная работа по химии на тему: Классификация химических реакций
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
1 ВАРИАНТ 1.Укажите схемы реакций соединения:
2.Укажите схемы реакций, для проведения которых обязательно используется катализатор:
3.Отметьте уравнения или схемы реакций разложения:
3) NaOH + HCl = NaCl + H2O;
3.Укажите уравнения или схемы реакций замещения:
4.Отметьте уравнения или схемы экзотермических реакций:
4) CaCO3 = CaO + CO2 + 157 кДж .
5.Укажите уравнения или схемы реакций обмена:
6.Число продуктов всегда меньше числа исходных веществ в случае реакций:
7.Отметьте уравнения или схемы окислительно-восстановительных реакций:
8.Укажите уравнения или схемы необратимых реакций:
3) NaOH + HCl = NaCl + H 2 O ;
9.Число продуктов всегда больше числа исходных веществ в случае реакций:
10.Окислительно-восстановительной в неорганической химии всегда является реакция:
2 ВАРИАНТ1.В неорганической химии реакция замещения протекает:
1) между двумя простыми веществами;
2) двумя сложными веществами;
3) простым и сложным веществами;
4) как двумя простыми, так и двумя сложными веществами.
2.Окислительно-восстановительными могут быть реакции:
3.Без изменения степени окисления атомов элементов всегда протекают реакции:
4.В реакцию обмена между собой могут вступать вещества:
1) простое и сложное;
4) как два простых, так и два сложных.
5.В результате реакции разложения могут образоваться:
1) только простые вещества;
2) только сложные вещества;
3) или только простые, или только сложные вещества;
4) одновременно простые и сложные вещества.
6. реакцию соединения между собой могут вступать вещества:
1) только простые;
2) только сложные;
3) как простые, так и сложные;
4) простое со сложным.
7.Укажите справедливые утверждения:
1) в результате реакции разложения образуется не более двух новых веществ;
2) в реакции обмена число различных по составу продуктов всегда равно числу различных по составу исходных веществ;
3) в реакции соединения число различных по составу исходных веществ всегда больше, чем продуктов;
4) в неорганических реакциях замещения число различных по составу исходных веществ равно числу различных по составу продуктов.
8.Укажите схему или уравнение окислительно-восстановительной реакции разложения:
9.Отметьте уравнения или схемы окислительно-восстановительных реакций соединения:
10.Укажите схемы или уравнения окислительно-восстановительных реакций замещения:
3-Вариант 1.Реакция НЕ может быть одновременно:
1) обмена и окислительно-восстановительной;
2) окислительно-восстановительной и разложения;
3) замещения и окислительно-восстановительной;
4) соединения и окислительно-восстановительной.
2.Гомогенными могут быть:
1) только реакции обмена;
2) только реакции соединения;
3) только реакции разложения;
4) все вышеназванные реакции, а также реакции замещения.
3.Одна и та же реакция может быть одновременно:
а) обратимой и экзотермической;
б) замещения и обмена;
в) обмена и разложения;
г) соединения и разложения..
4.Отметьте уравнения или схемы гомогенных реакций соединения:
4.Укажите уравнения или схемы гомогенных окислительно-восстановительных реакций разложения:
5.Отметьте уравнения или схемы гетерогенных окислительно-восстановительных реакций:
6.Укажите схемы или уравнения гомогенных экзотермических реакций обмена :
1) NaOH (p-p) + HCl (p-p) = NaOH (p-p) + H2O (ж) + Q;
7.Даны схемы (уравнения) реакций получения SO2. Из них гетерогенными окислительно-восстановительными будут реакции:
8.Даны реакции: а) обжиг пирита; б) обжиг известняка; в) фотосинтез; г) взаимодействие водных растворов сульфата натрия и хлорида бария. Окислительно-восстановительными из перечисленных будут реакции:
9.Для описания реакции нейтрализации подходят признаки:
1) всегда гомогенная;
3) продукты — как правило, соль и вода;
4) может быть гомогенной и гетерогенной.
10.Даны вещества, формулы которых Zn, ZnO, Zn(OH)2, ZnCO3, SO2. Укажите число веществ, которые могут реагировать с H2SO4 (разб.) по типу реакции обмена:
Курс повышения квалификации
Охрана труда
- Сейчас обучается 120 человек из 44 регионов
Курс профессиональной переподготовки
Охрана труда
- Сейчас обучается 236 человек из 54 регионов
Курс профессиональной переподготовки
Библиотечно-библиографические и информационные знания в педагогическом процессе
- Сейчас обучается 353 человека из 64 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 593 176 материалов в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
«Психологические методы развития навыков эффективного общения и чтения на английском языке у младших школьников»
Свидетельство и скидка на обучение каждому участнику
Другие материалы
- 31.12.2020
- 2842
- 0
- 31.12.2020
- 3541
- 1
- 31.12.2020
- 4080
- 0
- 31.12.2020
- 4527
- 9
- 31.12.2020
- 3899
- 0
- 31.12.2020
- 3771
- 0
- 31.12.2020
- 4460
- 0
- 31.12.2020
- 3895
- 0
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 15.07.2020 618
- DOCX 21.1 кбайт
- 2 скачивания
- Рейтинг: 1 из 5
- Оцените материал:
Настоящий материал опубликован пользователем Колесникова Юлия Викторовна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 1 год и 2 месяца
- Подписчики: 0
- Всего просмотров: 26825
- Всего материалов: 229
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Минобрнауки создаст для вузов рекомендации по поддержке молодых семей
Время чтения: 1 минута
Курские власти перевели на дистант школьников в районах на границе с Украиной
Время чтения: 1 минута
В приграничных пунктах Брянской области на день приостановили занятия в школах
Время чтения: 0 минут
В ростовских школах рассматривают гибридный формат обучения с учетом эвакуированных
Время чтения: 1 минута
В Белгородской области отменяют занятия в школах и детсадах на границе с Украиной
Время чтения: 0 минут
Каждый второй ребенок в школе подвергался психической агрессии
Время чтения: 3 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
1.Укажите схемы реакций соединения:
1) Fe(OH)3 → Fe2O3 + H2O;
2) AgNO3 → Ag + NO2 + O2;
4) NO2 + O2 + H2O → HNO3.
2.Укажите схемы реакций, для проведения которых обязательно используется катализатор:
1) KOH + H2SO4 → K2SO4 + H2O;
3) NH3 + O2 → NO + H2O;
4) NH3 + O2 → N2 + H2O.
3.Отметьте уравнения или схемы реакций разложения:
1) HNO3 → H2O + NO2 +O2;
2) Fe + Cu(NO3)2 = Fe(NO3)2 + Cu;
3) NaOH + HCl = NaCl + H2O;
4) H2O2 → H2O + O2.
4.Укажите уравнения или схемы реакций замещения:
1) Zn + 2AgNO3 = Zn(NO3)2 + 2Ag;
2) Fe + H2SO4 = FeSO4 + H2;
3) CaCl2 + Na2CO3 = CaCO3 + 2NaCl;
4) CuO + H2 → Cu + H2O.
5.Отметьте уравнения или схемы экзотермических реакций:
1) N2 + H2 → NH3 + Q;
2) SO2 + O2 + Q → SO3;
3) C + O2 = CO2 + 369 кДж;
4) CaCO3 = CaO + CO2 + 157 кДж.
6.Укажите уравнения или схемы реакций обмена:
1) NaOH + H2SO4 → Na2SO4 + H2O;
2) Ba(NO3)2 + K2SO4 → BaSO4 + KNO3;
3) N2O5 + H2O → HNO3;
4) CuO + 2HNO3 = Cu(NO3)2 + H2O.
7.Число продуктов всегда меньше числа исходных веществ в случае реакций:
Гомогенные реакции: описание и примеры
Для правильного проведения химических реакций важно знать, в каких условиях они протекают. Гомогенная среда реагентов позволяет определять скорость их взаимодействия. Существуют особые факторы, которые могут замедлять или ускорять гомогенные реакции.
Классификация
Химические взаимодействия можно разделить на разные группы, благодаря присутствию большого числа критериев.
Существуют следующие признаки:
- Наличие раздела реакционной фазы. Реакции могут быть гомогенными или гетерогенными.
- Изменение окислительной степени реагирующих веществ.
- Выделение или поглощение тепла.
- Тип изменений реагирующих веществ, связанных с соединением, разложением, замещением или обменом.
Гомогенная среда
Это однородная система, в которой химические и физические характеристики компонентов в любой ее точке постоянны, а если они изменяются, то в непрерывном темпе, без проявления резких скачков. Все ее части не имеют поверхностного разделения. Так протекают гомогенные химические реакции.
Наличие нескольких реагентов в однородной фазе нельзя визуально определить или отделить их механическим способом. Такая особенность возможна благодаря равномерному распределению составных частиц одного компонента в другом.
К примерам однородных фаз следует отнести газовые смеси, замерзшую воду, растворы в жидкой или твердой форме.
Определение гомогенных взаимодействий
Их еще называют гомофазными реакциями. Это процессы, протекающие в области одной однородной среды, а реагирующие компоненты и получаемые продукты находятся в неизменном состоянии.
Гомогенные реакции имеют величины, которые остаются в одинаковых показателях, а если они меняются, то с непрерывной скоростью.
Когда процессы проходят в области разделения двух фаз, то их называют гетерогенными.
Если реакции многостадийные, то они могут быть смешанного типа. В них начальные этапы протекают в гомогенной среде, а конечные процессы в гетерогенной фазе. Такие взаимодействия чаще всего происходят в природе.
Гомогенные реакции, примеры уравнений
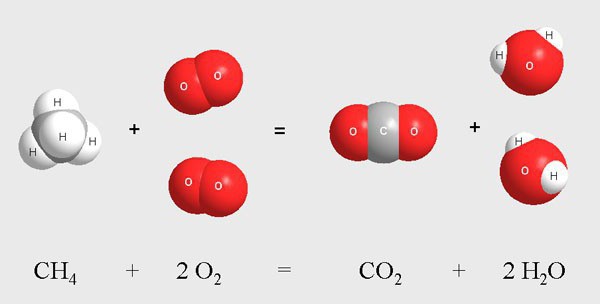
К ним относят процесс хлорирования молекул метана в газовой среде. Данная реакция протекает при высокой температуре или при воздействии ультрафиолета. В результате смешивания метана и хлора происходит поэтапное взаимодействие экзотермического типа.
Промежуточными продуктами являются газообразные вещества, к которым относят молекулы хлорметана, дихлорметана, трихлорметана, хлороводорода. Во время реакции происходит постепенное замещение атомов водорода в метане на атомы хлора. Конечным веществом служит четыреххлористый углерод.
Существуют и одноэтапные гомогенные реакции. Примеры таких взаимодействий указаны ниже.
К гомофазным процессам можно отнести:
- расщепление оксида пятивалентного азота в газовой среде под действием высокой температуры: N2O5↑ + N2O5↑ → NO2 + NO2 + NO2 + NO2 + O2;
- нейтрализацию раствором гидроксида натрия раствора соляной кислоты, с образованием раствора хлорида натрия и воды: HCl + NaOH → NaCl + H2O;
- этановое горение с выделением оксида четырехвалентного углерода и водяного пара: С2Н 6↑ + С2Н 6↑ + 7О2↑ → 4СО2↑ + 6Н2О↑;
- превращение молекулярного кислорода во время грозы в озон: 3О2↑ → 2О3↑.
Гомогенные реакции достаточно часто протекают в жидкой среде. К ним причисляют процессы галоидирования, расщепления всевозможных сложных соединений на более простые или на радикалы, замещение одних атомов другими по нуклеофильному или электрофильному типу, отщепление частей молекулы или их перегруппировка, удлинение цепочки за счет полимеризации, окислительное взаимодействие. В результате образуются жидкие продукты.
Скорость реакций гомогенных
Протекание того или иного процесса может занимать разные временные промежутки. Важной характеристикой такого взаимодействия является скорость гомогенной реакции. Представляет она числовую величину, которая определяет изменение концентрации любого реагента за временной промежуток.
Ее можно охарактеризовать по-другому: как значение, устанавливающее перемену количества взаимодействующего компонента в заданном объеме за определенное время. Главным условием является отсутствие изменения массы в системе.
При расчете скорости реакции в гомогенной среде (обозначают как Vi) используют убыль или прирост молярного количества реагирующего вещества (Ci) за определенное время (t). Существует специальная формула расчета:
Для химического процесса HCl + NaOH → NaCl + H2O быстроту протекания можно определить по уменьшению концентрации каждого реагента (соляной кислоты или натрия гидроксида) или по увеличению количества продуктов превращения (натрия хлорида или воды) за временной промежуток при постоянных температурных условиях.
Для определения скорости гомогенных реакций концентрацию берут в молях на литр, а время измеряют в секундах. Расчет производится следующим образом:
Vi = ± Ci / t = − [HCl] / t = − [NaOH] / t = [NaCl] / t = [H2O] / t.
Факторы, влияющие на скорость
Гомогенной является реакция, у которой быстрота протекания данного процесса прямо пропорциональна заданному веществу в единице объема. Чем больше молекул задействовано, тем быстрее осуществляется взаимодействие.
Основными факторами, влияющими на скорость процессов в однородной среде, являются концентрация реагентов и продуктов реакции, их химическая природа, температурные условия, давление в реакционном объеме, а также наличие ускорителей, катализирующих изменения.
Зависимость быстроты протекания реакций от нагревания была установлена ученым Вант-Гоффом. Согласно его утверждению, каждое температурное повышение на 10° увеличивает в гомогенных реакциях скорость в 2 или 4 раза. В более теплой среде молекулы начинают активнее двигаться, сталкиваться друг с другом, что приводит к их взаимодействию.
Гомогенные реакции со временем протекают с разной интенсивностью, поэтому их скорости могут быть истинными (в определенный момент) и средними, что следует учитывать при расчетах.
http://znanija.org/himiya/36027340.html
http://www.syl.ru/article/236404/new_gomogennyie-reaktsii-opisanie-i-primeryi