Вопрос 2. Параметры состояния и уравнения состояния.
Вопрос 2. Параметры состояния и уравнения состояния.
Параметры состояния — физические величины, характеризующие внутреннее состояние термодинамической системы. Параметры состояния термодинамической системы подразделяются на два класса: интенсивные (не зависят от массы системы) и экстенсивные (пропорциональны массе).
Термодинамическими параметрами состояния называются интенсивные параметры, характеризующие состояние системы. Простейшие параметры:
1. 
2. 
3. 
4. 
Связь между параметрами, характеризующими состояние простого тела, называется уравнением состояния F (р, v, T) = 0.
Изменение состояния системы называется процессом.
Равновесный процесс — это непрерывная последовательность равновесных состояний системы.
Обратимый процесс — равновесный процесс, который допускает возможность возврата этой системы из конечного состояния в исходное путем обратного процесса.
Термодинамическим процессомпринято считать обратимый равновесный процесс.
Равновесные процессы могутбыть изображены графически на диаграммах состояния p-v, р-Т и т. д. Линия, изображающая изменение параметров в процессе, называется кривой процесса. Каждая точка кривой процесса характеризует равновесное состояние системы.
Уравнение термодинамического процесса – уравнение вида 
Уравнение состояния для простого тела — 
Идеальный газ – совокупность материальных точек (молекул или атомов), находящихся в хаотическом движении. Эти точки рассматриваются как абсолютно упругие тела, не имеющие объёма и не взаимодействующие друг с другом. Уравнением состояния идеального газа является уравнение Менделеева-Клапейрона:
PV=nRT, где P – давление, [Па]; V – объём системы [м 3 ]; n – количество вещества, [моль]; T – термодинамическая температура, [К]; R – универсальная газовая постоянная.
Реальный газ – газ, молекулы которого взаимодействуют друг с другом и занимают определённый объём. Уравнением состояния реального газа является обобщённое уравнение Менделеева-Клапейрона:

_____________________________________________________________
Вопрос 3. Термодинамическая работа, координаты P-V.
Термодинамическая работа: 


Удельная работа: 


— Если 


— Если 


— При малом изменении объёма давление практически не изменяется.


1. В случае если 

2. В случае если дано уравнение процесса — 




Вопрос 4. Потенциальная работа, координаты P-V, распределение работы.
Потенциальная работа – работа, вызываемая изменением давления.

— Если 

— Если 

— При малом изменении давления объём почти не меняется.


1. В случае если 

2. В случае если дано уравнение процесса — 



переданная внешним системам.

________________________________________________________
Вопрос 16. Изобарный процесс изменения состояния простого тела. Уравнение процесса, изображение в координатах P-V, связь между параметрами, работа и теплообмен, изменение функций состояния.
Если 







Так как 

Для идеального газа:
Первое начало термодинамики: 
Для идеального газа: 







Вопрос 63. Дросселирование. Эффект Джоуля-Томсона. Основные понятия
Дросселирование – процесс движения вещества через внезапное сужение. Причинами возникновения местных сопротивлений при движении потока рабочего тела по каналам могут быть запорные, регулирующие и измерительные устройства; повороты, сужение, загрязнение каналов и т.д.
Эффект Джоуля-Томсона — изменение температуры вещества при адиабатном дросселировании.
Рис. 1.7. Процесс дросселирования в h-s диаграмме
Различают дифференциальный и интегральный дроссель – эффекты. Величина дифференциального дроссель – эффекта определяется из соотношения


Интегральный дроссель-эффект: 
Коэффициент Джоуля – Томсона выводится из математических выражений первого начала термодинамики и второго начала термостатики
1. Если дроссель–эффект положительный (Dh > 0), то снижается температура рабочего тела (dT 0);
3. Если дроссель–эффект равен нулю (Dh = 0), то температура рабочего тела не изменяется. Состояние газа или жидкости, которому соответствует условие Dh = 0, называется точкой инверсий.
___________________________________________________________________
Двухтактный дизель
Рабочий процесс в двухтактном дизеле в основном протекает так же как и в двухтактном карбюраторном двигателе, и отличается только тем что продувка цилиндра производится чистым воздухом. По окончании ее оставшийся в цилиндре воздух сжимается. В конце сжатия через форсунку впрыскивается топливо в камеру сгорания и воспламеняется.Схема двухтактного дизеля с кривошипно-камерной продувкой показана на рисунке 14, а, а индикаторная диаграмма — на рисунке 14, 6.
Рабочий процесс в двухтактном дизеле протекает следующим образом.
Первый такт. При движении поршня вверх от н. м. т. к в. м. т. вначале происходит окончание продувки, а затем окончание выпуска. На индикаторной диаграмме продувка изображена линией b»— a» а выпуск — а» — а.
После закрытия выпускного окна поршнем в цилиндре происходит сжатие воздуха. Линия сжатия на индикаторной диаграмме изображена кривой а—с. В это время под поршнем в кривошипной камере создается разрежение, под действием которого автоматический клапан открывается, и в кривошипную камеру засасывается чистый воздух. В начале движения поршня вниз, вследствие уменьшения объема под поршнем, давление воздуха в кривошипной камере повышается, и клапан закрывается.
Второй такт. Поршень движется от в. м. т. к н. м. т. Впрыск и горение топлива начинаются перед концом сжатия и заканчиваются после того, как поршень пройдет в. м. т. По окончании горения происходит расширение. Протекание процесса расширения на индикаторной диаграмме изображено кривой r-b.
Остальные процессы, выпуск и продувка протекают так же, как и в карбюраторном двухтактном двигателе.
Вопрос 2. Параметры состояния и уравнения состояния.
Параметры состояния — физические величины, характеризующие внутреннее состояние термодинамической системы. Параметры состояния термодинамической системы подразделяются на два класса: интенсивные (не зависят от массы системы) и экстенсивные (пропорциональны массе).
Термодинамическими параметрами состояния называются интенсивные параметры, характеризующие состояние системы. Простейшие параметры:
1. 
2. 
3. 
4. 
Связь между параметрами, характеризующими состояние простого тела, называется уравнением состояния F (р, v, T) = 0.
Изменение состояния системы называется процессом.
Равновесный процесс — это непрерывная последовательность равновесных состояний системы.
Обратимый процесс — равновесный процесс, который допускает возможность возврата этой системы из конечного состояния в исходное путем обратного процесса.
Термодинамическим процессомпринято считать обратимый равновесный процесс.
Равновесные процессы могутбыть изображены графически на диаграммах состояния p-v, р-Т и т. д. Линия, изображающая изменение параметров в процессе, называется кривой процесса. Каждая точка кривой процесса характеризует равновесное состояние системы.
Уравнение термодинамического процесса – уравнение вида 
Уравнение состояния для простого тела — 
Идеальный газ – совокупность материальных точек (молекул или атомов), находящихся в хаотическом движении. Эти точки рассматриваются как абсолютно упругие тела, не имеющие объёма и не взаимодействующие друг с другом. Уравнением состояния идеального газа является уравнение Менделеева-Клапейрона:
PV=nRT, где P – давление, [Па]; V – объём системы [м 3 ]; n – количество вещества, [моль]; T – термодинамическая температура, [К]; R – универсальная газовая постоянная.
Реальный газ – газ, молекулы которого взаимодействуют друг с другом и занимают определённый объём. Уравнением состояния реального газа является обобщённое уравнение Менделеева-Клапейрона:

_____________________________________________________________
Уравнение состояния вещества
Параметры состояния связаны друг с другом. Соотношение, при котором определяется данная связь, называют уравнением состояния данного тела. В самом простом случае равновесное состояние тела определяется значением следующих параметров: давления p , объема V и температуры (масса тела или системы, как правило, известна).
Что такое идеальный газ
Уравнение состояния так называемого идеального газа является простым, но достаточно информативным.
Идеальный газ – это газ, в котором пренебрегают взаимодействием молекул между собой.
Идеальными считают разреженные газы. Особенно близки к идеальным газы гелий и водород. Идеальный газ – это упрощенная математическая модель реального газа: молекулы движутся хаотически, а соударения между молекулами и удары молекул о стенки сосуда упругие, не приводящие к потерям энергии в системе. Подобная упрощенная модель весьма удобна, поскольку не требует учета силы взаимодействия между молекулами газа. Множество реальных газов не отличаются в своем поведении от идеального газа в условиях, когда суммарный объем молекул пренебрежимо мал в сравнении с объемом сосуда (то есть при атмосферном давлении и комнатной температуре). Это дает возможность применять уравнение состояния идеального газа для сложных расчетов.
Уравнение состояния идеального газа запишем несколько раз ( 2 ) , ( 3 ) , ( 5 ) :
p V = m μ R T = ν R T ( 2 ) .
Уравнение ( 2 ) – уравнение Менделеева-Клапейрона, где m – это масса газа, μ – это молярная масса газа, R = 8 , 31 Д ж м о л ь · К – это универсальная газовая постоянная, ν – это число молей вещества.
где N – это количество молекул газа в массе m , k = 1 , 38 · 10 — 23 Д ж К , постоянная Больцмана, определяющая «долю» газовой постоянной, которая приходится на 1 молекулу и
N A = 6 , 02 · 10 23 м о л ь — 1 – это постоянная Авогадро.
Если поделить в ( 4 ) обе части на V , то получаем следующий вид записи уравнения состояния идеального газа:
где n = N V – это количество частиц в единице объема или же концентрация частиц.
Что такое реальный газ
Рассмотрим теперь более сложные системы: неидеальные газы и жидкости.
Реальный газ – это газ, между молекулами которого наблюдаются заметные силы взаимодействия.
Необходимо учитывать, что в неидеальных, плотных газах взаимодействие молекул высоко. Известно, что взаимодействие молекул очень сильно усложняет физическую картину, потому точную формулу уравнения состояния неидеального газа не получается записать в простом виде. В данном случае прибегают к приближенным формулам, найденным полу-эмпирическим путем. Самая удачная формула – это уравнение Ван-деp-Ваальса.
Взаимодействие молекул обладает сложным характером. На достаточно больших расстояниях между молекулами действуют силы притяжения. С уменьшением расстояния силы притяжения вначале растут, однако потом уменьшаются и преобразуются в силы отталкивания. Притяжение и отталкивание молекул будем рассматривать и учитывать отдельно. Уравнение Ван-дер-Ваальса, которое описывает состояние одного моля реального газа, имеет вид:
p + a V μ 2 V μ — b = R T ( 6 ) ,
где a V μ 2 – это внутреннее давление, обусловленное силами притяжения между молекулами, b – это поправка на собственный объем молекул, учитывающая действие сил отталкивания между молекулами, при этом:
b = N A 2 3 πd 3 ( 7 ) ,
где d – это диаметр молекулы. Значение a рассчитывается по формуле:
a = — 2 πN A 2 ∫ d ∞ W p ( r ) r 2 dr ( 8 ) ,
где W p ( r ) – это потенциальная энергия притяжения 2 -х молекул.
При увеличении объема значение поправок в уравнении ( 6 ) становится менее существенным. И в пределе уравнение ( 6 ) превращается в уравнение ( 2 ) . Это согласовано с тем фактом, что с уменьшением плотности реальные газы по своим характеристикам приближаются к идеальным.
Положительным в уравнении Ван-деp-Ваальса является тот факт, что данное равенство при очень больших плотностях приблизительно описывает также и свойства жидкости, в частности, плохую ее сжимаемость. Потому существует основание предполагать, что уравнение Ван-деp-Ваальса позволяет отразить и переход от жидкости к газу (либо от газа к жидкости).
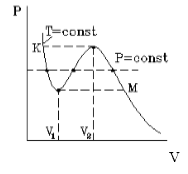
На рисунке 1 представлена изотерма Ван-дер-Ваальса для некоторого постоянного значения температуры T , которая построена из соответствующего уравнения.
В месте “извилины” (участок КМ) изотерма 3 раза пересекает изобару. На участке
V 1 , V 2 давление увеличивается с ростом объема.
Подобная зависимость невозможна. Это означает, что в этой области с веществом происходит что-то необыкновенное. Что именно, не видно в уравнении Ван-деp-Ваальса. Обратимся к опыту. В месте “извилины” на изотерме в состоянии равновесия вещество расслаивается на 2 фазы: жидкую и газообразную. Обе фазы существуют одновременно и находятся в фазовом равновесии. В таком состоянии происходит испарение жидкости и конденсация газа. Процессы протекают с такой интенсивностью, что полностью компенсируют друг друга: объем жидкости и газа со временем не изменяется.
Газ, который находится в фазовом равновесии со своей жидкостью, называется насыщенным паром. Если фазовое равновесие отсутствует, отсутствует также компенсация испарения и конденсации, тогда газ называется ненасыщенным паром.
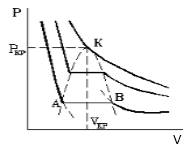
Что происходит с изотермой в области двухфазного состояния вещества (то есть в месте «извилины» изотермы Ван-деp-Ваальса)? Эксперимент показывает, что в этом месте при изменении объема давление остается неизменным. График изотермы идет параллельно оси V (рисунок 2 ).
С увеличением температуры участок двухфазных состояний на изотермах уменьшается до тех пор, пока не превращается в точку (рисунок 2 ). Это особая точка К , в которой исчезает разница между жидкостью и паром. Ее называют критической точкой.
Параметры, которые соответствуют критическому состоянию, являются критическими (критическая температура, критическое давление, критическая плотность вещества).
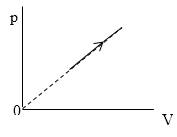
Необходимо найти величину n . В процессе, представленном на рисунке 3 , давление p
Из графика, приведенного на рисунке 3 , запишем уравнение процесса в параметрах p ( V ) :
С учетом уравнения Менделеева-Клайперона:
V вместо объема, получаем:
Моль кислорода охлаждают до — 100 ° C . Необходимо определить давление, которое оказывает газ на стенки сосуда, если занимаемый газом объем V = 0 , 1 л . Необходимо также сравнить p с давлением идеального газа p i d , если бы кислород вел себя как идеальный газ. Величина постоянных Ван-дер-Ваальса a и b , для кислорода a = 0 , 1358 П а · м 6 / м о л ь 2 , b = 3 , 167 · 10 — 5 м 3 / м о л ь .
Из уравнения Ван-Дер-Ваальса имеем:
p = R T V μ — b — a V μ 2
Переведем температуру в систему измерения: T = t + 273 , По условию T = 173 K , V = 0 , 1 л = 10 — 4 м 3 .
Произведем расчет: p = 8 , 31 · 173 ( 10 — 3 , 2 ) · 10 — 5 — 0 , 1358 ( 10 — 4 ) 2 = 75 , 61 · 10 5 ( П а ) .
Для идеального газа:
Рассчитаем: p i d = 1 · 8 , 31 · 173 10 — 4 = 143 · 10 5 ( П а ) .
Параметры состояния в термодинамике и первый закон термодинамики (стр. 1 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 |
Параметры состояния в термодинамике
и первый закон термодинамики.
1. Определение понятий.
1.1. Расчеты и их точность.
1.1.1. Физическая величина – категория мышления, характеризуется отвлеченным числом и наименованием. Отвлеченное число определяет количество, наименование – качество. И эти два понятия (количество и качество) для физической величины нераздельны.
Чтобы какая-то величина, характеристика стала физической, необходимо и достаточно, чтобы существовал способ ее измерения (сравнения с эталоном) или метод ее расчета.
Наименование физической величины еще называют размерностью. У физических величин 20С, 2 км, 2 рубля – количество одинаково, а качество, физический смысл этого количества совсем разный.
1.1.2. Операции над физическими величинами.
Математики совершенно не задумываются о смысле, о качестве величин, над которыми они совершают свои действия, процедуры. Физик же должен быть предельно осторожен. Действительно, что такое 23км? Это 8 чего? Каково качество, наименование у числа 8? Наконец, 23км = 23000м справедливо ли? Для математика – нет, а для физика? Далее, 2м +20С = 4 чего?
Эти простые примеры показывают, что целый ряд операций над физическими величинами недопустимы в силу неопределенности наименования (качества), размерности результата.
Разрешается проводить операцию алгебраического сложения только для одноименных (одинаковой размерности) слагаемых. В частности, все члены любого уравнения должны иметь одну и туже размерность.
Разрешается возводить в степень, умножать и делить физические величины разного наименования. При этом эти операции совершаются и над отвлеченным числом (как делают математики), и над наименованием. Например, 60С : 2м/сек = 3 0С*сек*м-1.
Следствие. Размерность любых физических величин всегда представляет собой произведение степеней размерностей основных величин в данной системе размерностей. В системе СИ, а только в ней по закону РФ мы и должны работать, основными величинами являются: м (метр), кг (килограмм массы), с (секунда), К (градус Кельвина), а (ампер), св (свеча).
1.1.3. Точность расчетов.
Расчетная формула для определения какой-то физической величины представляет собой последовательность математических операций над исходными физическими величинами: сделай сначала это, потом то и …. т. д.
Точность результата расчета измеряется погрешностью, абсолютной и относительной.
Абсолютной погрешностью определения (т. е. расчета или измерения в опыте) величины Х называется
ΔХ = |Храсч — Хист|,
где величина Храсч – расчетное (измеренное) значение физической величины, Хист – истинное, как правило, не известное.
Относительной погрешностью δХ называется отношение
Из этих определений следует, что и абсолютная и относительная погрешность определения Храсч не зависит от порядка самой величины.
Культура грамотного расчета любой физической величины основана на следующей простой истине: погрешность результата расчета по любой расчетной формуле не меньше погрешности исходных величин в формуле. Иными словами, расчет по любой формуле не может увеличить точность результата по сравнению с точностью исходных данных. Если в составе исходных величин для расчета находятся величины разной погрешности (точности), то погрешность результата не лучше максимальной погрешности величин в исходных данных.
На практике стараются использовать такие исходные данные, относительная погрешность которых одинакова, и тогда относительная погрешность результата расчета по какой-то формуле не меньше погрешности исходных величин.
В химической технологии стараются вести все расчеты с точностью 2% – 3% (относительная ошибка). И тогда, можно легко показать, в результате расчета следует указывать (записывать) число с тремя значащими цифрами, независимо от порядка величины. Например, 2,84; 0,0284 = 2,84 * 10-2; 28400 = 2,84 * 104 – и это все величины, имеющие одинаковую относительную погрешность (2% — 3%), причем цифра 2 – точная, цифра 8 – тоже точная, а цифра 4 определена не точно: там может быть любая цифра от 1 до 9. Следовательно, при использовании калькулятора при проведении расчетов не следует в результат списывать цифры из всех разрядов калькулятора, разумно сразу сначала округлять справа налево вплоть до третьей цифры слева. Например, калькулятор высветил результат 2,843687 * 10-2, записывать результат следует в виде 2,84 * 10-2, или следует записывать в виде 5,64 * 107.
1.2. Основные термодинамические понятия.
1.2.1. Термодинамическая система и внешняя среда.
Пусть рассматривается некоторая совокупность объектов (материальных тел). Заключим их в некоторую абстрактную (виртуальную) воображаемую или материальную границу (оболочку). И все, что находится внутри этой границы, назовем термодинамической системой. Выбор центрального для термодинамических расчетов объекта определяет сам исследователь, и он же решает, что собой представляет внешняя (окружающая) среда, с которой это центральное тело взаимодействует.
В технической термодинамике объектом исследования является рабочее тело (газ, жидкость или твердое) как единая макросистема какого-то вещества или смеси веществ. Взаимодействие термодинамической системы (рабочего тела) с внешней средой, по предположению, осуществляется только на границе. «Взаимодействие – вот главное, когда мы рассматриваем природу в целом» отметил философ и естествоиспытатель Ф. Энгельс.
1.2.2. Взаимодействием термодинамической системы с внешней средой называется акт энергообмена. Есть энергообмен в какой-то форме – значит есть взаимодействие. Иначе, взаимодействия нет. «Добродетельным можно быть самим по себе, а для порока нужны двое» отметил тот же Ф. Энгельс. В частности, если рабочее тело заключено в объем с неподвижными прочными стенками, то внешняя среда не может деформировать (сжимать или расширять) рабочее тело. Тогда в термодинамике говорят, что термодинамическая система деформационно изолирована от внешней среды. Если на границе термодинамической системы расположить толстый слой теплоизоляции, то система не может обмениваться теплотой с внешним миром. (Зимой люди одевают шубы и теплые пальто.) Тогда говорят, что рабочее тело теплоизолировано, а все процессы в нем называют адиабатическими. Аналогично, можно говорить о химическом взаимодействии (физхимия), о электрическом, магнитном, о соответствующей изоляции от внешней среды.
2. Параметры состояния в термодинамике.
2.1. Термин «параметр» — греч. Parametron – отмеривающий. Параметр состояния – физическая величина, т. е. количественная и качественная характеристика свойств или поведения термодинамической макросистемы (рабочего тела). На рассвете развития и становления термодинамики параметры состояния системы избирались на основе прямых измерений в опытах. В современной термодинамике параметры состояния обязательно соотносят с каким-то видом (родом) взаимодействия системы с внешней средой.
Человеческий опыт позволяет различать множество взаимодействий по их роду (типу, виду): деформационное изменение рабочего тела по геометрии объема, поверхности или длины рабочего тела, термическое (нагрев или охлаждение), химическое (молекулы в исходной смеси веществ химически взаимодействуют с образованием молекул новых веществ), электрическое (перемещение зарядов под действием внешнего электрического поля), магнитное (диполи, микро магниты, домены рабочего тела занимают новое положение в пространстве под действием внешнего магнитного поля).
Техническая термодинамика, будучи частью термодинамики вообще, занимается только деформационным и термическим взаимодействиями, происходящими с телами в целом в их массе и объеме (макросистемы).
2.2. Классификация и систематизация термодинамических параметров состояния.
В любой реальной системе при ее взаимодействии с внешней средой потенциалом называется такой параметр, разность значений которого в системе и внешней среде является первопричиной взаимодействия.
Иными словами, разность потенциалов – необходимое условие взаимодействия (и любого рода энергообмена или массообмена).
Необходимым условием деформации (изменения геометрии и формы рабочего тела) является разность давлений р внутри и вне системы, других причин для деформации объема просто нет. В гидравлике (текучие рабочие тела) эта же разность давлений является причиной движения жидких сред.
Необходимым условием термического взаимодействия системы с внешней средой является разность температур Т внутри и вне системы
Вообще, разность значений внешнего Ре и внутреннего Р потенциала можно назвать «движущей силой».
Итак, — р (минус) – потенциал деформационного взаимодействия. Причина появления минуса рассматривается далее.
Т – потенциал термического взаимодействия.
По определению, давлением р называется отношение силы воздействия к площади поверхности действия силы:
р = f / s, [f] = н (ньютон), [s] = м2. [p] = н/м2. [T] = К (Кельвин). (1.1)
2.2.2. Координата состояния.
Координатой состояния называется такой параметр состояния, который обязательно изменяется при данном роде взаимодействия.
Иными словами, изменение координаты состояния является достаточным условием взаимодействия (т. е. энергообмена или массообмена) системы с внешней средой.
Поиском конкретного вида таких параметров – координат занимается экспериментальная и теоретическая физика в ее различных разделах. Для механического деформационного взаимодействия координатой являются: длина – при линейном воздействии (растягивание пружины, например), площадь – при поверхностном воздействии (выдувании пузырей, например), объем – при воздействии на трехмерное тело, масса – при химическом взаимодействии двух или более веществ (убывание исходных веществ и увеличение количества продуктов реакции).
Для деформационного взаимодействия координатой состояния является геометрический объем V м3, поверхность S м2 или протяженность l м конкретного тела (вещества). Однако геометрические характеристики объема м3, поверхности м2 или длины м ничего кроме абсолютного значения (количества) не дают. Подобные количественные характеристики не могут относиться к параметрам состояния системы (поэтому называются экстенсивными величинами). Для рабочего тела в обобщенном виде параметром состояния, т. е. характеристикой последнего, служит удельное значение геометрической характеристики: удельного объема, т. е. геометрического объема, отнесенного к массе m кг рабочего тела, помещенного в объем V:
v = V / m, м3 / кг (1.2)
Заметим здесь же, что удельный объем вещества в термодинамической системе очень просто связан с плотностью ρ среды, которая почему-то более привычна студентам:
v ≡ 1 / ρ; ρ ≡ 1/ v кг/м3 (1.3)
Плотность вещества и его удельный объем просто обратно пропорциональны, т. е. vρ = 1.
Термическая координата состояния и ее экстенсивная величина носит название энтропия, обозначается буквой S, имеет размерность дж/К, а параметром состояния рассматривается удельное значение энтропии, относящееся к интенсивным величинам (характеристикам), оно обозначается буквой s:
s = S / m, дж / кг К (1.4)
Энтропия рабочего тела – такая же физическая величина, как хорошо знакомые давление, объем, температура. Энтропию также можно измерять в специальном эксперименте или рассчитывать по некоторой методике. Исторически энтропия была введена немецким термодинамиком Клаузиусом аналитическим анализом термодинамических взаимодействий.
Еще и еще раз подчеркнем: координата состояния данного рода взаимодействия никогда не изменяется, если отсутствует этот род взаимодействия.
3. Первый закон термодинамики – взаимные энергопревращения в термодинамических системах.
3.1. Количество воздействия.
Воздействием внешней среды на термодинамическую систему мы назвали акт обмена энергией между двумя объектами. Поэтому естественной мерой воздействия является количество энергии, которой обменивается система с внешней средой. Формальную запись количества воздействия термодинамика позаимствовала у теоретической механики. В аппарате последней, как и в теории поля, термин потенциал относится к энергии рабочего тела, а не к его параметру.
Элементарным количеством воздействия данного рода называется произведение потенциала на приращение сопряженной координаты.
│dKd│ = pdv, дж/кг, │dKT│ = Tds, дж/кг, (1.7)
где К – количество воздействия, индексы «d» и «Т» — соответственно деформационное и термическое воздействие, │ │- символика абсолютного значения величины.
Здесь уместно отметить об отличии направления действия сил и потенциалов. В теоретической механике, которая возникла исторически ранее термодинамики, знак «+» был принят для работы расширения системы (dv > 0). В термодинамике для потока теплоты q от системы во внешнюю среду принимается знак «-« (ds 0.
Это же правило устанавливается строго термодинамически. Для записи в одном уравнении количеств воздействия Кd и КТ обмена системы с окружающей средой следует лишь вспомнить качественную связь между направлением действия движущей силы и изменением координаты. Действительно, при силовых взаимодействиях Xe > X (dX > 0) координата убывает (dx Р (dP > 0) координата возрастает и количество внешнего воздействия должно входить в уравнение со знаком «+». Иными словами, формально потенциал это минус сила.
3.2. Внутренняя энергия.
Внутренней энергией термодинамической системы называется сумма всех видов энергии в системе.
В школьном курсе физики различают два вида энергии: кинетическая и потенциальная. Под кинетической энергией понимают энергию движения конечного количества массы макротела в геометрическом пространстве. При этом различают движение поступательное, как движение центра масс, движение вращательное вокруг какой-то оси и движение колебательное, как перемещение частей массы относительно друг друга.
Разумеется, внутренняя энергия возрастает или убывает за счет потоков через границу рабочего тела (за счет количеств внешних воздействий между системой и внешней средой). Именно подобные энергетические преобразования по существу между каким-то внешним телом и рабочим телом увеличивают или уменьшают внутреннюю энергию. В самом веществе рабочего тела происходят структурно-энергетические преобразования. Последние адекватны роду (виду) взаимодействия. Если это электрические импульсы (за счет разности электрических потенциалов ΔV), то в системе происходит движение зарядов. Если воздействие на рабочее тело тепловое, то интенсифицируется движение молекул (растет их кинетическая энергия) и т. д.
Однако, термодинамика не занимается таким детальным рассмотрением роли и влияния на вещество видов энергии – это задача физики и физической химии.
Обозначение внутренней энергии в термодинамике – U дж или u = U/m дж/кг.
3.3. Первый закон термодинамики.
На специфическом языке термодинамики это просто закон сохранения энергии в замкнутой системе: изменение внутренней энергии термодинамической системы равно сумме количеств внешних воздействий.
Аналитическая запись закона (основное уравнение термодинамики:
dU = ∑ δKi или dU = δQ – δW = T dS – p dV. (1.8)
для термодеформационной системы. В (1.8) приращение внутренней энергии dU записано через параметры состояния р, V,Т, S, т. е. через потенциалы и координаты двух видов взаимодействия. В интенсивной форме запись первого закона термодинамики имеет вид:
dq ≡ T ds, dw ≡ p dv и тогда du = dq – dw = Tds — pdv. (1.9)
Здесь dq = Tds – элементарное количество теплоты, подведенное (отведенное) к системе, т. е. это элементарное количество термического воздействия, dw = pdv – элементарное количество работы деформации (механической работы), т. е. элементарное количество деформационного воздействия.
Замечание. В уравнении первого закона (основного закона термодинамики) в правой части входят внешние воздействия, т. е. при потенциальных воздействиях Pedxe и силовых –Xedxe, т. е.
dU = ∑Pedxe — ∑Xedxe (1.9.1)
Если изучаются равновесные (квазистационарные) процессы, в которых нет отличия по величине сил (Х) и потенциалов в системе (Р) и окружающей среде (Ре), т. е. между ними бесконечно малая разница по величине, то все переменные основного уравнения термодинамики – функция U и аргументы P, X,x относятся к исследуемому рабочему телу. Действительно, из (1.9.1) при Pe – P = ΔP и Xe – X = ΔX получим
dU = ∑(P +ΔP)dx — ∑(X + ΔX)dx,
и при ΔР → о(ΔР) и ΔХ → о(ΔХ) окончательно с учетом равенства │dxe│ = │dx│получаем (1.8) и (1.9).
Окончательно, основное уравнение технической термодинамики, изучающей квазистатические (равновесные) процессы имеет вид:
du = Tds – pdv. (1.9.2.)
Подведем предварительные итоги. Выше представлены основные определения понятий термодинамики, их необходимо запомнить, чтобы говорить на языке термодинамики. Взаимосвязь понятий иллюстрирует схема на рис 1.
Схема последовательности ввода и взаимосвязей
понятий в термодинамике.
4. Уравнения состояния.
Уравнением состояния рабочего тела называется функциональная зависимость потенциала от всех координат состояния.
Следовательно, сколько родов взаимодействия термодинамической системы с внешней средой, столько потенциалов, столько координат состояния и столько уравнений состояния.
Для термодеформационной системы (т. е. для двух родов взаимодействия: термического и деформационного) уравнений состояния два, т. к. два потенциала в соответствии с (1.9.2):
p = f(s, v), T = φ(s, v). (1.10)
Конкретный вид функций f(s, v) и φ(s, v) предоставляют для термодинамики физики, которые для этого проводят специальные теоретические и экспериментальные исследования. Полученные соотношения параметров состояния системы четко отражают физические связи внутри рабочего тела (системы) – первичными сигналами изменения состояния являются координаты. Сами соотношения относятся к уравнениям состояния – это общий вид такого уравнения в термодинамике.
В силу исторических обстоятельств развития физики и термодинамики уравнение состояния идеального газа не содержит энтропию:
pv = RT (уравнение Клайперона – Менделеева), (1.11)
где R = 8314/μ. Здесь 8314 дж/кмольК – универсальная газовая постоянная, μ – молекулярный вес вещества рабочего тела, кг/кмоль. Это уравнение было получено из опытов с газами при невысоких давлениях и температурах. Разумеется, из (1.10) обе аналитические связи можно свести к одной F(p, v,T) = 0, которая не противоречит экспериментальному (1.11). Этим не исчерпывается роль термодинамики в решении проблемы уравнений состояния. Она накладывает существенные ограничения на функциональный вид этих функций. Эти функции могут быть не любыми, а обязательно удовлетворять условиям:
(∂f/∂v)s ≡ (∂(-p)/∂v)s ≥ 0 и (∂φ/∂s)v ≡ (∂T/∂s)v ≥ 0 (1.12)
В этой записи, а мы будем ею широко пользоваться в дальнейшем, индекс внизу справа у скобки с частной производной означает, что соответствующий параметр состояния фиксирован.
Эти неравенства обычно называют критерием стабильности термодинамики, в химии – это формальная запись принципа ле Шателье – Брауна, хорошо знакомого студентам химико-технологического профиля образования.
Происхождение критерия стабильности термодинамики – эмпирический факт. Многочисленные наблюдения за различными термодинамическими системами показывают, что с ростом координаты состояния какого-то рода взаимодействия (и отсутствия других видов) соответствующий потенциал самопроизвольно не убывает (т. е. растет или неизменен). Обратно, с увеличением потенциала сопряженная координата состояния самопроизвольно также не убывает (т. е. растет или неизменна)
Для теплоизолированной системы (s = const) c увеличением удельного объема, согласно критерию стабильности, давление в системе только уменьшается, но это и очевидно. Для деформационно изолированной системы (v = const) с увеличением энтропии температура газа обязательно увеличится, и обратно, с увеличением температуры энтропия только увеличится. Действительно, если закрытый газовый баллон с каким-то газом положить в костер, то температура газа обязательно увеличится в согласии с критерием стабильности. Вот такие и многие другие экспериментальные факты термодинамика «присвоила» себе.
4. Размерности, измерение и расчет параметров состояния.
Измерение или расчет каких-либо характеристик рабочего тела относятся к количественной оценке величины этих характеристик по сравнению с эталоном самой величины. Подобные эталоны приняты в международной практике при введении стандартов на сами характеристики и их эталоны. В настоящее время действует, как обязательный, международный стандарт (SI) или Российский (СИ), утвержденный в 1980 году как обязательный для всех отраслей науки и техники. Основных единиц в этом стандарте – 6 и это: длина – метр, масса – килограмм, термодинамическая температура – градус Кельвина, сила тока – ампер, сила света – свеча, время – секунда. Все они используются в различных разделах термодинамики. В производные единицы включены термодинамические величины: сила – ньютон (Н), давление – (Н/м2), работа и количество теплоты – джоуль (дж).
Из курса физики известно, что производные величины представляют результат взаимодействия двух или более физических объектов в пространстве или во времени. Характеристика и размерность производных величин отличаются от таких же для исходных взаимодействующих объектов, а размерность первых определяется по уравнениям законов связи вторых. Так работа – это произведение действующей силы на путь, т. е. производная величина определяется по уравнению W = X*x, в котором сила Х выражается в избранной системе единиц. Но вне зависимости от системы единиц понятие силы едино согласно второму закону Ньютона – это произведение массы тела на ускорение его Х = mа. Тогда для обязательной в употреблении системе СИ получим [X] = 1 кг*1 м/с2 = 1кг м/с2 и эта сила называется Ньютон, т. е. 1 Н = кг м/с2.
В технической системе единиц, встречающейся в учебниках и старых проектах производств, принята иная единица силы – кГ – килограмм силы, полученная из того же уравнения второго закона Ньютона для массы 1 кг и ускорения силы тяжести g = 9,81 м/с2 (точнее 9,80665). Очевидна связь между этими двумя единицами силы: 1 кГ = 9,81 Н. Соответственно работа в технической системе единиц вычисляется по величине (количеству) в кГм, а в системе СИ в Нм, названной джоулем (дж). Размерность последней величины кгм2с-2 и она же используется для расчетов количества теплоты Q, которая в технической системе единиц имеет единицу – Ккал или кал. Согласно закону эквивалентности 427 кГм работы эквивалентны 1 Ккал, т. е. 1 ккал = 4,19 кдж.
Размерность давления по определению – сила, отнесенная к единице поверхности действия силы: н/м2 = кг/мс2. Единица давления н/м2 = П названа паскаль. Но, оказалось, в технике используются много большие давления, чем паскали. Поэтому введена величина 1 бар = 105 П, которая удобно соответствует технической единице – одной технической атмосфере, равной 104 кГ/м2 или 0,981*105 П.
Прямые измерения абсолютного давления, как параметра состояния рабочего тела, невозможны чисто технически. Косвенные измерения всегда связаны с применением приборов, замеряющих разность давлений, – манометров. В производственных условиях применяются механические или тензометрические манометры, а при давлениях в аппаратах ниже атмосферного или немного выше его используются жидкостные манометры, чаще всего так называемые U-образные дифманометры. Они представляют собой две вертикальные параллельные стеклянные трубки, соединенные внизу перемычкой, коленом из самой трубки. В таком приборе вес столба жидкости h выравнивается разностью давлений Δр внутри аппарата и в атмосфере (рис.2). В аналитической форме:
где ρ – плотность жидкости, залитой в U-образный манометр, кг/м3, g = 9,81 м/с2 – ускорение свободного падения, h – разность столбов жидкости в коленах U-образного манометра. Легко видеть, что
где В – барометрическое давление. В этом уравнении все величины, естественно, приведены к одной размерности. Заметим, что величина В – давление в атмосфере по отношению к глубокому (космическому) вакууму.
При наличии в аппарате среды под разряжением (под вакуумом) столб жидкости в U-образном манометре вместе с остаточным давлением газа в аппарате будут уравновешены атмосферным давлением:
т. е. само абсолютное давление будет рассчитываться по прежним переменным
Рис. 2. Иллюстрация к измерению давления.
Здесь р – давление в сосуде, h — разность столбов жидкости
в U-образном манометре.
В сечении а – а давления в трубках справа и слева уравновешены.
Подчеркнем еще раз – параметром состояния является лишь абсолютное давление, которое отсчитывается от безуслов0ного нуля, т. е. природного абсолютного начала отсчета (космосе). В земных (технических) условиях договорились об абсолютной шкале давлений согласно закону Шарля:
р = р0(1 + βТ) или Δр/р0 = βТ.
Здесь из опытов получено для идеальных газов β = 1/273.
Температурная шкала создается следующим образом. Для любого идеального газа выполняется уравнение состояния в виде:
где F(..) – универсальная функция температуры. Опыт показывает, что эта функция линейно растет с ростом температуры:
где α и β – константы. Тогда для температуры плавления льда и температуры кипения воды (при давлении 105 Па) в градусах Цельсия запишем:
0 = α(pV)0 + β, 100 = α(pV)100 + β. (4.2)
Система уравнений (4.2) относительно α и β легко решается, и это решение подставим в (4.1). Получим:
θ = 1000C * (pV –(pV)0)/((pV)100 – (pV
Из опыта известно, что для идеального газа
(pV)100 / (pV)0 = 1,366.
Подставляя это соотношение в (4.3), получаем
pV = (pV)0 (1 + 0,00366θ).
Здесь величина θ есть «идеально-газовая температура». Величина pV, равная универсальной функции температуры, станет равной 0, если θ = θ0 = -1/0,00366 = -273,150С. Если перенести начало отсчета температуры θ из 00С в точку θ0, то получим
Т(К) = θ – θ0 = (θ + 273,15) К.
Так получается шкала термодинамической (абсолютной) температуры Т в кельвинах, зная эмпирическую шкалу температуры Цельсия. Часто вместо θ используют обозначение t, одновременно для практических расчетов пренебрегают величиной 0,15 на фоне 273. Таким образом
Где температура Т в кельвинах, а температура t в Цельсиях.
В англо-язычной научно-технической литературе часто встречается понятие температуры по шкале Фаренгейта. Связь этой шкалы со шкалой Цельсия следующая:
t0F = 9/5 (t0C + 32) или t0C = 5/9 (t0F – 32).
5. Статистическая физика и параметры состояния в термодинамике.
Параметры состояния в термодинамике являются макрохарактеристиками системы, т. е. они определяют свойства и поведение системы в целом, а не свойства и поведение ее частей, не внутренних составляющих системы. Термодинамика занимается только макросистемами.
В предыдущей главе по существу изложена аксиоматика термодинамики, ее базис, фундамент. Так, собственно, поступали Евклид, Лобачевский, Риман, создавая свои «математики». Однако, для свободного и глубокого владения методом термодинамического анализа необходим широкий спектр физических представлений, образов, ассоциаций, связанных с основными понятиями термодинамики.
Как же представляет себе статистическая физика параметры состояния в термодинамике? По существу сказать: «Параметры состояния – это макрохарактеристика объекта», сказать: «Термодинамика занимается макросистемами» — означает, на языке теории вероятностей и статистики, что параметры состояния в термодинамике являются просто средними величинами, математическим ожиданием некоторых случайных величин.
Удельный объем v м3/кг.
Рассмотрим некоторый фиксированный геометрический объем V, м3 какого-то газа с границей Г. Пусть этот объем находится в том же газе, а стенки границы Г абсолютно проницаемы для молекул газа (см. рис. 3).
Рис. 3. Иллюстрация к понятию удельного объема.
Молекулы совершают случайное, хаотическое блуждание, какие-то из них войдут в объем V через границу Г, а какие-то выйдут из объема. Следовательно, число молекул в объеме V является случайной величиной с каким-то математическим ожиданием, т. е. средним значением. Если это среднее значение умножить на массу молекулы и произведение разделить на V, то и получим, по определению, величину плотности ρ. И в соответствии с (1.3) далее получаем величину удельного объема v. Отметим важное обстоятельство: чем больше число молекул газа в V, тем точнее находится оценка среднего значения числа молекул в V. Именно в этом смысл макрорассмотрения: число молекул газа должно быть очень большим. Что такое v или ρ, если в объеме V «бегает» одна – две молекулы – не знает никто.
Рассмотрим газ и непроницаемую стенку (рис. 4).
Рис. 4. Иллюстрация к понятию давления р.
Молекулы газа беспорядочно движутся в объеме около стенки. Скорость их движения случайна и по величине и по направлению. При подходе молекулы к стенке происходит удар: молекула деформирует стенку (сминает), далее стенка упруго локально отталкивает молекулу обратно, и весь этот процесс происходит за какое-то время Δτ секунд. Если до удара нормальную к стенке компоненту вектора скорости поступательного движения молекулы обозначить как W, то после удара ее скорость станет равной –W (минус). Это означает, что количество движения молекулы изменилось на величину -2 μW. (μ – масса молекулы). Но согласно второму закону Ньютона это означает, что на молекулу действовала сила F в течение времени Δτ:
Следовательно, каждая молекула, ударившись о стенку, оказывает на нее силовое воздействие F. И это воздействие случайно. Найдем среднее значение силы ударов молекул по стенке, усредняя по множеству этих молекул за время много большее Δτ, разделим на величину площади поверхности стенки и получим величину давления р.
Опять обращаем внимание, что чем больше будет ударов молекул р стенку, тем точнее, ближе к истине величина р. Что такое давление, если у стенки «бегает» одна молекула, не знает никто.
Забегая вперед, заметим, что, чем больше молекул находится у стенки (чем больше плотность газа ρ), тем естественно больше давление р. Одновременно, чем больше скорость W молекул (т. е. чем больше температура газа), тем тоже больше давление р. А от этих рассуждений уже и не далеко до вывода уравнения состояния идеального газа.
Температура Т, К.
Рассмотрим поступательное движение молекул вещества, их колебательное и вращательное движения. Каждому из них можно сопоставить количество кинетической энергии. Так как поведение молекул реального газа стохастично, случайно, то и количество кинетической энергии молекул вещества тоже случайно. Можно найти среднее значение этих энергий по множеству всех молекул и сопоставить это среднее значение с температурой. В частности, в статистической физике показывается, что при рассмотрении простейшего газа, молекулы которого представимы в виде материальных точек (нет вращения и колебаний) получается следующее. Оказывается, что среднее значение (математическое ожидание) кинетической энергии поступательного движения молекулы равно 3/2 kT, где k – константа Больцмана. Следовательно, термический потенциал в термодинамике Т можно понимать именно как среднюю кинетическую энергию поступательного движения молекул вещества.
И опять-таки никто не знает, что такое температура одной, двух молекул. Оценка среднего значения по одной двум молекулам такая «плохая», что ее нельзя считать физической величиной.
В теории плазмы физики вынуждены вводить в рассмотрение аж две температуры. Одна – для атомов без электронов, другая – для электронов: уж очень большая разница в скоростях и массах.
Если вещество находится в газовой фазе, то температура характеризует преимущественно кинетическую энергию поступательного движения молекул. Для жидкой и твердой фазы поступательное движение сильно затруднено из-за большой плотности. Для твердой фазы характерно колебательное движение атомов и молекул, для жидкой еще и вращение.
Рассматривая интерпретацию термодинамических параметров состояния с точки зрения статистической физики, можно увидеть, что эти параметры являются математическими ожиданиями некоторых случайных величин:
где Мх – среднее значение случайной величины х, f(x) – плотность распределения вероятностей этой случайной величины. В теории вероятностей все просто: f(x) — известна, значит надо взять интеграл и получить величину математического ожидания. Больцман поставил вопрос совсем иначе: сколько существует распределений молекул (т. е. функций f(…)) в пространстве координат и скоростей, чтобы получить одну и туже величину средних величин? Математик, не задумываясь, ответит – бесконечно много. Физик с ним согласится, что действительно много. Чтобы не работать с огромными числами, Больцман предложил работать с их логарифмами. Если общее число вариантов распределений молекул в пространстве координат и скоростей обозначить как W, то по Больцману
где k — константа Больцмана, s — энтропия.
Иллюстрацией может служить толпа людей, митингующих на площади, затем те же люди, идущие на демонстрации, наконец, те же люди как в армии построенные в колонну и марширующие по той же площади. Здесь видно, что хаоса, беспорядка все меньше и меньше, поэтому и энтропия все меньше. Зато средние значения каких-то случайных величин по множеству людей одни и те же.
Подведем итоги: статистическая физика рассматривает термодинамические параметры состояния как средние значения некоторых случайных величин, усредненных по огромному множеству молекул в геометрическом и скоростном пространстве. Энтропия – мера хаоса и беспорядка, мера числа разных распределений вероятностей, дающих одни и те же средние значения некоторых случайных величин.
http://zaochnik.com/spravochnik/fizika/molekuljarno-kineticheskaja-teorija/uravnenie-sostojanija-veschestva/
http://pandia.ru/text/77/363/84998.php