Напишите в молекулярной и ионной формах уравнения реакций для следующих превращений: 105. Pb(NO3)2 Pb(OH)NO3 Pb(OH)2 K2PbO2






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Напишите в молекулярной и ионной формах уравнения реакций для следующих превращений:
105. Pb(NO3)2 ® Pb(OH)NO3 ® Pb(OH)2 ® K2PbO2
Решение :
Pb 2+ + 2NO3 — + Na + + OH — ® Pb(OH) + + NO3 — + Na + + NO3 —
Pb 2+ + OH — ® Pb(OH) +
| Изучите химию на странице ➔ решение заданий и задач по химии. |
| Похожие готовые решения: |
- Напишите в молекулярной и ионной формах уравнения реакций для следующих превращений: 115. NiBr2 (NiOH)2SO4 Ni(OH)2 NiBr2
- Напишите в молекулярной и ионной формах уравнения реакций гидролиза солей, укажите значения рН растворов этих солей (больше или меньше семи). 121. NaNO2, Cu(NO3)2
- Напишите для предложенных соединений уравнения диссоциации, а также в молекулярной и ионной формах уравнения возможных реакций взаимодействия их H2SO4 с и NaOH. 81. HCl; Cr(OH)3
- Напишите для предложенных соединений уравнения диссоциации, а также в молекулярной и ионной формах уравнения возможных реакций взаимодействия их H2SO4 с и NaOH. 95. KOH; H2CO3
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
Частные реакции катионов второй аналитической группы
Реакции катиона свинца Pb 2+
1. Хлороводородная кислота HCl и растворимые хлориды осаждают из умеренно концентрированных растворов солей свинца (II) белый хлопьевидный осадок хлорида свинца (II), легко растворимый в горячей воде:
Pb(NO3)2 + 2HCl 
Pb 2+ + 2Cl — 
Выполнение реакции. В пробирку помещают 2 капли раствора нитрата свинца (II) Pb(NO3)2 и добавляют 2 капли хлороводородной кислоты. К раствору с осадком добавляют 0,5 мл дистиллированной воды и нагревают смесь на водяной бане. Наблюдают растворение осадка и постепенное его выпадение при охлаждении раствора.
2. Едкие щелочи из растворов солей свинца (II) осаждают гидроксид свинца (II) – осадок белого цвета:
Pb(NO3)2 + 2KOH 
Pb 2+ + 2OH — 
Гидроксид свинца (II) обладает амфотерными свойствами, поэтому он растворяется в разбавленной азотной или уксусной кислотах и в избытке щелочи:
Pb(OH)2 + 2KOH 
Выполнение реакции. К 2 каплям соли свинца (II) прибавляют сначала 1 каплю раствора щелочи, а затем ее избыток и наблюдают выпадение осадка и последующее его растворение в избытке щелочи.
3. Серная кислота H2SO4 и растворимые сульфаты выделяют из свинцовых солей труднорастворимый сульфат свинца – осадок белого цвета:
Pb(NO3)2 + H2SO4 
Pb 2+ + SO4 2- 
Осадок растворим при нагревании в растворах щелочей (10-15%):
PbSO4 + 4NaOH 
Выполнение реакции. К 2 каплям раствора соли свинца (II) прибавляют 2 капли разбавленной серной кислоты и наблюдают выпадение осадка.
4. Иодид калия KI, взаимодействуя со свинцовыми солями, дает желтый осадок иодида свинца (II):
Pb(NO3)2 + KI 
Pb 2+ + 2I — 
Реакция часто применяется для открытия ионов Pb 2+ .
Выполнение реакции. К 2 каплям раствора нитрата свинца (II) Pb(NO3)2 добавляют 2 капли раствора иодида калия. В полученный раствор с осадком добавляют 0,5 мл воды и 3-4 капли разбавленной уксусной кислоты; нагревают смесь на кипящей водяной бане в течение 2 мин, затем охлаждают содержимое пробирки под струей воды. Растворившийся при нагревании осадок иодида свинца вновь выпадает в виде красивых золотистых чешуек.
5. Хромат калия K2CrO4 или хромат натрия Na2CrO4 выделяет из раствора соли свинца желтый осадок соли свинца (II):
Pb(NO3)2 + K2CrO4 
Pb 2+ + CrO4 2- 
Осадок не растворяется в уксусной кислоте, но растворяется в азотной кислоте и щелочах. Реакция чувствительна и является характерной для ионов Pb 2+ .
Выполнение реакции. К 2 каплям раствора соли свинца (II) добавляют 2 капли раствора хромата калия и наблюдают выпадение осадка.
Реакции катиона серебра Ag +
1. Хлороводородная кислота HCl и растворимые хлориды осаждают из нейтральных и кислых растворов солей серебра в виде белого творожистого осадка хлорида серебра:
AgNO3 + HCl 
Ag + + Cl — 
Осадок легко растворяется в избытке аммиака с образованием комплексной соли:
AgCl + 2 NH3 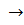
При подкислении аммиачного раствора концентрированной азотной кислотой эта соль разрушается и вновь выпадает осадок хлорида серебра:
[Ag(NH3)2]Cl + 2HNO3 
Эту реакцию обычно используют для открытия иона Ag + . Она является фармакопейной.
Выполнение реакции. В пробирку помещают 2 капли раствора нитрата серебра, добавляют к нему 2 капли разбавленной хлороводородной кислоты. К раствору с осадком добавляют 5 капель концентрированного раствора аммиака и встряхивают смесь до растворения осадка. К полученному раствору добавляют 6 капель концентрированной азотной кислоты. Наблюдают выпадение осадка.
2. Иодид калия KI образует с ионом Ag + светло-желтый осадок AgI:
AgNO3 + KI 
Ag + + l — 
Иодид серебра не растворяется в растворе аммиака в отличие от хлорида серебра.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли иодида калия и наблюдают выпадение осадка.
3. Хромат калия K2CrO4 из растворов солей серебра осаждает кирпично-красный хромат серебра:
2AgNO3 + K2CrO4 
2Ag + + CrO4 2- 
Осадок растворяется в растворе аммиака и азотной кислоте.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли раствора хромата калия и наблюдают выпадение осадка.
4. Едкие щелочи из растворов солей серебра осаждают грязно-коричневый осадок оксида серебра:
2AgNO3 + 2KOH 
2Ag + + 2OH — 
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли раствора щелочи и наблюдают выпадение осадка.
5. Тиосульфат натрия Na2S2O3 из растворов солей серебра выделяет белый осадок, который быстро желтеет, затем буреет и переходит в черный:
2AgNO3 + Na2S2O3 
Ag2 S2O3 + H2O 
Осадок Ag2 S2O3 растворяется в избытке тиосульфата с образованием комплексных солей, поэтому осадок образуется при избытке ионов серебра. Реакция является фармакопейной.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 1 каплю раствора тиосульфата натрия. Наблюдается изменение цвета осадка.
Реакции катиона ртути (I) Hg2 2+
1. Хлороводородная кислота HCl и растворимые хлориды из растворов солей ртути (I) осаждают хлорид ртути (I), или каломель, — осадок белого цвета:
Hg2(NO3)2 + HCl 
Hg2 2+ +2Cl — 
Водный раствор аммиака окрашивает осадок в черный цвет, обусловленный образованием черной мелкораздробленной ртути:
Hg2Cl2 + 2 NH3 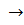
С помощью этой реакции открывают ион Hg2 2+ .
Выполнение реакции. К 2 каплям раствора нитрата ртути (I) Hg2(NO3)2 добавляют 2 капли раствора разбавленной хлороводородной кислоты. К раствору с осадком добавляют 3 капли раствора аммиака. Наблюдают почернение осадка.
2. Иодид калия KI из растворов солей ртути (I) осаждает иодид ртути (I) – осадок болотно-зеленого цвета:
Hg2(NO3)2 + 2KI 
Осадок довольно легко распадается на иодид ртути (II) и металлическую ртуть; при этом цвет осадка изменяется:
Hg2I2 
Выполнение реакции. К 2 каплям раствора нитрата ртути (I) Hg2(NO3)2 добавляют 2 капли раствора иодида калия. Наблюдают выпадение осадка и изменение его цвета при встряхивании.
3. Хромат калия K2CrO4 
Hg2(NO3)2 + K2CrO4 
2Hg + + CrO4 2- 
Осадок не растворяется в щелочах и разбавленной уксусной кислоте.
Выполнение реакции. 2 капли раствора Hg2(NO3)2 , помещенные в пробирку, нагревают на водяной бане и добавляют 2 капли хромата калия.
http://zdamsam.ru/b4833.html


