Перманганат калия и перекись водорода реакция уравнение
18.5. ОВР пероксида водорода
В молекулах пероксида водорода H2O2 атомы кислорода находятся в степени окисления –I. Это промежуточная и не самая устойчивая степень окисления атомов этого элемента, поэтому пероксид водорода проявляет и окислительные, и восстановительные свойства.
Окислительно-восстановительная активность этого вещества зависит от концентрации. В обычно используемых растворах с массовой долей 20 % пероксид водорода довольно сильный окислитель, в разбавленных растворах его окислительная активность снижается. Восстановительные свойства для пероксида водорода менее характерны, чем окислительные, и также зависят от концентрации.
Пероксид водорода – очень слабая кислота (см. приложение 13), поэтому в сильнощелочных растворах его молекулы превращаются гидропероксид-ионы.
В зависимости от реакции среды и от того, окислителем или восстановителем является пероксид водорода в данной реакции, продукты окислительно-восстановительного взаимодействия будут разными. Уравнения полуреакций для всех этих случаев приведены в таблице 1.
Уравнения окислительно-восстановительных полуреакций H2O2 в растворах
Реакция среды
H2O2 окислитель
H2O2 восстановитель
 + 2e – = 4H2O
+ 2e – = 4H2O


 + H2O + 2e – = 3OH
+ H2O + 2e – = 3OH 
 + OH
+ OH  – 2e – = O2 + H2O
– 2e – = O2 + H2OРассмотрим примеры ОВР с участием пероксида водорода.
Пример 1. Составьте уравнение реакции, протекающей при добавлении раствора йодида калия к раствору пероксида водорода, подкисленному серной кислотой.
| 1 | H2O2 + 2H3O  + 2e – = 4H2O + 2e – = 4H2O |
| 1 | 2I  – 2e – = I2 – 2e – = I2 |
H2O2 + 2H3O 

H2O2 + H2SO4 + 2KI = 2H2O + I2 
Пример 2. Составьте уравнение реакции между перманганатом калия и пероксидом водорода в водном растворе, подкисленном серной кислотой.
| 2 | MnO4  + 8H3O + 8H3O  + 5e – = Mn 2 + 5e – = Mn 2  + 12H2O + 12H2O |
| 5 | H2O2 + 2H2O – 2e – = O2 + 2H3O  |
2MnO4 


2KMnO4 + 3H2SO4 + 5H2O2 = 2MnSO4 + 8H2O + 5O2 
Пример 3. Составьте уравнение реакции пероксида водорода с йодидом натрия в растворе в присутствии гидроксида натрия.
| 3 | 6 | HO2  + H2O + 2e – = 3OH + H2O + 2e – = 3OH  |
| 1 | 2 | I  + 6OH + 6OH  – 6e – = IO3 – 6e – = IO3  + 3H2O + 3H2O |
3HO2 



3NaHO2 + NaI = 3NaOH + NaIO3
Без учета реакции нейтрализации между гидроксидом натрия и пероксидом водорода это уравнение часто записывают так:
Это же уравнение получится, если сразу (на стадии составления баланса) не принимать во внимание образование гидропероксид-ионов.
Пример 4. Составьте уравнение реакции, протекающей при добавлении диоксида свинца к раствору пероксида водорода в присутствии гидроксида калия.
Диоксид свинца PbO2 – очень сильный окислитель, особенно в кислотной среде. Восстанавливаясь в этих условиях, он образует ионы Pb 2 

| 1 | PbO2 + 2H2O + 2e – = [Pb(OH)3]  + OH + OH  |
| 1 | HO2  + OH + OH  – 2e – = O2 + H2O – 2e – = O2 + H2O |
PbO2 + H2O + HO2 

Без учета образования гидропероксид-ионов уравнение записывается так:
PbO2 + H2O2 + OH 


Если по условию задания добавляемый раствор пероксида водорода был щелочным, то молекулярное уравнение следует записывать так:
PbO2 + H2O + KHO2 = K[Pb(OH)3] + O2
Если же в реакционную смесь, содержащую щелочь, добавляется нейтральный раствор пероксида водорода, то молекулярное уравнение может быть записано и без учета образования гидропероксида калия:
PbO2 + KOH + H2O2 = K[Pb(OH)3] + O2
Среди окислительно-восстановительных реакций выделяют реакции дисмутации (диспропорционирования, самоокисления-самовосстановления).
| Реакции дисмутации – ОВР, в которых часть атомов одного и того же элемента в одной и той же степени окисления восстанавливается, а часть – окисляется. |
Примером известной вам реакции дисмутации является реакция хлора с водой:
Cl2 + H2O 
В этой реакции половина атомов хлора(0) окисляется до степени окисления +I, а вторая половина восстанавливается до степени окисления –I:
Составим методом электронно-ионного баланса уравнение аналогичной реакции, протекающей при пропускании хлора через холодный раствор щелочи, например KOH:
| 1 | Cl2 + 2e – = 2Cl  |
| 1 | Cl2 + 4OH  – 2e – = 2ClO – 2e – = 2ClO  + 2H2O + 2H2O |
2Cl2 + 4OH 


Все коэффициенты в этом уравнении имеют общий делитель, следовательно:
Cl2 + 2OH 


Cl2 + 2KOH = KCl + KClO + H2O
Дисмутация хлора в горячем растворе протекает несколько иначе:
10

2
 – 10e – = 2ClO3
– 10e – = 2ClO3  + 6H2O
+ 6H2O3Cl2 + 6OH 


3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
Большое практическое значение имеет дисмутация диоксида азота при его реакции c водой (а) и с растворами щелочей (б):
1
 + 2H3O
+ 2H3O 
1
 – e – = NO3
– e – = NO3  + H2O
+ H2O1

1

2NO2 + 2H2O = NO3 

2NO2 + 2OH 


2NO2 + H2O = HNO3 + HNO2
2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
Реакции дисмутации протекают не только в растворах, но и при нагревании твердых веществ, например, хлората калия:
2
6
Еще один тип реакций, протекающих при нагревании твердых веществ – внутримолекулярные ОВР.
| Внутримолекулярные ОВР – ОВР, в которых атомы-окислители и атомы-восстановители входят в состав одного и того же вещества. |
Характерным и очень эффектным примером внутримолекулярной ОВР является реакция термического разложения дихромата аммония (NH4)2Cr2O7. В этом веществе атомы азота находятся в своей низшей степени окисления (–III), а атомы хрома – в высшей (+VI). При комнатной температуре это соединение вполне устойчиво, но при нагревании интенсивно разлагается. При этом хром(VI) переходит в хром(III) – наиболее устойчивое состояние хрома, а азот(–III) – в азот(0) – также наиболее устойчивое состояние. С учетом числа атомов в формульной единице уравнения электронного баланса:
1
1
а само уравнение реакции:
(NH4)2Cr2O7 = Cr2O3 + N2 

Другой важный пример внутримолекулярной ОВР – термическое разложение перхлората калия KClO4. В этой реакции хлор(VII), как и всегда, когда он выступает в роли окислителя, переходит в хлор(–I), окисляя кислород(–II) до простого вещества:
4
8
и, следовательно, уравнение реакции
KClO4 = KCl + 2O2
Аналогично разлагается при нагревании и хлорат калия KClO3, если разложение проводить в присутствии катализатора (MnO2): 2KClO3 = 2KCl + 3O2
В отсутствие катализатора протекает реакция дисмутации.
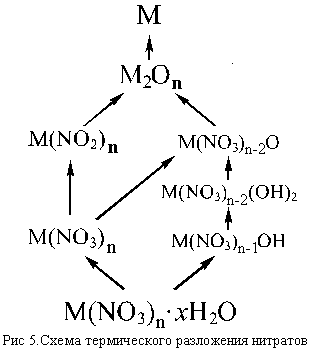
К группе внутримолекулярных ОВР относятся и реакции термического разложения нитратов.
Обычно процессы, протекающие при нагревании нитратов довольно сложны, особенно в случае кристаллогидратов. Если в кристаллогидрате молекулы воды удерживаются слабо, то при слабом нагревании происходит обезвоживание нитрата [например, LiNO3 . 3H2O и Ca(NO3)2 4H2O обезвоживаются до LiNO3 и Ca(NO3)2], если же вода связана прочнее [как, например, в Mg(NO3)2 . 6H2O и Bi(NO3)3 . 5H2O], то происходят своего рода реакции » внутримолекулярного гидролиза» с образованием основных солей – гидроксид-нитратов [Mg(NO3)OH и Bi(NO3)2OH], которые при дальнейшем нагревании могут переходить в оксид-нитраты <[Be4(NO3)6O] и [Bi6O6](NO3)6>, последние при более высокой температуре разлагаются до оксидов.
Безводные нитраты при нагревании могут разлагаться до нитритов (если они существуют и при этой температуре еще устойчивы), а нитриты – до оксидов. Если нагревание проводится до достаточно высокой температуры, или соответствующий оксид малоустойчив (Ag2O, HgO), то продуктом термического разложения может быть и металл (Cu, Cd, Ag, Hg).
Несколько упрощенная схема термического разложения нитратов показана на рис. 5.
Примеры последовательных превращений, протекающих при нагревании некоторых нитратов (температуры приведены в градусах Цельсия):
KNO3 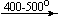
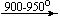
Ca(NO3)2 . 4H2O 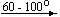
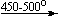
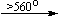
Mg(NO3)2 . 6H2O 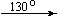
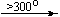
Cu(NO3)2 . 6H2O 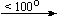

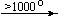
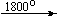
Bi(NO3)3 . 5H2O 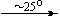
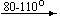
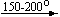
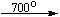
Несмотря на сложность происходящих процессов, при ответе на вопрос, что получится при » прокаливании» (то есть при температуре 400 – 500 o С) соответствующего безводного нитрата, обычно руководствуются следующими предельно упрощенными правилами:
1) нитраты наиболее активных металлов (в ряду напряжений – левее магния) разлагаются до нитритов;
2) нитраты менее активных металлов (в ряду напряжений – от магния до меди) разлагаются до оксидов;
3) нитраты наименее активных металлов (в ряду напряжений – правее меди) разлагаются до металла.
Используя эти правила, следует помнить, что в таких условиях
LiNO3 разлагается до оксида,
Be(NO3)2 разлагается до оксида при более высокой температуре,
из Ni(NO3)2 помимо NiO может получиться и Ni(NO2)2,
Mn(NO3)2 разлагается до Mn2O3,
Fe(NO3)2 разлагается до Fe2O3;
из Hg(NO3)2 кроме ртути может получиться и ее оксид.
Рассмотрим типичные примеры реакций, относящихся к этим трем типам:
KNO3 KNO2 + O2
| 2 | N +V +2e– = N +III |
| 1 | 2O– II – 4e– = O2 |
2KNO3 = 2KNO2 + O2
Zn(NO3)2 ZnO + NO2 
| 4Ѕ | N +V + e– = N +IV |
| 1Ѕ | 2O– II – 4e– = O2 |
2Zn(NO3)2 = 2ZnO + 4NO2 
AgNO3 Ag + NO2 
| 2 | Ag +1 + e– = Ag |
N +5 + e– = N +4
2AgNO3 = 2Ag + 2NO2 + O2
| ОВР конмутации – ОВР, в которых происходит выравнивание степени окисления атомов одного и того же элемента, находившихся до реакции в разных степенях окисления. |
Эти реакции могут быть как межмолекулярными, так и внутримолекулярными. Например, внутримолекулярные ОВР, протекающие при термическом разложении нитрата и нитрита аммония, относятся к реакциям конмутации, так как здесь происходит выравнивание степени окисления атомов азота:
NH4NO3 = N2O 

NH4NO2 = N2 

При более высокой температуре (250 – 300 o С) нитрат аммония разлагается до N2 и NO, а при еще более высокой (выше 300 o С) – до азота и кислорода, и в том и в другом случае образуется вода.
Примером межмолекулярной реакции конмутации является реакция, протекающая при сливании горячих растворов нитрита калия и хлорида аммония:
NH4 

Если проводить аналогичную реакцию, нагревая смесь кристаллических сульфата аммония и нитрата кальция, то, в зависимости от условий, реакция может протекать по-разному:
Первая и третья из этих реакций – реакции конмутации, вторая – более сложная реакция, включающая как конмутацию атомов азота, так и окисление атомов кислорода. Какая из реакций будет протекать при температуре выше 250 o С, зависит от соотношения реагентов.
Реакции конмутации, приводящие к образованию хлора, протекают при обработке соляной кислотой солей кислородсодержащих кислот хлора, например:
Также по реакции конмутации образуется сера из газообразных сероводорода и диоксида серы:
ОВР конмутации довольно многочисленны и разнообразны – к ним относятся даже некоторые кислотно-основные реакции, например:
Для составления уравнений ОВР конмутации используется как электронно-ионный, так и электронный баланс, в зависимости от того, в растворе протекает данная реакция или нет.
Изучая главу IX, вы познакомились с электролизом расплавов различных веществ. Так как подвижные ионы присутствуют и в растворах, электролизу могут быть подвергнуты также растворы различных электролитов.
Как при электролизе расплавов, так и при электролизе растворов, обычно используют электроды, изготовленные из материала, не вступающего в реакцию (графита, платины и т. п.), но иногда электролиз проводят и с » растворимым» анодом. » Растворимый» анод используют в тех случаях, когда необходимо получить электрохимическим способом соединение элемента, из которого изготовлен анод. При электролизе имеет большое значение разделены анодное и катодное пространство, или электролит в процессе реакции перемешивается – продукты реакции в этих случаях могут оказаться разными.
Рассмотрим важнейшие случаи электролиза.
1. Электролиз расплава NaCl. Электроды инертные (графитовые), анодное и катодное пространства разделены. Как вы уже знаете, в этом случае на катоде и на аноде протекают реакции:
K: Na 
A: 2Cl 
Записав таким образом уравнения реакций , протекающих на электродах, мы получаем полуреакции, с которыми можем поступать точно так же, как в случае использования метода электронно-ионного баланса:
K:
 + e – = Na
+ e – = NaA:
 – 2e – = Cl2
– 2e – = Cl2Сложив эти уравнения полуреакций, получаем ионное уравнение электролиза
2Na 

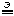
а затем и молекулярное
2NaCl 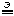
В этом случае катодное и анодное пространства должны быть разделены для того, чтобы продукты реакции не реагировали между собой. В промышленности эта реакция используется для получения металлического натрия.
2. Электролиз расплава K2CO3. Электроды инертные (платиновые). Катодное и анодное пространства разделены.
K:
 + e – = K
+ e – = KA:
 – 4e – = 2CO2
– 4e – = 2CO2  + O2
+ O2
4K+ + 2CO3 2 
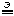


2K2CO3 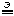

3. Электролиз воды (H2O). Электроды инертные.
K:
 + 2e – = H2 + 2H2O
+ 2e – = H2 + 2H2OA:
 – 4e – = O2 + 2H2O
– 4e – = O2 + 2H2O4H3O 

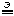


2H2O 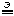

Вода – очень слабый электролит, в ней содержится очень мало ионов, поэтому электролиз чистой воды протекает крайне медленно.
4. Электролиз раствора CuCl2. Электроды графитовые. В системе присутствуют катионы Cu 2 





При электролизе растворов простые (одноатомные) анионы разряжаются (окисляются) раньше, чем сложные (многоатомные) ионы.
Следовательно в нашем случае на анода будут разряжаться хлоридные ионы.
K:
 + 2e – = Cu
+ 2e – = CuA:
 – 2e – = Cl2
– 2e – = Cl2Cu 2 

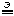
CuCl2 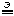
5. Электролиз раствора CuSO4. Электроды графитовые.
В водных растворах за счет автопротолиза воды (2H2O 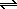







K:
 + 2e – = Cu
+ 2e – = CuK:
 + 2e – = Cu
+ 2e – = CuA:

A:

 + 6H2O
+ 6H2O 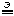 2Cu + O2
2Cu + O2  + 4H3O
+ 4H3O 
 + 2H2O
+ 2H2O 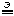 2Cu + O2
2Cu + O2  + 4H
+ 4H 
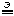 2Cu + O2
2Cu + O2  + H2SO4
+ H2SO4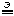 2Cu + O2
2Cu + O2  + H2SO4
+ H2SO4На катоде выделяется медь, на аноде – кислород, а в растворе накапливается серная кислота.
Ионы металлов, стоящих в ряду напряжений правее водорода, при электролизе растворов солей разряжаются.
В принципе ионы металлов, стоящих в ряду напряжений левее водорода, при электролизе водных растворов не должны разряжаться. В этих случаях должен был бы выделяться водород. Практически, из-за специфических особенностей разряда ионов водорода, при электролизе выделяются и более активные металлы.
Ионы металлов, стоящих в ряду напряжений между алюминием и водородом при электролизе растворов солей разряжаются вместе с водородом.
При этом, чем активнее металл, тем больше водорода выделяется, и тем большая часть электрической энергии расходуется бесполезно.
6. Электролиз раствора NiBr2. Электроды графитовые. Катодное и анодное пространства разделены.
K:
 + 2e – = Ni
+ 2e – = NiA:
 – 2e – = Br2
– 2e – = Br2Ni 2 

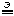
NiBr2 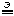
Одновременно с этим на катоде выделяется водород, в растворе накапливаются гидроксид-ионы, и, как следствие, протекает побочная реакция образования нерастворимого гидроксида никеля.
Ионы металлов, стоящие в ряду напряжений до алюминия при электролизе не разряжаются.
7. Электролиз раствора Na2SO4. Электроды платиновые. Раствор перемешивается.
В этом случае на катоде разряжаются не ионы натрия, а ионы оксония (2H3O 

K:

A:

10H2O 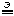



Так как раствор перемешивается, происходит реакция нейтрализации. В итоге получаем
2H2O 

то есть, реакцию электролиза воды. При электролизе воды для повышения ее электропроводности в нее специально добавляют соли с неразряжающимися катионами и анионами, что значительно ускоряет процесс электролиза.
8. Электролиз раствора CuSO4. Анод медный.
K:
 + 2e – = Cu
+ 2e – = CuA:

В результате сложения уравнений полуреакций мы можем прийти к ошибочному выводу, что ничего не происходит. На самом деле эти полуреакции описывают реальный технологический процесс электролитического рафинирования (очистки) меди: с катода, содержащего примеси на анод переходят только ионы меди.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
3*. Составьте электронно-ионные уравнения для реакции пероксида водорода с перманганатом калия, приведенной в данном параграфе.
задача №3
к главе «Задачи к § 24.5».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Перманганат калия и перекись водорода реакция уравнение
- Главная
- Список секций
- Химия
- ИССЛЕДОВАНИЕ СВОЙСТВ ПЕРОКСИДА ВОДОРОДА
ИССЛЕДОВАНИЕ СВОЙСТВ ПЕРОКСИДА ВОДОРОДА
Автор работы награжден дипломом победителя III степени
Перекись водорода (систематическое наименование — пероксид водорода, H2O2) — это самое первое из открытых соединений подобного вида. Вещество представляет собой несимметричную молекулу, состоящую из атомов водорода и кислорода, с образованием сильных полярных связей (Приложение 1). Ими обусловлены основные физико-химические свойства перекиси водорода, ее реакционная способность и активность в качестве растворителя. Перекись водородасчитается одним из сильнейших окислителей, в связи с чем это вещество получило широкое распространение, как в бытовых, так и в промышленных целях.
На бытовом уровне пероксид водорода используется в качестве эффективного антисептика для обработки открытых ран и других травм. Установлено, что растворы с концентрацией в 1 % способны полностью убивать большинство патогенных микроорганизмов, не угнетая активность клеток человеческого организма. Кроме того, пероксид водорода обладает способностью мягко очищать ткани от инородных включений. Весьма часто слабые растворы пероксида используются для обесцвечивания волос и пигментных пятен на коже, что может негативно сказаться на состоянии роговых покровов.
Промышленная сфера применения перекиси водорода значительно шире. Благодаря высоким реакционным свойствам это вещество широко используется в качестве катализатора или восстановителя в различных реакциях, в том числе — для очистки металлов. Пероксид водорода является незаменимым компонентом большинства средств бытовой химии, а также используется в пищевой промышленности в качестве безопасного антисептика. Также это вещество нашло применение в сфере энергетики: его используют в качестве окислителя для ракетного топлива, торпед и турбин.
Актуальность. Пероксид водорода интересен, во-первых, двоякостью своих свойств: с одной стороны, это типичный окислитель, но с другой стороны, при определенных условиях он проявляет восстановительные свойства. Интересно, как ведет себя соединение с необычной степенью окисления кислорода (–1). Во-вторых, его слабые растворы часто применяются в быту, а с другой стороны — учёные 19-го века не раз отмечали опасность чистого пероксида водорода.
Цель работы: изучить физические и химические свойства пероксида водорода.
Для достижения указанной цели поставлены следующие основные задачи:
выяснить историю открытия и получения H2O2;
узнать, какие физические и химические свойства характерны для исследуемого объекта;
провести эксперимент по исследованию окислительно-восстановительных свойств;
обобщить полученные сведения в учебной исследовательской работе.
Гипотеза исследования: если всесторонне изучить свойства пероксида водорода, то можно гарантировать правильное использование этого соединения.
Объект: растворы пероксида водорода различной концентрации
Предмет: исследование свойств пероксида водорода в лабораторных условиях.
Методы: эксперимент, наблюдение, сравнение, анализ результатов.
Теоретическая часть
1. Открытие пероксида водорода (историческая справка)
Впервые пероксид водорода получил в 1818 французский химик Луи Жак Тенар (1777 – 1857), действуя сильно охлажденной соляной кислотой на пероксид бария:
Пероксид бария, в свою очередь, получали сжиганием металлического бария. Для выделения из раствора Н2О2. Тенар удалил из него образовавшийся хлорид бария:
Чтобы не использовать дорогую соль серебра, в последующем для получения H2O2использовали серную кислоту, поскольку при этом сульфат бария остается в осадке:
Иногда применяли другой способ: пропускали углекислый газ во взвесь ВаО2 в воде, поскольку карбонат бария также нерастворим:
Этот способ предложил французский химик Антуан Жером Балар (1802–1876), прославившийся открытием нового химического элемента брома (1826).
Применяли и более экзотические методы, например, действие электрического разряда на смесь 97% кислорода и 3% водорода при температуре жидкого воздуха (около –190° С), так был получен 87%-ный раствор H2O2.
Концентрировали H2O2 путем осторожного упаривания очень чистых растворов на водяной бане при температуре не выше 70–75 °С – так можно получить примерно 50%-ный раствор. Сильнее нагревать нельзя – происходит разложение H2O2,поэтому отгонку воды проводили при пониженном давлении, используя сильное различие в давлении паров (и, следовательно, в температуре кипения) Н2О и Н2О2. Так, при давлении 15 мм рт.ст. сначала отгоняется в основном вода, а при 28 мм рт.ст. и температуре 69,7°С, отгоняется чистый пероксид водорода. Другой способ концентрирования – вымораживание, так как при замерзании слабых растворов лед почти не содержит Н2О2. Окончательно можно обезводить поглощением паров воды серной кислотой на холоде под стеклянным колоколом.
Многие исследователи 19 века, получавшие чистый пероксид водорода, отмечали опасность этого соединения. Так, когда пытались отделить Н2О2 от воды путем экстракции из разбавленных растворов диэтиловым эфиром с последующей отгонкой летучего эфира, полученное вещество иногда без видимых причин взрывалось. В одном из таких опытов немецкий химик Ю.В.Брюль получил безводный Н2О2, который обладал запахом озона и взорвался от прикосновения неоплавленной стеклянной палочки. Несмотря на малые количества Н2О2(всего 1–2 мл), взрыв был такой силы, что пробил круглую дыру в доске стола, разрушил содержимое его ящика, а также стоящие на столе и поблизости склянки и приборы.
2. Физические свойства
Чистый пероксид водорода очень сильно отличается от знакомого всем 3%-ного раствораH2O2. Прежде всего, он почти в полтора раза тяжелее воды (плотность при 20°С равна 1,45 г/см 3 ). ЗамерзаетH2O2 при температуре немного меньшей, чем температура замерзания воды – при минус 0,41° С, но если быстро охладить чистую жидкость, она обычно не замерзает, а переохлаждается, превращаясь в прозрачную стеклообразную массу. Растворы H2O2 замерзают при значительно более низкой температуре: 30%-ный раствор – при минус 30°С, а 60%-ный – при минус 53°С. Кипит H2O2 при температуре более высокой, чем вода – при 150,2° С. На коже чистый пероксид водорода и его концентрированные растворы оставляют белые пятна и вызывают ощущение жгучей боли из-за сильного химического ожога.
В статье, посвященной получению пероксида водорода, Тенар не очень удачно сравнил это вещество с сиропом, возможно, он имел в виду, что чистый H2O2, как и сахарный сироп, сильно преломляет свет. Действительно, коэффициент преломления безводногоH2O2(1,41) намного больше, чем у воды (1,33). Однако, то ли в результате неверного толкования, то ли из-за плохого перевода с французского, практически во всех учебниках до сих пор пишут, что чистый пероксид водорода – «густая сиропообразная жидкость», и даже объясняют это теоретически – образованием водородных связей. Но ведь вода тоже образует водородные связи. На самом деле вязкость у H2O2 такая же, как и у чуть охлажденной (примерно до 13° С) воды, но нельзя сказать, что прохладная вода густая, как сироп.
3. Химические свойства
Для перекиси водорода характерно наличие одновременно окислительных и восстановительных свойств, что объясняется особым состоянием атомов кислорода в молекуле этого вещества. Тем не менее, перекись водорода более охотно проявляет окислительные свойства при взаимодействии с металлами, гидроксидами, солями, щелочами.
При этом образуются оксиды или пероксиды других соединений, а перекись водорода восстанавливается до воды. В присутствии других сильных окислителей (кислот или активных соединений) пероксид водорода проявляет свойства восстановителя, что может быть использовано в целях очистки соединений от примесей.
Окислительно-восстановительные свойства
В молекулах пероксида водорода H2O2 атомы кислорода находятся в степени окисления –1. Это промежуточная и не самая устойчивая степень окисления атомов этого элемента, поэтому пероксид водорода проявляет и окислительные, и восстановительные свойства.
Окислительно-восстановительная активность этого вещества зависит от концентрации. В обычно используемых растворах с массовой долей 20% пероксид водорода довольно сильный окислитель, в разбавленных растворах его окислительная активность снижается. Восстановительные свойства для пероксида водорода менее характерны, чем окислительные, и также зависят от концентрации.
Пероксид водорода – очень слабая кислота, поэтому в сильнощелочных растворах его молекулы превращаются в гидропероксид-ионы.
В зависимости от реакции среды и от того, окислителем или восстановителем является пероксид водорода в данной реакции, продукты окислительно-восстановительного взаимодействия будут разными.
4. Получение
На сегодняшний день пероксид водорода получают на основе реакции с антрахиноном. Концентрация получаемого раствора варьирует в пределах от 20 до 40%. При необходимости концентрацию можно увеличить до 50-70% с помощью вакуумного дистиллятора. В вакуумном дистилляторе создается пониженное давление, в результате чего вода испаряется при температуре ниже 100 °С, в то время как пероксид водорода, температура кипения которого при нормальных условиях составляет 150,2 °С, остается в растворе. Конечный продукт хранится и транспортируется в цистернах, изготовленных из нержавеющей стали или из алюминия.
За счет добавления стабилизатора в раствор пероксида водорода мы имеем возможность значительно продлять срок его хранения, удается добиться того, чтобы за месяц распаду подвергалось менее 0,1 % вещества. Подобную защиту обеспечивают такие вещества, как станнат натрия (Nа2SnO3·ЗН20) и различные фосфаты, которые связывают все металлы, находящиеся в растворе, и не дают им катализировать разложение перекиси.
5. Применение
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель на текстильном производстве и при изготовлении бумаги (Приложение 2). Применяется как ракетное топливо, в качестве окислителя или как однокомпонентное (с разложением на катализаторе), в том числе для привода турбонасосных агрегатов. Используется в аналитической химии, в качестве пенообразователя при производстве пористых материалов, в производстве дезинфицирующих и отбеливающих средств.
При обработке ран пероксид водорода может мешать заживлению и способствовать образованию рубцов из-за разрушения новообразующихся клеток кожи. Однако в качестве средства для очистки глубоких ран сложного профиля, гнойных ран, санация которых затруднена, пероксид водорода остаётся предпочтительным препаратом, так как он обладает не только антисептическим эффектом, но и создаёт большое количество пены при взаимодействии с ферментом каталазой.
Пероксид водорода применяется также для отбеливания зубов и обесцвечивания волос, эффект в обоих случаях основан на окислении.
В пищевой промышленности растворы пероксида водорода применяются для дезинфекции технологических поверхностей оборудования, непосредственно соприкасающихся с продукцией. Кроме того, на предприятиях по производству молочной продукции и соков, растворы перекиси водорода используются для дезинфекции упаковки (технология «Тетра Пак»).
Для технических целей пероксид водорода применяют в производстве электронной техники.
В быту применяется также для выведения пятен MnO2, образовавшихся при взаимодействии перманганата калия («марганцовки») с предметами (ввиду его восстановительных свойств).
3%-ный раствор пероксида водорода используется в аквариумистике для оживления задохнувшейся рыбы, а также для очистки аквариумов и борьбы с нежелательной флорой и фауной в аквариуме.
Практическая часть.
Исследование химических свойств пероксида водорода (Приложение 3)
1. Пероксид водорода – кислота, но очень слабая. Пробуем подтвердить это. Добавляем индикатор к щелочи, затем пероксид. Светло-розовый (из-за наличия фенолфталеина) раствор гидроксида натрия обесцвечивается при добавлении пероксида водорода
2.Необычно идет окисление формальдегида: Н2О2 восстанавливается не до воды (как обычно), а до свободного водорода:
Если взять 30%-ный раствор Н2О2 (гидроперит) и 40%-ный раствор НСНО (формалин), то после небольшого подогрева начинается бурная реакция, жидкость вскипает и пенится.
3.Окислительное действие разбавленных растворов Н2О2 больше всего проявляется в кислой среде, например, при взаимодействии со щавелевой кислотой.
Наблюдали выделение бесцветного газа.
4.Под действием света идет окисление и соляной кислоты:
Небольшое выделение желто-зеленого газа.
5.Добавление Н2О2 к кислотам сильно увеличивает их действие на металлы. При добавлении разбавленной серной кислоты к меди реакция не идет (медь – неактивный металл), но в случае добавления пероксида медь начинает растворяться, при нагревании этот процесс ускорился, выделился газ, а раствор стал светло-голубым.
6. Необычно происходит окисление калий-натриевой соли винной кислоты (сегнетовой соли) в присутствии сульфата кобальта в качестве катализатора. В ходе реакции розовый CoSO4 изменяет цвет на зеленый из-за образования комплексного соединения с тартратом – анионом винной кислоты. По мере протекания реакции и окисления тартрата комплекс разрушается, и катализатор снова розовеет.
Если вместо соли кобальта использовать в качестве катализатора медный купорос CuSO4 ∙ 5H2O, то промежуточное соединение, в зависимости от соотношения исходных реагентов, будет окрашено в оранжевый или зеленый цвет. После окончания реакции восстанавливается синий цвет медного купороса.
2. Особенности окислительно-восстановительной активности
7. Реакции с перманганатом калия в разных средах
а) в нейтральной среде:
Наблюдается выпадение коричневого осадка и выделение бесцветного газа.
б) в кислой среде:
при добавлении пероксида розовый раствор перманганата калия начинает быстро светлеть: соль, придававшая окраску раствору, вступает в реакцию и образует соединения, неспособные окрашивать раствор.
в) в щелочной среде:
При добавлении гидроксида натрия раствор перманганата посветлел, после добавления пероксида водорода приобрёл желтоватый оттенок, выделился газ.
8. Реакции с хроматом калия в разных средах
а) в нейтральной среде:
Жёлтый раствор хромата калия после добавления перекиси помутнел, образовался осадок, выделился газ.
б) в кислой среде:
После добавления серной кислоты желтый раствор становится более ярким. При добавлении перекиси водорода приобретает зелёный оттенок, со временем светлеет.
в) в щелочной среде:
При добавлении перекиси в смесь растворов гидроксида натрия и хромата калия особых изменений не наблюдалось.
9. Реакции с дихроматом калия в разных средах
а) в нейтральной среде:
При добавлении перекиси в водный раствор дихромата калия стали подниматься пузырьки газа, раствор приобрёл коричневый цвет, из-за полученного гидроксида хрома (III).
После добавления пероксида водорода в смесь серной кислоты и дихромата калия раствор под влиянием сульфата хрома (III) сталярко-синим, а после посветлел.
в) в щелочной среде:
При проведении реакции особых признаков выявлено не было.
10. Реакция с сульфидом свинца
При добавлении нитрата свинца в водный раствор сульфида натрия выпал черный осадок сульфида свинца
После добавления пероксида он превратился в белый творожистый осадок
11. Реакция с нитратом серебра
После добавления пероксида водорода появились пузырьки газа, а раствор стал светло-голубым, из-за выделения кислорода и восстановления серебра.
11. Реакции с иодидом калия в разных средах
а) в нейтральной среде:
После добавления перекиси водорода раствор стал зеленоватым, из-за получившегося в ходе реакции иода.
б) в кислой среде:
При добавлении пероксида раствор сначала пожелтел, а затем стал оранжевым, выпал осадок.
в) в щелочной среде:
Видимых признаков реакции не наблюдалось.
12. Такие необычные свойства Н2О2 позволяет, например, провести окисление гексацианоферрата(II) калия, а затем, изменив условия, восстановить продукт реакции в исходное соединение с помощью того же реактива. Первая реакция идет в кислой среде, вторая – в щелочной:
Двойственный характер Н2О2 позволил одному преподавателю химии сравнить пероксид водорода с героем повести известного английского писателя Стивенсона «Странная история доктора Джекила и мистера Хайда», под влиянием придуманного им состава он мог резко изменять свой характер, превращаясь из добропорядочного джентльмена в кровожадного маньяка.
IV. Выводы
Перекись водорода, химическая формула которой H2O2, при контакте с водой распадается до составляющих, то есть на воду и кислород, поэтому перекись водорода вполне справедливо считается экологически чистым веществом, которое не может принести никакого вреда окружающей среде.
Что касается безусловной пользы перекиси водорода, то это, прежде всего, ее использование в медицинских целях. Как известно, согласно официальным рекомендациям, в медицинских целях используется перекись водорода трехпроцентная, причем назначение этого средства исключительно наружное — обработка незначительных повреждений кожи (ссадин, царапин, ран небольшого размера), остановка незначительных кровотечений, а также использование для полосканий при заболевании стоматитом.
Чем же объясняется эффект обеззараживания, который оказывает перекись водорода на различные повреждения кожных покровов? Обеззараживающий (антисептический) эффект объясняется тем, что при контакте перекиси водорода с кожей происходит высвобождение кислорода (появляется пенка), и, как следствие, рана получает возможность очиститься механическим способом — образовавшаяся кислородная пена очищает рану просто механически, вымывая микробы, грязь и даже некротические образования, которые могли уже появиться в ране.
Итак, проведя исследование физических и химических свойств пероксида водорода, я сделала выводы:
1. Такие физические свойства, как температура замерзания, температура кипения, плотность и коэффициент преломления у пероксида водорода зависят от концентрации вещества.
2. Как правило, в химических реакциях пероксид проявляет и окислительные свойства, восстанавливаясь до воды, и восстановительные, окисляясь до кислорода.
3. Использовать это удивительное соединение необходимо только учитывая его свойства.
Таким образом, я могу утверждать, что гипотеза моего исследования подтверждена.
V. Заключение
Итак, я провела планируемое исследование и узнала много нового. Над своим исследованием я трудилась очень увлеченно, мне было интересно узнать, каковы состав и строение пероксида водорода, что придает ей полезные свойства.
В перспективе мне хотелось бы обратиться к биолого-анатомическому и медицинскому аспекту данной темы, узнать, как именно влияет перекись водорода на органы и ткани человеческого организма, с чем связан ее лечебный эффект.
При подготовке работы и презентации к ней, я подробно ознакомилась с требованиями к оформлению исследовательских работ, что обязательно пригодится мне в дальнейшей учебной деятельности в школе и в вузе. Свойства пероксида водорода, изученные в теории и на практике помогут мне правильно и безопасно применять его в жизни.
VI. Литература
1. Ахметов Н. С. Общая и неорганическая химия.
2. Долгоплоск Б.А., Тинякова Е.И. Генерирование свободных радикалов и их реакции.
3. Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия.
4. Хомченко Г. П., Севастьянова К. И., Окислительно-восстановительные реакции, 2 изд., М., 1980
VII. Приложения
Приложение 1. Строение молекулы пероксида водорода H2O2
Молекула H2O2 неплоская, имеет строение H−O−O−H с σ — связью O − O на ребре и связями H-O на плоскостях двугранного угла:
молекула пероксида водорода
Степень окисления кислорода равна −I, валентность атома O равна 2. Группу -O-O- называют пероксогруппой.
Пероксид водорода H2O2 — бесцветная жидкость, неограниченно смешивается с водой.
Приложение 2. Формы выпуска пероксида водорода
Приложение 3. Фото опытов
Раствор гидроксида натрия с фенолфталеином
При добавлении пероксида обесцвечивается:
При добавлении пероксида в формальдегид начинается обильное выделение газа:
Выделение бесцветного газа при добавлении пероксида водорода в раствор щавелевой кислоты:
При добавлении перекиси водорода и при последующем нагревании медь реагирует с серной кислотой, в результате чего происходит выделение газа и изменение цвета:
Раствор перманганата калия:
При добавлении пероксида в нейтральной среде:
При добавлении пероксида в кислой среде:
При добавлении пероксида в щелочной среде:
Раствор хромата калия:
После добавления пероксида водорода к хромату калия в нейтральной среде:
При добавлении пероксида в кислой среде:
При добавлении пероксида водорода в щелочной среде:
Раствор иодида калия:
При добавлении пероксида в нейтральной среде:
http://5terka.com/3-sostavte-elektronno-ionnye-uravneniya-dlya-reaktsii-peroksida-vodoroda-s-permanganatom-kaliya-priv
http://school-science.ru/3/13/33259