Жесткое окисление алкенов. Как записать уравнение?
Жесткое окисление алкенов в кислой среде
Данный процесс чаще всего осуществляют, действуя на алкены подкисленным раствором перманганата калия, либо дихромата калия. В качестве средообразователя всегда используют серную кислоту. При таком окислении происходит полный разрыв углеродного скелета по двойной связи, и в зависимости от особенностей строения продуктами окисления могут быть различные вещества.
Давайте сначала разберемся с тем, какие углеродсодержащие продукты образуются при жестком окислении алкенов с различным строением. Представим, что у нас стоит задача определить продукты окисления для следующих двух веществ:
Обратите внимание, что углеродные атомы при двойной связи обозначены разными цветами.
Атом углерода, выделенный красным цветом, является первичным, то есть связан только с одним другим атомом углерода.
Атом углерода, выделенный желтым цветом, является вторичным, то есть связан с двумя другими атомами углерода.
Атом углерода, выделенный зеленым цветом, является третичным, то есть связан с тремя другими атомами углерода.
Жесткое окисление подразумевает разрыв углеродного скелета по месту двойной связи:
Следует запомнить, что первичные атомы углерода (красные) при таком окислении переходят в углекислый газ.
Вторичные атомы углерода (желтые) переходят в состав карбоксильной группы (COOH), то есть образуется карбоновая кислота.
Третичные атомы углерода(зеленые) переходят в состав карбонильной группы, то есть образуется кетон.
Теперь осталось разобраться с остальными продуктами реакции. Если в качестве окислителя используется сернокислый раствор перманганата калия, то продуктами будут также MnSO4, K2SO4 и H2O. Если же в качестве окислителя взяли сернокислый раствор дихромата калия, продуктами будут Cr2(SO4)3, K2SO4 и H2O.
Давайте разберем все эти случаи. Начнем с реакции пропена с сернокислым раствором перманганата калия.
Пропен + KMnO4 +H2SO4
Исходя из вышесказанного, запишем схему этой реакции:
Осталось расставить коэффициенты. Определим, какие атомы изменили степени окисления. В случае марганца ничего сложного нет: степень окисления его в перманганате была +7, стала равна +2. Также степени окисления меняют те атомы углерода, у которых изменилось окружение. В схеме эти атомы обозначены желтым и красным цветами. Определим степени окисления этих атомов методом блоков. Изолируем друг от друга фрагменты молекулы по углерод-углеродным связям следующим образом:
Далее, условно примем, что заряд каждого выделенного блока равен нулю (как у нейтральной молекулы). Степень окисления водорода в органических веществах всегда равна +1. Обозначим степени окисления «желтого» атома С как х, «красного» — как y:
Далее, учитывая, что заряд каждого блока мы приняли равным нулю, мы можем составить и решить два уравнения:
Аналогично рассчитаем степень окисления «желтого» атома углерода в уксусной кислоте и «красного» в молекуле углекислого газа, учитывая, что степень окисления кислорода в органических веществах всегда равна -2 (кроме органических пероксидов, изучение которых в не входит в программу ЕГЭ):
Далее, аналогично, составим и решим два уравнения, учитывая, что заряд выделенного блока мы приняли равным нулю, а заряд молекулы углекислого газа, как и у любой другой молекулы, также нейтрален.
Таким образом, «желтый» атом углерода имел степень окисления до реакции, равную -1, а после +3.
«Красный» атом углерода изменил свою степень окисления с -2, на +4.
Учитывая, что марганец изменил свою степень окисления с +7 на +2, еще раз запишем схему реакции и составим электронный баланс. «Желтый» и «красный» атомы углерода, очевидно, всегда будут в соотношении 1 к 1, независимо от коэффициента перед органическим веществом, потому запишем их в одной строчке «полуреакции» окисления.
Перенесем коэффициенты из баланса:
Поскольку в левой части схемы мы видим два атома калия, в правой части схемы перед сульфатом калия коэффициент 1, ставить который не нужно. В правой части уравнения мы видим 3 сульфатных остатка, поэтому ставим перед серной кислотой коэффициент 3:
Осталось поставить коэффициент перед водой в правой части. Это можно сделать по кислороду или водороду на выбор. Поскольку мы уравняли число сульфатных остатков в левой и правой частях, то кислород в них можно не учитывать. Считаем только кислород в остальных соединениях. Слева мы видим 8 атомов кислорода (не считая кислород в серной кислоте). В правой части не считая воду — 4 атома кислорода. Поэтому перед водой коэффициент будет равен 4:
Сравнивая количества всех элементов слева и справа, видим, что все коэффициенты расставлены верно.
2-метилпропен + KMnO4 + H2SO4
Аналогично предыдущему примеру рассчитаем степени окисления углеродных атомов, которые изменили свою степень окисления:
Учитывая, что заряд каждого выделенного блока мы приняли равным нулю, составим и решим уравнения:
Аналогично поступим с продуктами окисления:
составим и решим уравнения:
Таким образом, «зеленый» атом углерода до реакции имел степень окисления, равную 0, после +2, «красный» изменил свою степень окисления с -2 на +4.
Далее запишем схему окисления и составим электронный баланс:
Перенесем коэффициенты из электронного баланса в схему:
Далее мы видим, что в левой части схемы 8 атомов калия, потому перед сульфатом калия поставим коэффициент 4.
Теперь можно заметить, что в правой части уравнения 12 сульфатных групп (8 в сульфате марганца, 4 в сульфате калия). Поэтому перед серной кислотой в левой части нужно поставить коэффициент 12:
Осталось поставить коэффициент перед водой. Сделаем это по кислороду. Количество сульфатных групп мы уравняли, потому кислород в них можно не учитывать. Слева мы видим 32 атома кислорода (8*4). В правой части уравнения, не считая воды и сульфатных групп, 15 атомов кислорода (5 в молекуле кетона и 10 в 5 молекулах углекислого газа). Таким образом, перед водой необходимо поставить коэффициент 17.
Посчитав водород слева и справа, мы убеждаемся, что коэффициенты расставлены верно.
Пропен + K2Cr2O7 + H2SO4
Состав продуктов будет точно таким же, как и в случае окисления перманганатом, за исключением того, что вместо сульфата марганца (II) образуется сульфат хрома (III). Запишем схему реакции и составим электронный баланс.
Перенесем коэффициенты из баланса в схему:
Далее уравняем калий, поставив коэффициент 5 перед сульфатом калия:
В правой части мы видим 20 сульфатных групп. Следовательно, перед формулой серной кислоты нужно поставить коэффициент 20:
Осталось поставить последний коэффициент перед формулой воды. Сделаем это, как и в двух предыдущих случаях, по кислороду, не считая кислород в сульфатных группах, поскольку их количества уравнены. В левой части мы видим 35 атомов кислорода. В правой части, не считая воды, 12 атомов кислорода (6 в трех молекулах CH3COOH и 6 в трех молекулах CO2). Таким образом, перед формулой воды нужно поставить коэффициент 23:
Посчитав водород слева и справа, мы убеждаемся, что коэффициенты расставлены верно.
2-метилпропен + K2Cr2O7 + H2SO4
Запишем схему реакции и электронный баланс:
Перенесем коэффициенты из баланса в схему:
Перед сульфатом калия поставим коэффициент 4, чтобы уравнять количества атомов калия в левой и правой частях схемы:
Перед серной кислотой поставим коэффициент 16, чтобы уравнять количество сульфатных групп:
Последний коэффициент перед водой поставим по кислороду, игнорируя сульфатные группы, поскольку их количество уравнено. Слева мы видим 28 атомов кислорода. Справа, не считая воды, 9 атомов кислорода. Таким образом, перед водой необходимо поставить коэффициент 19.
Далее, подсчитав водород в обеих частях уравнения, убеждаемся, что коэффициенты расставлены верно.
Метод электронного баланса и ионно-электронный метод (метод полуреакций)
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение.
Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
Метод электронного баланса
В его основе метода электронного баланса лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
Найдем степень окисления элементов:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6. S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
3) Составить электронные уравнения и найти коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 | 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 | 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
4) Уравнять количества атомов элементов, не изменяющих степень окисления
Соблюдаем последовательность: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
6H + + 3O -2 = 3H2O
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления.
При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде).
При написании полуреакций в ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы:
H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Пример 1.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции:
2) Записать уравнение в ионном виде
В уравнении сократим те ионы, которые не принимают участие в процессе окисления-восстановления:
SO3 2- + MnO4 — + 2H + = Mn 2+ + SO4 2- + H2O
3) Определить окислитель и восстановитель и составить полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
SO3 2- + H2O — 2e — = SO4 2- + 2H +
4) Найти коэффициенты для окислителя и восстановителя
Необходимо учесть, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O |2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + |5 восстановитель, процесс окисления
5) Просуммировать обе полуреакции
Предварительно умножая на найденные коэффициенты, получаем:
2MnO4 — + 16H + + 5SO3 2- + 5H2O = 2Mn 2+ + 8H2O + 5SO4 2- + 10H +
Сократив подобные члены, находим ионное уравнение:
2MnO4 — + 5SO3 2- + 6H + = 2Mn 2+ + 5SO4 2- + 3H2O
6) Записать молекулярное уравнение
Молекулярное уравнение имеет следующий вид:
Пример 2.
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Пример 3.
Составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Еще больше примеров составления окислительно-восстановительных реакций приведены в разделе Задачи к разделу Окислительно-восстановительные реакции. Также в разделе тест Окислительно-восстановительные реакции
Окислительно – восстановительные реакции с участием перманганата калия, серной и азотной кислот
Цель работы: провести окислительно – восстановительные реакции с участием перманганата калия, серной и азотной кислот.
Оборудование и реактивы: пробирки, пипетки, резиновая груша, стеклянные стаканы, фильтровальная бумага, спиртовка, дистиллированная вода, кристаллический перманганат калия (KMnO4), концентрированные соляная, серная, азотная кислоты (HCl, H2SO4, HNO3), иодид калия (KI), 0,1Н раствор перманганата калия (KMnO4), 10% и 0,1Н раствор серной кислоты (H2SO4), 10% и концентрированный раствор гидроксида натрия (NaOH), раствор сульфита натрия (Na2SO3), гранулы цинка (Zn), медная стружка (Cu), дихромат аммония ((NH4)2Cr2O7), нитрит натрия (NaNO2), сульфат марганца (MnSO4).
Протекание химических реакций в целом обусловлено обменом частицами между реагирующими веществами. Часто обмен сопровождается переходом электронов от одной частицы к другой. Процесс потери электронов частицей называют окислением, а процесс приобретения электронов – восстановлением. Окисление и восстановление протекают одновременно, поэтому взаимодействия, сопровождающиеся переходом электронов от одних частиц к другим, называют окислительно-восстановительными реакциями.
Протекание окислительно-восстановительных реакций сопровождается изменением степеней окисления элементов участвующих в реакции веществ. При восстановлении степень окисления элемента уменьшается, при окислении – увеличивается. Вещество, в состав которого входит элемент, понижающий степень окисления, называют окислителем, вещество, в состав которого входит элемент, повышающий степень окисления, называют восстановителем.
1) В препараторской насыпали в пробирку небольшое количество кристаллического перманганата калия;
2) Добавили несколько капель концентрированной соляной кислоты (наблюдаем шипение и выделение газа — хлора);
 |



3) Поднесли к отверстию пробирки смоченную раствором йодида калия фильтровальную бумагу. Выделяющийся из пробирки хлор замещал йодид ион в растворе йодида калия. В результате этого мы наблюдали потемнение фильтровальной бумаги вокруг отверстия пробирки, связанное с выделение йода;

4) В 3 пробирки налили по 1 мл. 1Н раствора перманганата калия;
5) В первую пробирку добавили 1 мл. 10% раствор серной кислоты;
6) Во вторую пробирку 10% раствор гидроксида натрия;
7) В каждую из трёх пробирок добавили 1Н раствор сульфида натрия;
В первой пробирке (кислая среда):




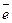
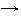
Наблюдаем обесцвечение раствора;
Во второй пробирке (щелочная среда):

 |

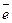

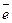

Наблюдаем появление светло – зелёной окраски, из – за появление иона (MnO4) 2- ;
В третей пробирке (нейтральная среда):



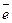

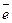

Цвет раствора стал бурым, благодаря появлению оксида марганца (IV);
Перманганат – ион проявляет более высокую окислительно – восстановительную активность в кислой среде.
8) Налили в две пробирки по 1 мл. 0,01Н раствора перманганата калия и добавили несколько капель 10% раствора серной кислоты;
9) В первую пробирку добавили добавили 1Н раствор сульфита натрия, а во вторую 1Н раствор йодида калия до появления устойчивой окраски;
Первая пробирка:



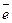

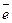
Вторая пробирка:



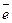

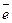

Выделяющийся йод образовывал с избытком иодида калия йодную воду, вследствие чего раствор приобрёл коричневую окраску;
10) В одну пробирку положили несколько гранул цинка, а во вторую – немного медной стружки;
11) Прилили в обе пробирки 10% раствор серной кислоты;


12) Повторили опыт с концентрированной серной кислотой;



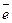

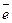




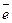

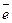

В обоих случаях наблюдаем выделение оксида серы (IV);
13) В две чистых пробирки поместили немного медных стружек;
14) В первую пробирку прилили немного концентрированной азотной кислоты, а во вторую немного разбавленной азотной кислоты;



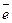
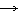
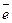


 |

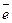
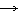
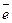

Перманганат калия, серная и азотная кислоты проявляют сильные окислительные свойства, причём наиболее сильные окислительные свойства перманганат калия проявляет в кислой среде.
http://zadachi-po-khimii.ru/obshaya-himiya/metod-elektronnogo-balansa-ionno-elektronnyj-metod-metod-polureakcij.html
http://poisk-ru.ru/s34271t3.html