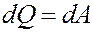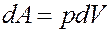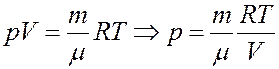Первое начало термодинамики. Применение I начала термодинамики к изопроцессам. Адиабатный процесс. Уравнение Пуассона. Скорость звука в газах.
Первое начало термодинамики является обобщением закона сохранения и превращения энергии для тепловых процессов. Первое начало было установлено, после того как экспериментально была доказана взаимосвязь теплоты и работы.
Первое начало термодинамики: количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
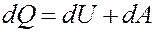
где dQ – элементарное количество теплоты, dA – элементарная работа, dU – приращение внутренней энергии.
Если dQ > 0 система получает теплоту, dQ 0 – система выполняет работу над внешними телами, dA 0, если тепловой поток направлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную работу над окружающими телами.
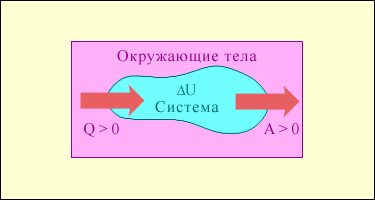 |
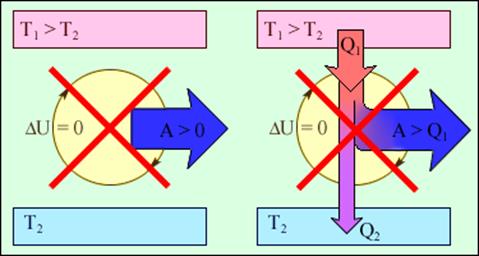
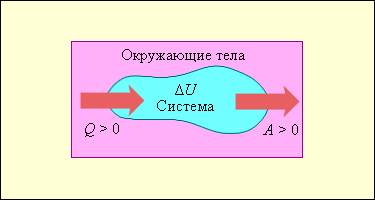
Рис.1. Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы.
Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую.
Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины. Такая гипотетическая машина получила название вечного двигателя (perpetuum mobile) первого рода. Многочисленные попытки создать такую машину неизменно заканчивались провалом. Любая машина может совершать положительную работу A над внешними телами только за счет получения некоторого количества теплоты Q от окружающих тел или уменьшения ΔU своей внутренней энергии (рис.2).
Рис.2. Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1.
Внутренняя энергия изолированной системы постоянная величина. Для такой системы dQ = 0, dA = 0, следовательно, dU = 0 и значит U = const.
Какие бы процессы не протекали в изолированной системе, ее внутренняя энергия остается постоянной.
Если незамкнутая система выполняет круговой процесс, т.е. в результате его система возвращается в первоначальное состояние, то dU = U2—U1 = 0, следовательно, из (1) dQ = dA. То есть вся теплота, полученная системой, идет на выполнение работы. Отсюда вытекает невозможность создания вечного двигателя первого рода.
Применим I начало термодинамики к изопроцессам.
1). Изотермический процесс: T = const.
Внутренняя энергия идеального газа определяется выражением:
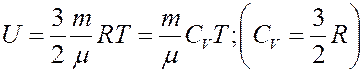
где CV – молярная теплоемкость при постоянном объеме. Определим изменение внутренней энергии.
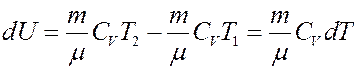
Если T = const, то dU = 0 и из I начала термодинамики получим:
Теплота, полученная системой, идет на выполнение работы над внешними телами. Определим величину этой работы (рис.3).
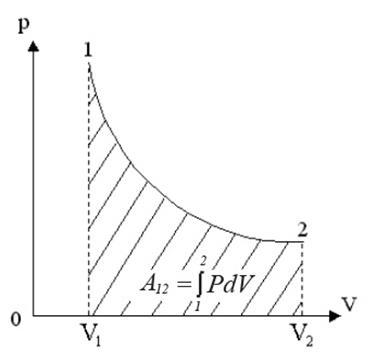
Рис.3. Работа при изотермическом процессе
Элементарная работа определяется выражением:
Из уравнения Клапейрона-Менделеева:
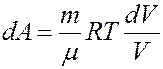
Проинтегрировав (4) найдем работу:
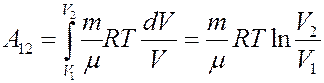
Работа численно равна площади под кривой 1 → 2. При расширении V2 > V1, и A12 > 0 система выполняет работу. При сжатии V2 V1 и A12 > 0, газ выполняет работу. При сжатии V2 T1, то Q12 > 0 газ получает тепло и его внутренняя энергия увеличивается, а если T2
| | | следующая лекция ==> | |
| Устройство пола из древесины | | | Политропический процесс. Теплоемкость. Принцип равномерного распределения энергии по степеням свободы и границы его применимости. |
Дата добавления: 2015-05-21 ; просмотров: 7353 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Первое начало термодинамики для атмосферы
ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ В АТМОСФЕРЕ
Первое начало термодинамики для атмосферы
Атмосфера представляет собой воздушную среду, в которой постоянно осуществляется переход энергии из одного вида в другие. Раздел метеорологии, рассматривающий общие закономерности преобразования энергии и изменения состояния атмосферы под влиянием притока тепла называется термодинамикой атмосферы.
В этом разделе широко используются выводы, вытекающие из первого начала термодинамики или закона сохранения энергии:
ü Невозможно возникновение или уничтожение энергии, возможен лишь переход одних видов энергии в другие.
Количественно это положение выражается в виде
уравнения первого начала термодинамики или
уравнения притока тепла.
Для вывода этого уравнения выделим в атмосфере частицу сухого воздуха единичной массы. К характеристикам, определяющим состояния этой частицы относятся рi, ρi,Ti, а к характеристикам, определяющим состояние окружающего эту частицу воздуха ре, ρе, Те.
В силу малой скорости движения частицы (по сравнению со скоростью звука), можно ввести допущение, что между характеристиками окружающего воздуха и выделенной частицы выполняются квазистатические условия, т. е.: рi = pe= p.
Рассмотрим изменение характеристик выделенной частицы при получении этой частицей количества тепла, равного dg. Это количество тепла будет израсходовано на увеличение внутренней энергии и
совершение работы на увеличение объема, занимаемого данной частицей.
В этом случае ее внутренняя энергия увеличится на du и совершится работа dw против внешних сил давления на увеличение объема:
Для идеального газа, к которому можно отнести и сухой и влажный ненасыщенный воздух, изменение внутренней энергии частицы справедливо выражение:
где cv — удельная теплоемкость сухого воздуха при постоянном объеме (v = const). Работа по расширению объема частицы определяется из выражения:
где dvi– приращение объема частицы.
С учетом полученных выражений (3.2) и (3.3) уравнение первого начала термодинамики для выделенного объема воздуха примет вид:
После преобразования выражения (3.4) получим:
Для изобарического процесса (dр = 0) выражение (3.7) примет вид:
Для данного вида процесса справедливо выражение:
где ср — удельная теплоемкость воздуха при постоянном давлении.
Соотношение (3.11) носит название уравнения Майера.
Для сухого воздуха: cv = 718 Дж/кг К, а сp = 1006 Дж/кг К,

Подставим (3.10) в (3.7), тогда с учетом (3.5) получим
уравнение первого начала термодинамики:
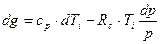
3.2. Адиабатический процесс
Термодинамический процесс называется адиабатическим, если он протекает без теплообмена частицы с окружающей средой.
При адиабатическом процессе dg = 0. Для такого процесса уравнения
(3.4) и (3.14) принимают вид:

Уравнение (3.15) показывает, что при адиабатическом процессе работа против внешних сил давления совершается только за счет внутренней энергии.
При этом, если работа положительная, т.е. направленная на расширение объема (dvi > 0), то внутренняя энергия частицы уменьшается (dТi 0), ее внутренняя энергия растет (dТi > 0).
При подъеме частицы объем ее увеличивается (dvi > 0), а давление падает (dр
Подставим (3.19) в (3.17) и после сокращения запишем:

Разделим выражение (3.20) на выражение (cp · dz):

Полученное выражение (3.21) определяет изменение температуры воздушной частицы, отнесенное к единице высоты при адиабатическом процессе.
ü Данное выражение показывает, что при адиабатическом подъеме воздушной частицы температура ее всегда падает
Это связано с тем, что при подъеме воздушной частицы происходит расход внутренней энергии на работу расширения.
Сухоадиабатическимградиентом 

Подставим (3.22) в (3.21) и получим:

Для реальной атмосферы 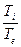
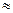
градиент для реальной атмосферы – величина постоянная (const).

Приближенно можно считать, что температура адиабатически поднимающейся воздушной частицы падает примерно на один градус при подъеме на каждые 100 м высоты.
Изменение с высотой температуры адиабатически поднимающейся воздушной частицы графически изображается в осях координат – температура – высота, в виде прямой линии. Она называется сухоадиабатой или кривой состояния сухой воздушной частицы.
3.4. Потенциальная температура
Потенциальной температурой ( 
Приближенное выражение для расчета потенциальной температуры имеет вид:

где р0 – давление воздуха на поверхности Земли;
Тi – температура воздуха на исходной поверхности;
z – расстояние перемещения частицы по вертикали.
В выражении (3.25) последнее слагаемое правой части представляет собой изменение температуры частицы при перемещении ее от поверхности Земли до уровня 1000 гПа.
Если давление воздуха у поверхности Земли менее 1000 гПа, то уровень 1000 гПа лежит ниже поверхности Земли. Поэтому при дополнительном перемещении частицы от поверхности земли до уровня 1000 гПа частица нагревается.
Потенциальная температура обладает важными свойствами.
§ При сухоадиабатическом перемещении частицы ее потенциальная температура сохраняет постоянное значение, хотя ее температура (как степень нагретости) изменяется.
Это свойство сохранения (консервативности) потенциальной температуры используется в качестве характеристики воздушных масс и оценки их вертикальных перемещений.
§ Если при перемещении частицы ее потенциальная температура изменилась, то это свидетельствует о притоке, либо оттоке тепла.
Другим свойством потенциальной температуры является ее связь с полной энергией воздушной частицы.
§ При адиабатическом перемещении частицы ее полная энергия не изменяется.
3.5. Критерии устойчивости атмосферы на основе метода частицы
Распределение температуры окружающего частицу воздуха в различных слоях атмосферы характеризуется вертикальным градиентом температуры
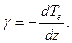
Распределение температуры и других метеорологических величин по высоте называется стратификацией атмосферы.
Для определения устойчивости к движению воздуха выделим в атмосфере воздушную частицу единичного объема. Характеристикой изменения температуры частицы является сухоадиабатический градиент 
При вертикальном движении частицы возможны три случая с разными соотношениями между вертикальным и сухоадиабатическим градиентами.
Первый случай: 


При 



Второй случай: 


Термическое состояние атмосферы в этом случае при 
Третий случай: 
Первый закон термодинамики
На рисунке 3 . 9 . 1 условно проиллюстрированы энергетические потоки между выделенной термодинамической системой и окружающими телами. В случае, если тепловой поток направлен к термодинамической системе, то некоторая величина Q > 0 , если же система совершает положительную работу над окружающими ее объектами, то справедливо неравенство A > 0 .
Рисунок 3 . 9 . 1 . Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы.
Состояние системы меняется, когда происходит процесс ее обмена теплом с окружающими объектами, и она совершает положительную или отрицательную работу. Изменяются макроскопические параметры системы, такие как температура, объем и давление. По причине того, что внутренняя энергия U всецело определяется макроскопическими параметрами, которые характеризуют состояние системы, процессы совершения работы и теплообмена провоцируют изменения внутренней энергии данной системы Δ U .
Определение 1 -го закона термодинамики
Первый закон термодинамики представляет собой некое обобщение закона сохранения и превращения энергии для термодинамической системы, и формулируется следующим образом:
Изменение Δ U внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q , переданной системе, и работой A , совершенной системой над внешними телами.
Формула первого закона термодинамики, зачастую записывается в ином виде:
Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
Первый закон термодинамики представляет из себя, по сути, обобщение опытных фактов. Если руководствоваться им, то можно заявить, что энергия не возникает и не исчезает бесследно, а передается от одной системы к другой, меняя свои формы. Невозможность создания вечного двигателя (perpetuum mobile) первого рода, то есть машины, которая может совершать полезную работу, не потребляя энергию извне и не претерпевая каких-либо изменений во внутренней конструкции агрегата, являлась важным следствием первого закона термодинамики. В подтверждение этого выступает тот факт, что каждая из огромного множества попыток создания такого устройства неизменно заканчивалась неудачей. Реальная машина может совершать положительную работу A над внешними объектами, только получая некоторое количество теплоты Q от окружающих тел или уменьшая Δ U своей внутренней энергии.
Первый закон термодинамики в процессах газов
Первый закон термодинамики может применяться к изопроцессам в газах.
В изохорном процессе, то есть в условиях неизменного объема ( V = c o n s t ) , газ не совершает работы, A = 0 .
В этом случае справедливой будет формула внутренней энергии газа:
Q = ∆ U = U ( T 2 ) — U ( T 1 ) .
В данном выражении U ( T 1 ) и U ( T 2 ) представляют внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит лишь от температуры, что исходит из закона Джоуля. При изохорном нагревании газ поглощает тепло ( Q > 0 ) , чем провоцирует увеличение его внутренней энергии. В условиях охлаждения тепло отдается внешним объектам ( Q 0 ) .
В изобарном процессе, предполагающем постоянность значения давления ( p = c o n s t ) , работа, совершаемая газом, выражается в виде соотношения:
A = p ( V 2 — V 1 ) = p ∆ V .
Первый закон термодинамики для изобарного процесса дает:
Q = U ( T 2 ) — U ( T 1 ) + p ( V 2 — V 1 ) = ∆ U + p ∆ V .
При изобарном расширении Q > 0 тепло поглощается газом, и он совершает положительную работу. При изобарном сжатии Q 0 тепло переходит внешним телам. В таком случае A 0 . При изобарном сжатии уменьшаются температура газа T 2 T 1 и значение внутренней энергии Δ U 0 .
В изотермическом процессе температура газа не меняет своей величины, следовательно, не изменяется и внутренняя энергия газа, Δ U = 0 .
Первый закон термодинамики для изотермического процесса выражается соотношением
Теплота Q , приобретенная газом в процессе изотермического расширения, превращается в работу, совершаемую над внешними объектами. И наоборот, изотермическое сжатие приводит к преобразованию уже работы внешних сил, произведенной над газом, в передающееся окружающим телам тепло.
Вместе с изохорным, изотермическим и изобарным процессами в термодинамике нередко исследуют процессы, происходящие в условиях отсутствующего теплообмена с окружающими объектами.
Адиабатическая оболочка – это сосуд с теплонепроницаемыми стенками.
Процессы сжатия или расширения газа в подобных емкостях называют адиабатическими.
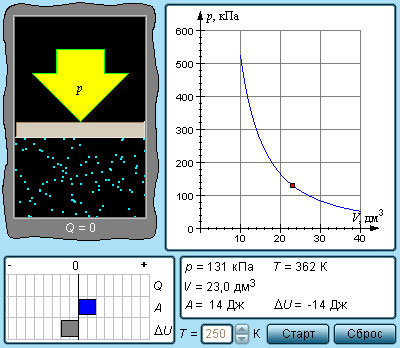
Рисунок 3 . 9 . 2 . Модель адиабатического процесса.
В адиабатическом процессе Q = 0 . По данной причине первый закон термодинамики принимает вид:
Выходит, что газ производит работу за счет падения значения его внутренней энергии.
Расширение или сжатие газа на плоскости p , V проиллюстрирована кривой, называемой адиабатой.
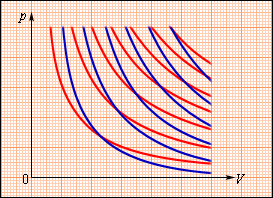
В процессе адиабатического расширения газом совершается положительная работа A > 0 , что является причиной понижения значения внутренней энергии Δ U 0 . Данное явление провоцирует падение его температуры. Исходя из этого, можно заявить, что величина давления газа при адиабатическом расширении понижается быстрее, чем это происходит в изотермическом (рис. 3 . 9 . 3 ).
Рисунок 3 . 9 . 3 . Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа.
В условиях координат ( p , V ) выводящееся в термодинамике уравнение адиабатического процесса для идеального газа принимает следующий вид:
p V γ = c o n s t .
Данное выражение, в котором γ = C p C V – показатель адиабаты, C p и C V – теплоемкости газа в процессах с постоянным давлением и с постоянным объемом, называется уравнением Пуассона. В условиях одноатомного газа γ = 5 3 = 1 , 67 , двухатомного γ = 7 5 = 1 , 4 , многоатомного γ = 1 , 33 .
Работа газа в адиабатическом процессе выражается через температуры начального T 1 и конечного T 2 состояний и принимает вид:
A = C V ( T 2 — T 1 )
Адиабатический процесс относится к изопроцессам.
В термодинамике важное место занимает физическая величина, называемая энтропией. Изменение энтропии в том или ином квазистатическом процессе эквивалентно некоторому обретенному системой теплу Δ Q T . Так как на каждом участке адиабатического процесса Δ Q = 0 , энтропия в нем не претерпевает изменений.
Любые изопроцессы, в том числе и адиабатические, являются квазистатическими. Промежуточные состояния газа в таких процессах близки к состояниям термодинамического равновесия. Каждая точка, принадлежащая адиабате, описывает равновесное состояние. Однако, процесс, который проводится в адиабатической оболочке, то есть при отсутствующем теплообмене с окружающими объектами, не обязательно удовлетворяет данному условию.
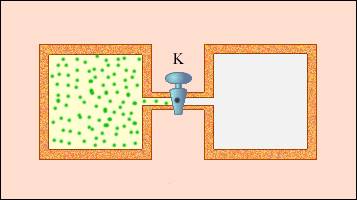
Примером неквазистатического процесса, в котором промежуточные состояния не находятся в состоянии равновесия, служит расширение газа в пустоту. На рисунке 3 . 9 . 3 иллюстрируется жесткая адиабатическая оболочка, состоящая из двух разделенных вентилем K сообщающихся емкостей. В изначальном состоянии газом заполнен один из сосудов, в это же время во втором находится лишь вакуум. Открытие вентиля запускает процесс расширения газа. Он заполняет оба сосуда, и устанавливается новое равновесное состояние.
В таком процессе Q = 0 , по той причине, что исключен теплообмен с окружающими телами, и A = 0 , так как оболочка недеформируема. Первый закон термодинамики позволяет сказать, что Δ U = 0 , то есть внутренняя энергия газа не претерпела никаких изменений. Так как внутренняя энергия идеального газа зависит лишь от температуры, температура газа в начальном и конечном состояниях одинакова. Изображающие эти состояния точки на плоскости ( p , V ) лежат на одной изотерме. Все промежуточные состояния газа не являются равновесными и не могут быть изображены на диаграмме.
Расширение газа в пустоту – пример необратимого процесса. Его нельзя провести в противоположном направлении.
Рисунок 3 . 9 . 4 . Расширение газа в пустоту.
http://lektsii.org/13-77028.html
http://zaochnik.com/spravochnik/fizika/termodinamika/pervyj-zakon-termodinamiki/