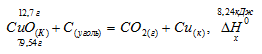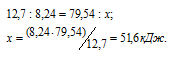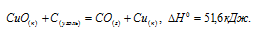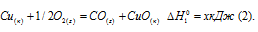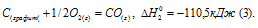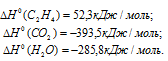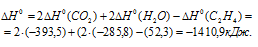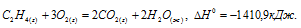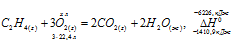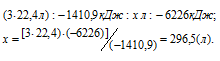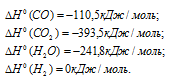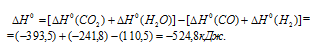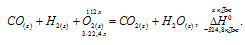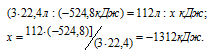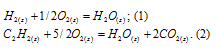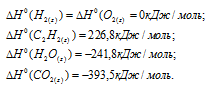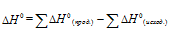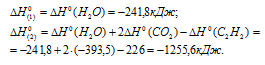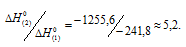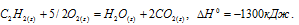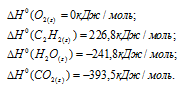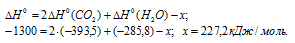По термохимическому уравнению реакции c2h4 h2o
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Приведите по два примера экзотермических и эндотермических реакций.
Экзотермические реакции:
N2 (г) + 3H2 (г) ⇄ 2NH3 (г) + 92 кДж
С (тв) + О2 (г) = СО2 (г) + 410 кДж
Эндотермические реакции:
CaCO3 (тв) = CaO (тв) + CO2 (г) ― 170 кДж
N2 (г) + O2 (г) = 2NO (г) ― 180 кДж
Задание 2
Даны термохимические уравнения нескольких реакций. Какие из них являются экзотермическими; эндотермическими?
а) 4P (тв) + 5O2 (г) = 2P2O5 (тв) + 2984 кДж; Экзотермическая реакция
б) 2Al (тв) + Fe2O3 (тв) = Al2O3 (тв) + 2Fe (тв) + 850 кДж; Экзотермическая реакция
в) N2 (г) + O2 (г) = 2NO (г) ― 180 кДж; Эндотермическая реакция
г) C6H12O6 (тв) + 6O2 (г) = 6CO2 (г) + 6H2O (ж) + 2800 кДж. Экзотермическая реакция
Задание 3
При кристаллизации свинца из расплава происходит выделение теплоты. Какой это процесс – экзо- или эндотермический? Экзотермический процесс, так как происходит выделение теплоты.
Задание 4
Пользуясь данными, приведёнными в параграфе, составьте термохимическое уравнение разложения жидкой воды на водород и кислород.
2Н2О (ж) = 2H2 (г) + O2 (г) ― 572 кДж
Задание 5
Дано термохимическое уравнение синтеза аммиака: N2(г) + 3H2(г) = 2NH3(г) + 92 кДж. Рассчитайте, сколько теплоты выделится при образовании:
а) 10 моль;
Решение
По термохимическому уравнению с 2 моль NH3 выделяется 92 кДж теплоты,
По условию задачи с 10 моль NH3 ― х кДж теплоты.
х=10 моль ● 92 кДж : 2 моль=460 кДж
Ответ: 460 кДж
б) 10 г;
Решение
По термохимическому уравнению с 34 г (2 моль) NH3 выделяется 92 кДж теплоты,
По условию задачи с 10 г NH3 ― х кДж теплоты.
х=10 г ● 92 кДж : 34 г=27 кДж
Ответ: 27 кДж
в) 10 л (н.у.) аммиака.
Решение
По термохимическому уравнению с 44,8 л (2 моль) NH3 выделяется 92 кДж теплоты,
По условию задачи с 10 л NH3 ― х кДж теплоты.
х=10 л ● 92 кДж : 22,4 л =20,5 кДж
Ответ: 20,5 кДж
Задание 6
Теплота сгорания угля равна 393,5 кДж/моль. Напишите термохимическое уравнение реакции. Рассчитайте количество теплоты, которое выделится при сгорании 1 кг угля. Какой объём углекислого газа (н.у.) образовался, если при сгорании угля выделилось 157,4 кДж теплоты?
Решение
C 12 г (1 моль) С выделяется 393,5 кДж теплоты,
с 1000 г С ― х кДж теплоты.
х=393,5 кДж : 12 г = 32780 кДж
С 22,4 л (1 моль) СО2 выделяется 393,5 кДж теплоты,
с х л СO2 ― 157,4 кДж теплоты.
х=157,4 кДж ● 393,5 кДж: 22,4 л=8,96 л
Ответ: выделится 32780 кДж теплоты, образуется 8,96 л углекислого газа.
Задание 7
На разложение 19,7 г карбоната бария на оксид бария и углекислый газ затратили 27,2 кДж теплоты. Напишите термохимическое уравнение этой реакции.
Решение
Составляем термохимическое уравнение с указанием агрегатного состояния веществ:
BaCO3 (т.) = BaO (т.) + CO2 (г.)
По термохимическому уравнению на 197 г (1 моль) BaCO3 затратили х кДж теплоты,
По условию задачи на 19,7 г BaCO3 ― 27,2 кДж теплоты
х=197 ● 27,2 кДж : 19,7 г = 272 кДж
Термохимическое уравнения реакции имеет вид: BaCO3 (т.) = BaO (т.) + CO2 (г.) -272 кДж
Задание 8
Рассчитайте количество теплоты, которая выделится при сгорании 1 м 3 (н.у.) природного газа, содержащего 90% метана CH4, 8% этана C2H6 и 2% пропана C3H8 (по объёму). Теплоты сгорания метана, этана и пропана равны соответственно 802, 1428 и 2045 кДж/моль.
Дано: V(смеси)=1 м 3 =1000 л, φ(CH4)=90%, φ(C2H6)=8%, φ(C3H8)=2%,
Найти: Q-?
Решение
V(CH4)=φ(CH4)●V(смеси):100%=90% ● 1000 л : 100%=900 л
V(C2H6)=φ(C2H6)●V(смеси):100%=8% ● 1000 : 100%=80 л
V(C3H8)=φ(C3H8)●V(смеси):100%=2% ● 1000 : 100%=20 л
С 22,4 л (1 моль) СH4 выделяется 802 кДж теплоты,
с 900 л СH4 ― x кДж теплоты.
х=802 кДж ● 900 л : 22,4 л=32223 кДж
С 22,4 л (1 моль) С2H2 выделяется 1428 кДж теплоты,
с 80 л С2H2 ― у кДж теплоты.
у=1428 кДж ● 80 л : 22,4 л=5100 кДж
С 22,4 л (1 моль) С3H8 выделяется 2045 кДж теплоты,
с 20 л С2H2 ― z кДж теплоты.
z=2045 кДж ● 20 л : 22,4 л=1826 кДж
Q =х + y + z= 32223 кДж + 5100 кДж + 1825 кДж = 39150 кДж
Ответ: Q=39150 кДж
Задание 9
Термохимическое уравнение реакции разложения воды на простые вещества: 2H2O (г) = 2H2 (г) + O2(г) — 484 кДж. Сколько теплоты надо затратить для разложения 90 г газообразной воды?
Решение
По термохимическому уравнению на 36 г (2 моль) H2O затратится 484 кДж теплоты,
По условию задачи на 90 г H2O ― х кДж теплоты.
х=90 г ● 484 кДж : 36 г=1210 кДж
Ответ: надо затратить 1210 кДж
Задание 10
Теплоты сгорания метана и ацетилена равны соответственно 802 и 1260 кДж/моль. Какой из двух газов даёт больше теплоты при сгорании: а) 1 кг вещества;
Решение
С 16 г (1 моль) СH4 выделяется 802 кДж теплоты,
с 1000 г СH4 ― х кДж теплоты.
х=1000 г ● 802 кДж : 16 г=50125 кДж
С 26 г (1 моль) C2H2 выделяется 1260 кДж теплоты,
с 1000 г С2H2 ― у кДж теплоты.
у=1000 г ● 1260 кДж : 26 г=48461 кДж
QCH4 > QC2H2
Ответ: 1 кг метана CH4 дает больше теплоты при сгорании.
б) 1 м 3 (н.у.) вещества.
Решение
С 22,4 л (1 моль) СH4 выделяется 802 кДж теплоты,
с 1000 л СH4 ― х кДж теплоты.
х= QCH4= 1000 л ● 802 кДж : 22,4 л=35804 кДж
С 22,4 л (1 моль) С2H2 выделяется 1260 кДж теплоты,
с 1000 л С2H2 ― y кДж теплоты.
y= QC2H2= 1000 л ● 1260 кДж : 22,4 л=56250 кДж
QCH4 QC2H2
Ответ: 1 м 3 ацетилена C2H2 дает больше теплоты при сгорании.
Задание 11
Используя данные задачи 2, определите тепловой эффект реакции фотосинтеза: 6CO2 (г) + 6H2O (ж) = C6H12O6 (тв) + 6O2 (г).
Дано: Qобр.(CO2)=393,5 кДж/моль, Qобр.(H2O)=286 кДж/моль, Qобр.(C6H12O6)=1274 кДж/моль
Найти: Qреакции=?
Решение
На 1 моль СO2 затрачивается 393,5 кДж теплоты,
на 6 моль CO2 ― х кДж теплоты.
х= Q1=6 моль ● 393,5 кДж : 1 моль=2361 кДж
На 1 моль H2O затрачивается 286 кДж теплоты,
на 6 моль H2O ― х кДж теплоты.
х= Q2=6 моль ● 286 кДж : 1 моль=1716 кДж
На 1 моль C6H12O6 затрачивается 1274 кДж теплоты, поэтому Q3= 1274 кДж
Qреакции= Q1— Q2— Q3= 1274 кДж — 1716 кДж — 2361 кДж=-2803 кДж
Ответ: Qреакции= -2803 кДж
Откуда берётся энергия, необходимая для этой реакции? Энергия солнца
Залание 12
Теплота сгорания водорода равна 286 кДж/моль. Используя данные задач 6 и 8, определите, какое топливо – уголь, водород или метан – даёт больше теплоты в расчёте на единицу массы (например, 1 г).
Решение
С 44 г (1 моль) С выделяется 393,5 кДж теплоты,
с 1 г C ― х кДж теплоты.
х= QС=1 г ● 393,5 кДж : 10 г=39,35 кДж
С 2 г (1 моль) H2 выделяется 286 кДж теплоты,
с 1 г H2 ― х кДж теплоты.
х= QH2=1 г ● 286 кДж : 2 г=143 кДж
С 16 г (1 моль) CH4 выделяется 802 кДж теплоты,
с 1 г CH4 ― х кДж теплоты.
х= QCH4=1 г ● 802 кДж : 16 г=50,125 кДж
QH2> QCH4> QC
Ответ: при сгорании водород даёт больше теплоты в расчёте на единицу массы, чем метан и уголь.
Задания 28. Расчеты объемных отношений газов при химической реакции. Тепловой эффект.
В результате реакции, термохимическое уравнение которой
выделилось 1452 кДж теплоты. Вычислите массу образовавшейся при этом воды (в граммах). (Запишите число с точностью до целых.)
Ответ: 108
Пояснение:
Из уравнения реакции следует, что при образовании 2 моль воды выделяется 484 кДж теплоты. У нас же выделилось 1452 кДж теплоты. Составим пропорцию
2 моль H2O — 484 кДж
x моль H2O — 1452 кДж
2 : x = 484 : 1452
x = 2 ∙ 1452 /484 = 6
т.е. n(H2O) = 6 моль, следовательно:
При взаимодействии оксида серы (IV) с 5,6 л (н.у.) кислорода в соответствии с уравнением
выделилось 19 кДж теплоты. Определите тепловой эффект реакции. (Запишите число с точностью до целых.)
Ответ: 76
Пояснение:
Рассчитаем количество вещества кислорода:
Т.е. при взаимодействии 0,25 моль кислорода с оксидом серы (IV) выделяется 19 кДж теплоты. Из представленного в условии термохимического уравнения следует, что при взаимодействии 1 моль кислорода с оксидом серы выделяется количество теплоты равное Q (тепловой эффект реакции). Тогда справедлива пропорция:
0,25 моль кислорода — 19 кДж
1 моль кислорода — Q
Исходя из этой пропорции:
Таким образом, тепловой эффект реакции составляет 76 кДж.
В соответствии с термохимическим уравнением реакции
выделилось 786 кДж теплоты. Какой объем (н.у.) углекислого газа при этом образовался? (Запишите число с точностью до десятых.)
Ответ: 44,8
Пояснение:
В соответствии с термохимическим уравнением реакции при образовании 1 моль углекислого газа выделяется 393 кДж теплоты. В нашем же случае вместо этого выделилось 786 кДж теплоты. Обозначив искомое количество вещества углекислого газа равным х моль, можно записать пропорцию:
1 моль CO2 — 393 кДж теплоты
x моль CO2 — 786 кДж теплоты
Следовательно, справедливо уравнение:
Решая которое получаем:
Т.е. количество вещества углекислого газа при образовании которого выделяется 786 кДж теплоты составляет 2 моль.
Рассчитаем объем такого количества углекислого газа при н.у.:
V(CO2) = 2 моль ∙ 22,4 л/моль = 44,8 л
В соответствии с термохимическим уравнением реакции
выделилось 2406 кДж теплоты. Определите объем (н.у.) израсходованного кислорода в литрах. (Запишите число с точностью до десятых.)
Ответ: 134,4
Пояснение:
Согласно термохимическому уравнению при участии в реакции горения метана 2 моль кислорода выделяется 802 кДж теплоты. В нашем же случае выделяется количество теплоты равное 2406 кДж. Обозначив количество вещества кислорода необходимое для выделения 2406 кДж теплоты через х моль мы можем записать следующую пропорцию:
2 моль O2 — 802 кДж теплоты
x моль O2 — 2406 кДж теплоты
Тогда, справедливо следующее уравнение:
2 ∙ 2406 = 802 ∙ x
Решая которое находим ,что:
Таким образом, количество вещества кислорода равно 6 моль. Рассчитаем его объем:
V(O2) = 6 ∙ 22,4 = 134,4 л.
Вычислите количество теплоты, которое потребуется для получения 25 г железа согласно уравнению реакции
(Запишите число с точностью до целых.)
Ответ: 6
Пояснение:
Рассчитаем количество вещества железа:
n(Fe) = m(Fe)/M(Fe) = 25/56 = 0,4464 моль,
Согласно термохимическому уравнению при образовании 2 моль металлического железа поглощается 27 кДж теплоты. Пусть количество поглощаемой в результате образования 0,4464 моль железа равно х кДж. Тогда можно записать пропорцию:
2 моль Fe — 27 кДж
0,4464 моль Fe — x кДж
Следовательно, справедливо уравнение:
2 ∙ x = 0,4464 ∙ 27
Таким образом, количество теплоты, которое необходимо для получения 25 г железа равно 6 кДж.
Вычислите объем сгоревшего согласно уравнению реакции
ацетилена, если при этом выделилось 67,5 кДж теплоты. (Запишите число с точностью до сотых.)
Ответ: 1,12
Пояснение:
Согласно термохимическому уравнению при сгорании 2 моль ацетилена выделяется 2700 кДж теплоты. В нашем же случае выделилось 67,5 кДж. Пусть, количество вещества ацетилена, которое сгорело при этом равно х моль. Таким образом можно записать пропорцию:
x моль — 67,5 кДж
2 ∙ 67,5 = 2700 ∙ x
Таким образом, количество вещества ацетилена равно 0,05 моль. Рассчитаем его объем:
V(C2H2) = 0,05 моль ∙ 22,4 л/моль = 1,12 л
В результате реакции, термохимическое уравнение которой
выделилось 280 кДж теплоты. Вычислите массу глюкозы, которая окислилась в результате этой реакции. (Запишите число с точностью до целых.)
Ответ: 18
Согласно термохимическому уравнению при окислении 1 моль глюкозы выделяется 2800 кДж теплоты. В нашем же случае выделилось 280 кДж теплоты. Пусть количество глюкозы, которое окислилось при этом равно x моль. Тогда можно записать следующую пропорцию:
1 моль глюкозы – 2800 кДж теплоты
x моль глюкозы – 280 кДж теплоты
Следовательно, справедливо уравнение:
1 ∙ 280 = 2800 ∙ x
Решая которое находим, что:
x = 0,1 моль, т.е. количество глюкозы составляет 0,1 моль. Рассчитаем ее массу:
Какое количество вещества аммиака вступает в реакцию в соответствии с термохимическим уравнением
если в результате реакции выделилось 634 кДж теплоты? (Запишите число с точностью до целых.)
Ответ: 2
Пояснение:
Согласно термохимическому уравнению при окислении 4 моль аммиака выделяется 1268 кДж теплоты. В нашем же случае выделилось 634 кДж теплоты. Обозначим количество вещества аммиака, которое при этом окислилось как x моль. Тогда можно записать пропорцию:
4 моль аммиака – 1268 кДж
x моль аммиака – 634 кДж
Следовательно, справедливо уравнение:
4 ∙ 634 = 1268 ∙ x
Решая которое находим, что:
x = 2, т.е. количество вещества аммиака составляет 2 моль.
В соответствии с термохимическим уравнением реакции
получено 1400 кДж теплоты. Какая масса (в граммах) глюкозы при этом окислилась? (Запишите число с точностью до целых.)
Ответ: 90
Пояснение:
Согласно термохимическому уравнению при окислении 1 моль глюкозы выделяется 2800 кДж теплоты. В нашем же случае выделилось 1400 кДж теплоты. Пусть количество глюкозы, которое окислилось при этом равно x моль. Тогда можно записать следующую пропорцию:
1 моль глюкозы – 2800 кДж теплоты
x моль глюкозы – 1400 кДж теплоты
Следовательно, справедливо уравнение:
1 ∙ 1400 = 2800 ∙ x
x = 0,5, т.е. количество вещества глюкозы для получения 1400 кДж тепла составляет 0,5 моль. Рассчитаем ее массу:
В соответствии с термохимическим уравнением реакции
выделилось 240 кДж теплоты. Определите массу полученного оксида магния. (Запишите число в точностью до целых.)
Ответ: 16
Пояснение:
Согласно термохимическому уравнению при образовании 2 моль оксида магния выделяется 1200 кДж теплоты. В нашем же случае выделилось 240 кДж теплоты. Пусть количество оксида магния, образовавшегося при этом равно x моль. Тогда можно записать пропорцию:
2 моль MgO – 1200 кДж
x моль MgO – 240 кДж
Следовательно, справедливо уравнение:
2 ∙ 240 = 1200 ∙ x
Решая которое находим, что:
x = 0,4, т.е. при выделении 240 кДж теплоты количество вещества образовавшегося оксида магния составляет 0,4 моль. Тогда его масса равна:
m(MgO) = n(MgO) ∙ M(MgO) = 0,4 ∙ 40 = 16 г
В ходе реакции, термохимическое уравнение которой
было затрачено 450 кДж теплоты. Определите объем (н.у.) получившегося при этом газа. (Запишите число с точностью до целых.)
Ответ: 56
Пояснение:
Выделившийся газ – CO2.
В соответствии с термохимическим уравнением при образовании одного моля CO2 поглощается 180 кДж теплоты. В нашем же случае поглощено 450 кДж теплоты. Обозначив количество вещества углекислого газа, образовавшегося при этом как x моль, можно записать следующую пропорцию:
1 моль CO2 – 180 кДж
x моль CO2 – 450 кДж
Следовательно, справедливо уравнение:
x = 2,5, т.е. количество вещества углекислого газа составляет 2,5 моль. Рассчитаем его объем:
В соответствии с термохимическим уравнением реакции
образовалось 168 г железа. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Ответ: 1110
Пояснение:
Рассчитаем количество вещества железа с массой 168 г:
n(Fe) = m(Fe)/M(Fe) = 168/56 = 3 моль,
В соответствии с термохимическим уравнением реакции при образовании 9 моль металлического железа выделяется 3330 кДж. В нашем же случае образуется 3 моль железа. Обозначив количество теплоты выделившейся при этом как x кДж можно составить пропорцию:
9 моль Fe — 3330 кДж
3 моль Fe — x кДж
тогда справедливо уравнение:
Таким образом, количество теплоты выделяющееся при образовании 168 г металлического железа составляет 1110 кДж.
Определите количество теплоты, которое выделится при взаимодействии 280 г негашеной извести с водой в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 324
Пояснение:
Негашеная известь — тривиальное название оксида кальция CaO. Рассчитаем его количество вещества, зная массу:
n(CaO) = 280 г/ 56 г/моль = 5 моль,
В соответствии с термохимическим уравнением реакции при взаимодействии с водой 1 моль CaO выделяется количество теплоты равное 64,8 кДж. В нашем же случае в реакции принимает участие 5 моль оксида кальция, в связи с чем мы можем записать следующую пропорцию:
1 моль CaO — 64,8 кДж
5 моль CaO — x кДж
Следовательно, справедливо уравнение:
Решая которое находим, что:
Таким образом, количество теплоты, которое выделится при взаимодействии 280 г негашеной извести водой составляет 324 кДж.
В результате реакции, термохимическое уравнение которой
выделилось 6620 кДж теплоты. Определите массу образовавшегося оксида железа (III). (Запишите число с точностью до целых.)
Ответ: 640
Пояснение:
В соответствии с термохимическим уравнением реакции при образовании 2 моль Fe2O3 выделяется 3310 кДж теплоты. В нашем же случае, выделилось 6620 кДж теплоты. Пусть количество вещества Fe2O3, образовавшегося при этом составляет x моль. Тогда можно записать следующую пропорцию:
Следовательно, справедливо уравнение:
2 ∙ 6620 = x ∙ 3310
Решая которое находим, что:
Таким образом, количество вещества Fe2O3 образовавшееся при этом составляет 4 моль. Следовательно масса образовавшегося Fe2O3 составляет:
При образовании 560 мл (н.у.) газообразного аммиака в соответствии с уравнением
выделилось 1,15 кДж теплоты. Чему равен тепловой эффект этой реакции? (Запишите число с точностью до целых.)
Ответ: 92
Пояснение:
Посчитаем какое количество вещества содержится в 560 мл газообразного аммиака. Прежде всего переведем его объем из мл в л:
Теперь, зная, что 1 моль любого газа при н.у. занимает объем равный 22,4 л, можно рассчитать количество вещества аммиака:
Из условия задания следует, что при образовании 0,025 моль (0,56 л) аммиака выделилось 1,15 кДж теплоты. В термохимическом же уравнении реакции фигурирует количество вещества аммиака равное 2 моль (коэффициент 2 перед NH3) и при этом выделяется количество тепла, равное Q (тепловой эффект реакции). Таким образом, мы можем записать следующую пропорцию:
0,025 моль — 1,15 кДж
Следовательно справедливо уравнение:
0,025 ∙ Q = 2 ∙ 1,15 кДж
Решая которое находим, что:
Т.е. тепловой эффект реакции равен 92 кДж.
В соответствии с термохимическим уравнением реакции
восстановили 464 г железной окалины. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Ответ: 2220
Пояснение:
Рассчитаем количество вещества железной окалины массой 464 г:
В соответствии с термохимическим уравнением реакции при восстановлении 3 моль Fe3O4 выделяется 3330 кДж теплоты. Пусть при восстановлении 2 моль Fe3O4 выделяется x кДж теплоты. Тогда можно составить следующую пропорцию:
Следовательно, справедливо уравнение:
Решая которое, получаем, что:
Таким образом, количество теплоты, выделившейся при восстановлении 464 г железной окалины составляет 2220 кДж.
В соответствии с термохимическим уравнением реакции
выделилось 2406 кДж теплоты. Определите объем (н.у.) израсходованного кислорода. (Запишите число с точностью до десятых.)
Ответ: 134,4
Пояснение:
В соответствии с термохимическим уравнением реакции при реакции с метаном 2 моль кислорода выделяется 802 кДж. В нашем же случае выделилось 2406 кДж теплоты. Пусть количество вещества израсходованного при этом кислорода составляет x моль. Тогда можно записать пропорцию:
2 моль O2 – 802 кДж
x моль O2 – 2406 кДж
Следовательно, справедливо уравнение:
2 ∙ 2406 = 802 ∙ x
Т.е. количество вещества кислорода составляет 6 моль. Найдем его объем:
В соответствии с термохимическим уравнением реакции
получено 422,2 кДж теплоты. Какой объем (н.у.) кислорода при этом израсходован? (Запишите число с точностью до целых.)
Ответ: 24
Пояснение:
В соответствии с термохимическим уравнением при израсходовании на горение угля 1 моля кислорода выделяется 393 кДж теплоты. В нашем же случае выделяется 422,2 кДж. Пусть при выделении такого количества теплоты расходуется x моль кислорода. Тогда, мы можем записать пропорцию:
1 моль O2 – 393 кДж
x моль O2 – 422,2 кДж
Следовательно, справедливо уравнение:
1 ∙ 422,2 = 393 ∙ x
Решая которое находим, что:
т.е. количество вещества израсходованного кислорода составляет 1,0743 моль. Рассчитаем его объем:
Какой объем (н.у.) кислорода потребуется для получения 5600 кДж теплоты в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до десятых.)
Ответ: 268,8
Пояснение:
Исходя из термохимического уравнения:
6 моль O2 — 2800 кДж теплоты
В нашем же случае должно выделиться 5600 кДж. Пусть количество вещества кислорода необходимое для выделения такого количества тепла составляет x моль. Тогда справедлива пропорция:
6 моль O2 — 2800 кДж теплоты
x моль O2 — 5600 кДж теплоты
Следовательно, верным является уравнение:
6 ∙ 5600 = 2800 ∙ x
Таким образом, количество вещества кислорода, которое должно принять участие в окислении глюкозы для выделения 5600 кДж теплоты, составляет 12 моль. Рассчитаем объем такого количества кислорода при н.у.:
При сжигании ацетилена в соответствии с термохимическим уравнением реакции
выделилось 186 кДж теплоты. Какой объем (н.у.) кислорода затрачен на сжигание ацетилена? (Запишите число с точностью до десятых.)
Ответ: 22,4
Пояснение:
Из термохимического уравнения реакции следует, что когда в реакции принимает участие 5 моль O2 выделяется 930 кДж теплоты.
В нашем же случае выделяется 186 кДж теплоты. Пусть количество вещества кислорода, израсходованного при этом, составляет x моль. Тогда мы можем записать следующую пропорцию:
5 моль O2 – 930 кДж
x моль O2 – 186 кДж
Следовательно, справедливо уравнение:
Решая которое находим, что:
Таким образом, количество вещества кислорода составляет 1 моль. Найдем его объем:
В соответствии с термохимическим уравнением реакции
выделилось 2580 кДж теплоты. Определите количество вещества оксида азота(IV), вступившего в реакцию. (Запишите число с точностью до целых.)
Ответ: 40
Пояснение:
Из термохимического уравнения реакции следует, что когда в реакции принимает участие 4 моль NO2 выделяется 258 кДж теплоты.
В нашем же случае выделяется 2580 кДж теплоты. Пусть количество вещества оксида азота (IV), прореагировавшего при этом, составляет x моль. Тогда мы можем записать следующую пропорцию:
4 моль NO2 – 258 кДж
x моль NO2 – 2580 кДж
Следовательно, справедливо уравнение:
4 ∙ 2580 = x ∙ 258
Решая которое находим, что:
Таким образом, количество вещества оксида азота (IV) составляет 40 моль.
Определите объём газообразного продукта (в литрах), который получается при взаимодействии 1 л водорода с избытком хлора. Объёмы газов измерены при одинаковых условиях. (Запишите число с точностью до целых.)
Ответ: 2
Пояснение:
Запишем уравнение реакции взаимодействия водорода с хлором:
Одним из следствий закона Авогадро является то, что объемы прореагировавших и образовавшихся газов относятся друг к другу точно так же, как и коэффициенты перед этими газообразными веществами в уравнении реакции. Для газообразных водорода и хлороводорода, применительно к нашей реакции, мы можем записать что:
V(HCl) = V(H2) ∙ k(HCl)/k(H2) = 1 л ∙ 2/1 = 2 л
Определите количество теплоты, которое выделяется при окислении серы кислородом взятым в объёме 100,8 л (н.у.) в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 1341
Определите количество теплоты, которое выделится при обжиге 720 г FeS2 согласно термохимическому уравнению реакции
(Запишите число с точностью до целых.)
Ответ: 4965
Вычислите количество выделившейся теплоты, если в реакцию вступает 3,5 моль кислорода в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 903
Какое количество теплоты выделится при взаимодействии 3,6 моль кремния с фтором в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 5814
В реакцию, термохимическое уравнение которой
вступило 88 г углекислого газа. Какое количество теплоты выделится при этом? (Запишите число с точностью до целых.)
Энергетика химических реакций. Тепловой эффект реакции
Задача 288.
При восстановлении 12,7г оксида меди (II) углем (с образованием СО) поглощается 8,24кДж. Определить 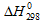
Решение:
Уравнение реакции имеет вид:
Находим тепловой эффект реакции восстановления оксида меди (II) углем из пропорции:
Значит, 
Обозначим искомую величину через x, запишем термохимическое уравнение образования CuO:
Из уравнения (20 и (3) можно получить уравнение (4). Для этого нужно вычесть уравнение (2) из уравнения (3), получим:
Сравнивая уравнение (1) и (4), получим:
Ответ: 162,1 кДж/моль.
Задача 289.
При полном сгорании этилена (с образованием жидкой воды) выделилось 6226 кДж. Найти объем вступившего в реакцию кислорода (условия нормальные).
Решение:
Уравнение реакции горения этилена:
Учитывая данные значения теплот образования веществ, находим 
Запишем данные задачи в уравнение, получим:
Рассчитаем объём кислорода, вступившего в реакцию с этиленом из пропорции:
Ответ: V(O2)=296,5 л.
Задача 290.
Водяной газ представляет собой смесь равных объемов водорода и оксида углерода (II). Найти количество теплоты, выделившейся при сжигании 112л водяного газа, взятого при нормальных условиях.
Решение:
Уравнение реакции сжигания водяного газа имеет вид:
Рассчитаем теплоту, которая выделяется при сжигании водяного газа, используя следствие из закона Гесса:
Следовательно, термохимическое уравнение будет иметь вид:
Рассчитаем теплоту, выделяющуюся при сжигании 112 л водяного газа из пропорции:
Ответ: Q = -1312 кДж.
Задача 291.
Сожжены с образованием Н2О(г) равные объемы водорода и ацетилена, взятых при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз?
Решение:
Уравнения реакций сгорания водорода и ацетилена:
Стандартные теплоты образования исходных веществ и продуктов реакций находим из таблицы, получим:
Для расчета теплоты, которая будет выделяться при сгорании водорода и ацетилена, используем следствие из закона Гесса:
Рассчитаем, во сколько раз больше выделяется теплоты при сгорании ацетилена:
Таким образом, при сгорании равных объемов водорода и ацетилена, взятых при одинаковых условиях в случае ацетилена выделится больше теплоты в 5,2 раза.
Ответ: При сжигании С2Н2 в 5,2 раза больше
Задача 292.
Определить 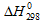
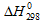
О2(г) и Н2О(ж) равно —1300кДж/моль, а 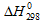
Решение:
Уравнение реакции горения ацетилена имеет вид:
Стандартные теплоты образования исходных веществ и продуктов реакций находим из таблицы, получим:
Обозначим искомую величину [

Уравнение реакции образования бензола имеет вид:
3C2H2 ⇔ C6H6, 
Находим 
http://scienceforyou.ru/reshenie-realnyh-zadanij-egje-2016-goda/raschety-obemnyh-otnoshenij-gazov-pri-himicheskoj-reakcii-teplovoj-jeffekt
http://buzani.ru/zadachi/khimiya-glinka/1129-teplovoj-effekt-reaktsii-zadach