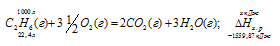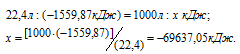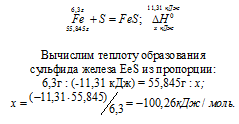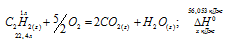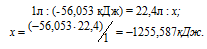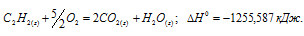Реакция горения бензола выражается термохимическим уравнением: С6Н6(ж) + 7 1/2 О2(г) = 6СО2(г)
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,299
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,247
- разное 16,834
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Правильный расчет теплового эффекта реакций и теплот образования веществ
Тепловой эффект реакции
Задание 95.
Реакция горения бензола выражается термохимическим уравнением:
С6Н6(ж) + 15/2О2(г) = 6СО2(г) + 3Н2О(г); 
Вычислите тепловой эффект этой реакции, если известно, что молярная теплота парообразования бензола равна +33,9 кДж. Ответ: —3135,58 кДж.
Решение:
∆H°С6Н6(парообр.) = +33,9 кДж/моль;
∆H°С6Н6(г) = +82,9 кДж/моль;
∆H°Н2О = -241,98 кДж/моль;
∆H°СО2 = -393,51 кДж/моль;
(С6Н6(ж) → (С6Н6(г); ∆H = +33,9 кДж;
ΔН = ?
Зная мольную теплоту парообразования и мольную теплоту образования газообразного бензола, рассчитаем мольную теплоту образования жидкого бензола из соотношения:
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:
Ответ: ΔН = -3136 кДж.
Задание 96.
Вычислите тепловой эффект и напишите термохимическое уравнение реакции горения 1 моля этана С2Н6(г), в результате которой образуются пары воды и диоксид углерода. Сколько теплоты выделится при сгорании 1 м 3 этана в пересчете на нормальные условия? Ответ: 63742,86 кДж.
Решение:
Уравнение реакции горения этана имеет вид:
С2Н6 (г) + 31/2O2 = 2СО2(г) + 3Н2О (ж); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:
Рассчитаем теплоту, выделяющуюся при сжигании 1м 3 этана из пропорции:
Ответ: . Q = 69637,05 кДж.
Теплота образования вещества
Задание 97.
Реакция горения аммиака выражается термохимическим уравнением:
4NH3(г) + 3O2 (г) = 2N2(г) + 6Н2O(ж); 
Ответ: —46,19 кДж/моль.
Решение:
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном дав-лении Qp равные изменению энтальпии системы 

Термохимическое уравнение реакции имеет вид:
4NH3(г) + 3O2 (г) = 2N2(г) + 6Н2O(ж); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:



Отсюда вычислим теплоту образования NH3:
4 


4 
4

Ответ: –46,19 кДж/моль.
Задание 98.
При взаимодействии 6,3 г железа с серой выделилось 11,31 кДж теплоты. Вычислите теплоту образования сульфида железа ЕеS. Ответ: —100,26 кДж/моль.
Решение:
Уравнение реакции имеет вид:
Ответ: —100,26 кДж/моль.
Задание 99.
При сгорании 1 л ацетилена (н.у.) выделяется 56,053 кДж теплоты. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксида углерода. Вычислите теплоту образования С2Н2(г). Ответ. 226,75 кДж/моль.
Решение:
Уравнение реакции горения ацетилена имеет вид:
Рассчитаем теплоту, выделяющуюся при сжигании 1моль ацетилена из пропорции:
Термохимическое уравнение реакции горения ацетилена будет иметь вид:
Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:




Отсюда вычислим теплоту образования С2Н2:




Ответ: 226,75 кДж/моль.
Задание 100.
При получении молярной массы эквивалента гидроксида кальция из СаО(к) и Н2О(ж) выделяется 32,53 кДж теплоты. Напишите термохимическое уравнение этой реакции и вычислите теплоту образования оксида кальция. Ответ: –635,6 кДж.
Решение:
Так как молярная масса эквивалента гидроксида кальция равна 1/2M(Са(ОН)2), то при по-лучении 1моль его выделится 65,06 кДж теплоты (2 . 32,53 = 65,06).
Термохимическое уравнение получения гидроксида кальция из СаО(к) и Н2О(ж) будет иметь вид:
СаО(к) + Н2О(ж) = Са(ОН)2(к); 
Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:




Отсюда вычислим теплоту образования С2Н2:





Реакция горения бензола выражается термохимическим уравнением:
С6Н6(ж) + 7 1/2 О2(г)
Реакция горения бензола выражается термохимическим уравнением:
С6Н6(ж) + 7 1/2 О2(г) = 6СО2(г) + 3Н2О(г) 3135,6 кДж.
Вычислите теплоту образования жидкого бензола. Определите теплотворную способность водянистого бензола при условии, что стандартные условия совпадают с нормальными.
- Стефания Гумбарова
- Подготовка к ЕГЭ/ОГЭ 2019-10-30 20:45:32 2 1
Тепловой эффект реакции равен:
Hр-цииnbsp;=nbsp;H 0 конnbsp;nbsp;H 0 исхnbsp;кДж/моль
В нашем случаеnbsp;Hр-цииnbsp;= 3135,6 кДж, найдем теплоту образования жидкого бензола:
Hр-ции=nbsp;6H 0 СO2nbsp;+ 3H 0 H2Onbsp;nbsp;nbsp;H 0 C6H6nbsp; 7,5H 0 O2
-H 0 C6H6nbsp;=nbsp;Hр-цииnbsp; 3(-241,84) + 6(- 393,51) 7,50 = 3135,6 3(-241,84) + 6(- 393,51) 7,50 = 49,02 кДж/моль
H 0 C6H6nbsp;= 49,02 кДж/моль
Теплотворная способностьnbsp;водянистого бензола рассчитывается по формуле:
М(бензола) = 78 г/моль
QТnbsp;= 3135,6 1000 / 78 = 4,0210 4 nbsp;кДж/кг
Теплотворная способностьnbsp;водянистого бензолаnbsp;QТnbsp;= 4,0210 4 nbsp;кДж/кг
http://buzani.ru/zadachi/khimiya-shimanovich/914-teplovoj-effekt-reaktsii-teplota-obrazovaniya-veshchestv-zadanie-95-100
http://obrazovalka.com/qa/ege-oge/13861357-reakcija-gorenija-benzola-vyrazhaetsja-termohimicheskim-uravneniembr-s6n6zh-7-12-o2g.html