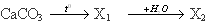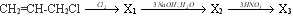1.Верны ли следующие суждения о карбоновых кислотах?
А Химические свойства карбоновых кислот обусловлены прежде всего атомом водорода гидроксильной группы.
Б. Самая сильная из одноосновных карбоновых кислот — муравьиная кислота.
1)Верно только А; 3) верны оба суждения;
2)верно только Б; 4) оба суждения неверны.
2. В отличие от этаналя, уксусная кислота взаимодействует с веществом, формула которого:
1) Са; 2) Сu(ОН)2; 3) Н2; 4) О2.
3. Реакция «серебряного зеркала» характерна для вещества, формула которого:
1) CH3COOH; 3) C2H5OH;
2) НСООН; 4) СН3СООС4Н9.
4. Сложный эфир можно получить при взаимодействии пропановой кислоты:
1)с этанолом; 3) с этаналем;
2)с этаном; 4) с пропеном-1.
5. В химических реакциях муравьиная кислота проявляет свойства:
1)спирта и альдегида;
2)спирта и карбоновой кислоты;
3)альдегида и карбоновой кислоты;
4)алкена и альдегида.
6. По углеводородному радикалу у карбоновых кислот происходит взаимодействие:
1)с солями; 3) с основаниями;
2)со спиртами; 4) с галогенами.
7. Уравнение реакции, в которой в реакцию вступает вся гидроксильная группа:
1)2СН3СООН + Mg → (CH3COO)2Mg + H2↑;
2)СН3СООН + Cl2 → СlСН2-СООН + НСl;
3)СН3СООН + NaOH → CH3COONa + Н2О;
4)СН3СООН + С2Н5ОН → СН3СООС2Н5 + Н2О.
8. Химическая реакция, уравнение которой C17H35COONa + Н2О С17Н35СООН + NaOH,
относится к реакциям:
1) соединения; 3) гидратации;
2) гидролиза; 4) замещения.
9. Верны ли следующие суждения о химических свойствах карбоновых кислот?
А. Карбоновые кислоты — сильные электролиты.
Б. По углеводородному радикалу карбоновые кислоты реагируют с галогенами.
1)верно только А; 3) верны оба суждения;
2)верно только Б; 4) оба суждения неверны.
10. С образованием воды идет реакция между:
1)масляной кислотой и хлором;
2)уксусной кислотой и магнием;
3)муравьиной кислотой и глицерином;
4)олеиновой кислотой и водородом.
12. Верны ли следующие суждения о химических свойствах сложных эфиров?
А. В реакции этерификации образуется вода.
Б. При образовании сложных эфиров от кислоты отщепляется атом водорода, а от спирта — ОН-группа.
1) верно только А;
2) верно только Б;
3)верны оба суждения;
4)оба суждения неверны.
13. Уравнение химической реакции, по которой можно судить о том, что у карбоновых кислот может вступать в реакцию углеводородный радикал:
1) 2СН3СООН + Са → (СН3СОО)2Са + Н2↑;
2)СН3СООН + КОН → СН3СООК + Н2О;
3)СН3СООН + Вг2 → ВгСН2СООН + НВг;
4)НСООН + С3Н7ОН → НСООС3Н7 + Н2О.
14. Масляная кислота будет реагировать с каждым из веществ, формулы которых:
1) С4Н9ОН, К2О, Вг2;
2)Mg3(PО4)2, ZnO, CH3OH;
3)Си, CuSО4, Cu(OH)2;
4)С3Н7ОН, НСl, Na2COs.
15. Блестящий налет серебра на стенках пробирки появляется в результате реакции аммиачного раствора оксида серебра с веществами, формулы которых:
При выполнении заданий данной части выберите правильный ответ, щелкнув мышью на кнопке с его номером.
Тест 1
Вопрос. Электронная коyфигурация 1s 2 2s 2 2p 6 3s 2 3p 6 соответствует частице
Тест 2
Вопрос. В порядке возрастания атомного радиуса химические элементы расположены в ряду:
Тест 3
Вопрос. В аммиаке и хлориде бария химическая связь соответственно
Тест 4
Вопрос. Одинаковую степень окисления фосфор имеет в соединениях
Тест 5
Вопрос. Кристаллическую структуру, подобную структуре алмаза, имеет
Тест 6
Вопрос. К амфотерным оксидам относится
Тест 7
Вопрос. В каком ряду химические элементы расположены в порядке усиления металлических свойств?
Тест 8
Вопрос. В ряду элементов: азот → кислород → фтор увеличивается
Тест 9
Вопрос. С водой без нагревания реагирует
Тест 10
Вопрос. Оксид углерода(IV) реагирует с каждым из двух веществ:
Тест 11
Вопрос. Гидроксид алюминия реагирует с каждым веществом
Тест 12
Вопрос. В уравнении реакции
веществом «X» является
Тест 13
Вопрос. В схеме превращений
веще ством « X2 » является
Тест 14
Вопрос. Изомерами являются
Тест 15
Вопрос. Число σ-связей пропионовой кислоты равно
Тест 16
Вопрос. При окислении метанола оксидом меди(II) образуется
Тест 17
Вопрос. По углеводородному радикалу проходит реакция, уравнение которой
Тест 18
Вопрос. В цепочке превращений
конечным веществом «X3» является
Тест 19
Вопрос. К какому из приведённых типов реакций можно отнести реакцию ионного обмена?
Тест 20
Вопрос. Для уменьшения скорости химической реакции необходимо
Тест 21
Вопрос. Изменение давления оказывает влияние на смещение равновесия в системе
Тест 22
Вопрос. Вещество, при диссоциации которого образуются катионы Na + , H + ,а также анионы SO4 2- , является
Тест 23
Вопрос. Образование осадка происходит при взаимодействии
Тест 24
Вопрос. Окислительно-восстановительной является реакция, уравнение которой
Тест 25
Вопрос. Кислую среду имеет водный раствор
Тест 26
Вопрос. Продуктом реакции бутена-1 с хлором является
Тест 27
Вопрос. Между собой могут взаимодействовать
Тест 28
Вопрос. Верны ли следующие суждения о свойствах концентрированной серной кислоты?
А. Серная кислота обугливает органические вещества, отнимая от них воду.
Б. Попадание кислоты на кожу приводит к тяжёлым ожогам.
Тест 29
Вопрос. Продуктами обжига пирита FeS2 являются
Тест 30
Вопрос. В соответствии с термохимическим уравнением
1206 кДж теплоты выделяется при горении угля массой
Разработка урока «Свойства карбоновых кислот»
Стригина Ирина Николаевна, учитель химии МАОУ СОШ №2 Режевской ГО
Цели урока: на примере уксусной кислоты изучение химические свойства предельных одноосновных карбоновых кислот; показать сходство и отличие неорганических и органических кислот; развитие умения записывать химические реакции с участием органических веществ; формирование приёмов аккуратного и безопасного обращения с химическими веществами; развитие критического мышления, самостоятельности и способности к рефлексии;
Тип урока: урок изучения и первичного закрепления новых знаний.
Используемые технологии: технология критического мышления, ИКТ.
Приёмы обучения: лабораторный опыт, маркировка текста, работа в парах и группах, дидактические игры.
Оборудование и реактивы: для каждой группы — листы бумаги формата А1, маркеры; этиловый спирт, уксусная кислота, серная кислота, штатив, спиртовка, держатель, стакан с водой, штатив с пробирками.
| Содержание слайда | Деятельность учителя | Деятельность обучающихся | ||
| I. ОРГАНИЗАЦИОННЫЙ МОМЕНТ | ||||
| Слайд №1 Тетрадь Ручка Учебник (1 мин.) Дело | Проверка готовности к уроку | Контролируют свою подготовку к уроку | ||
| II. АКТУАЛИЗАЦИЯ ОПОРНЫХ ЗНАНИЙ. МОТИВАЦИЯ УЧЕБНОЙ ДЕЯТЕЛЬНОСТИ | ||||
| Слайд №2 Что общего? (2 мин.) | Что объединяет помещённые на слайде изображения с точки зрения химии? кислоты: муравьиная, лимонная, яблочная, уксусная) | |||
| Слайд №3-5 Зашифрованная фраза MCDOЯFKCSKУSJДВОИАWBSL Аристотель (384–322 гг. до н. э.) «Познание начинается с удивления» Аристотель (384–322 гг. до н. э.) (3 мин.) | Задание: автором, которой является Аристотель Согласны ли вы с данным утверждением? . Проверим | Отгадывают фразу, затем высказываются: согласны с данным утверждением или нет, аргументируют. | ||
| Слайд №6. Верите ли вы в то, что… · в течение суток в организм человека образуется 400 г уксусной кислоты, что хватило бы для изготовления 8 л столового уксуса; · отвинтить ржавую гайку — 18 л уксуса в сутки»? (3 мин.) | Проводится игра «Верите ли вы в то, что…»: · Некоторые из карбоновых кислот получаются и расходуются в процессе обмена веществ в очень внушительных количествах. Например, в течение суток в организме человека образуется 400 г уксусной кислоты, что хватило бы для изготовления 8 л обычного уксуса. · Для отвинчивания ржавой гайки, например, на коллекторе автомашины, надо вечером положить на неё тряпку, смоченную в уксусной кислоте. Тогда утром отвинтить эту гайку будет значительно легче. · Однажды учёные ввели в компьютер сведения о калорийности различных пищевых продуктов и о сезонных колебаниях их стоимости, а компьютер должен был составить наиболее экономичное меню. После расчётов машина ответила: «Оптимальное меню — 18 л уксуса в сутки» | |||
| Слайд №7 Можно ли прожить без знаний о КК? (1 мин.) | · Может быть и можно, но, чтобы считать людьми, обязаны знать, что мы едим и пьем, с чем мы имеем дело в быту, что происходит в нашем организме. · Знать чем опасны эти вещества, с чем они могут прореагировать. | Обучающиеся высказывают свое мнение | ||
| (3 мин.) Слайд 8-9 Кислоты реагируют | 1. Впервые ли вывстречаетесь с кислотами как класс соединений? 3. Вспомните, пожалуйста, с чем реагировали неорганические кислоты? | Класс кислот изучался в курсе неорганической Если есть сходство в стро ении, то оно есть и в хи- Называют те классы соединений, с которыми вступают во взаимодейс- твие кислоты. | ||
| Так с чем же могут реагировать КК? . Почему нельзя одновременно употреблять в пищу кислые фрукты, соки, маринады и антибиотики пенициллинового ряда? | Кислоты, содержащиеся в этих продуктах, могут вступать в химическое взаимодействие с антибиотиками и нейтрализовать их действие формулирование темы урока. | Формулируют тему | ||
| Слайд №10 Тема урока «Свойства карбоновых кислот» | Записывают тему в тетрадь | |||
| III. ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА | ||||
| . ХРОМОТЕРАПИЯ – лечение цветом (желтый – солнце, интуиция стимулирует нервную систему; синий – спокойствие, ум, снижает раздражительность; зеленый – эмоциональное равновесие, восстанавливает силы; оранжевый – стимулирует деятельность сердца. | ||||
| Слайд №11 Памятка для обучающегося Внимательно читая текст, отмечай значками на полях (справа или слева), насколько новая и понятная для тебя «?» — не понял, есть вопросы (5 мин.) Гимнастика для глаз | Организую работу с (См.Приложение1)голубой | Читая текст, маркируют памяткой. | ||
| Совместный анализ маркировки текста, выделяя новые знания и переходя к лабораторному эксперименту (реакция этерификации) | ||||
| Слайд №12 Лабораторный опыт «Взаимодействие карбоновых кислот со спиртами» Будьте аккуратны, соблюдайте правила ТБ. (3 мин.) (Оранжевый лист) | Вспоминают правила ТБ | |||
| Слайд №13 Время опыта – 5 мин. карбоновых кислот со спиртами», используя инструкцию | Изучают инструкцию, планируют опыт, выполняют его, записывают уравнение реакции | |||
| Слайд №14 (2 мин.) | Запись уравнения на доске реакция взаимодействия кислоты со спиртом? обладает полученный эфир? эфир. | Записывают уравнения реакции, отвечают на вопросы. | ||
| IV. ПЕРВИЧНАЯ ПРОВЕРКА УСВОЕНИЯ ЗНАНИЙ. ПЕРВИЧНОЕ ЗАКРЕПЛЕНИЕ ЗНАНИЙ. КОНТРОЛЬ И САМОПРОВЕРКА ЗНАНИЙ | ||||
| Слайд №15-21 (5 мин.) | Кластер «Химические свойства одноосновных, предельных карбоновых кислот (Приложение №3) желтый лист | Создание кластера | ||
| Слайд №22-23 Тестирование и самопроверка 1. б; 2. б; 3. г; 4. а (3 мин.) | Рефлексия содержания учебного материала Зеленый лист | Выполняют тест и проводят самопроверку | ||
| V. ПОДВЕДЕНИЕ ИТОГОВ УРОКА. РЕФЛЕКСИЯ | ||||
| Слайд №25 Заверши фразу: (1 мин.) | Итоговая рефлексия | Завершают предложения | ||
| VI. ДОМАШНЕЕ ЗАДАНИЕ | ||||
Информация по теме «Химические свойства карбоновых кислот»
Внимательно читая текст, отмечай значками на полях (справа или слева), насколько новая и понятная для тебя информация:
«+» — уже знал; «−» — новое; «!» — думал иначе; «?» — не понял, есть вопросы
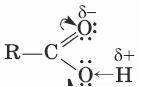
Многие химические свойства кислот объясняет электронно-структурная формула:
- Карбоновые кислоты — более сильные, чем спирты, поскольку атом водорода в
карбоксильной группе (СООН) обладает повышенной подвижностью благодаря влиянию группы (СО). В водном растворе карбоновые кислоты диссоциируют: RCOOH↔ RCOO — + Н +
Но из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты — это, как правило, слабые кислоты.
- Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот.
Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
RCOOH + NaOH → RCOONa + Н2О
- Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода:
RCH2− COOH + Br2 → RCHBr − COOH + HBr
- В атмосфере кислорода карбоновые кислоты окисляются до СО2 и Н2О
5.Образование сложных эфиров. Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
- а) В присутствии водоотнимающих средств (H2SO4(конц.)) муравьиная кислота отщепляет воду с выделением оксида углерода (II). б) Из-за наличия в молекуле НСООН альдегидного протона муравьиная кислота легко окисляется, дает реакцию «серебряного зеркала» и «медного зеркала».
Инструкция для проведения лабораторного опыта
«Взаимодействие карбоновых кислот со спиртами»
Оборудование и реактивы: штатив с пробирками, спиртовка, держатель для пробирок, спички, уксусная кислота – СН3СООН, этиловый спирт – С2Н5ОН, серная кислота – Н2SO4 (катализатор), стакан с водой.
Будьте аккуратны, соблюдайте правила ТБ.
- Налейте в пробирку уксусную кислоту (уровень жидкости приблизительно 1-1,5 см)
- Добавьте к уксусной кислоте этиловый спирт (уровень жидкости доведите до 2,5 -3см).
- Отметьте, что происходит? Ощущается ли запах эфира?
- Если реакция не идет, добавьте в пробирку с реагентами катализатор (концентрированный раствор серной кислоты 4-5 капель) нагрейте пробирку с реагентами.
- Вылейте содержимое пробирки в стакан с водой, зафиксируйте запах полученного эфира (сладковато-резковатый, напоминающий запах ацетона).
- Составьте уравнение реакции взаимодействия уксусной кислоты и этилового спирта (реакция этерификации).
- Наведите порядок на рабочем месте.
Задание для группы №1
- I. Выберите (из данного перечня 1-10) уравнения химических реакций, характеризующие общие свойства карбоновых кислот, что их сближает со всеми кислотами (неорганическими и органическими)
- II. Составьте кластер (графическая форма организации информации)
Задание для группы №2
- I. Выберите (из данного перечня 1-10) уравнения химических реакций, характеризующие общие свойства карбоновых кислот, что их сближает только с органическими кислотами
- II. Составьте кластер (графическая форма организации информации)
Задание для группы №3
- I. Выберите (из данного перечня 1-10) уравнения химических реакций, характеризующие индивидуальные свойства муравьиной кислоты, что её отличает от других карбоновых кислот
- II. Составьте кластер (графическая форма организации информации)
- При взаимодействии муравьиной кислоты с магнием образуются:
а) формиат магния и вода;
б) формиат магния и водород;
в) ацетат магния и вода;
г) ацетат магния и водород
- С уксусной кислотой не взаимодействует:
- По углеводородному радикалу проходит реакция, уравнение которой:
- 4. Уксусная кислота может реагировать с каждым из двух веществ:
http://buzani.ru/raznoe/testy/1104-testy-po-khimii-11-klass-ege-chast-1-variant-3
http://chemistryteacher.com.ru/strigina-4.html