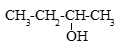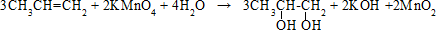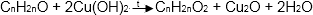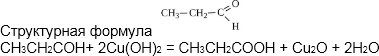Уравнение реакций. химия 10 класс Рудзитис вопрос 14 параграф 21
Доброго вечера. Помогите с решением, сам никак не соображу(( Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
СН4-СН3-СН3-СН3-СН2-ОН-СН3-СН3
СН3-СН2-ОН-СН2=СН2-СН3-СН3-СН3-СН2-CI-СН3-С =0-Н
СН3-СН2-ОН-СН2=СН-СН=СН2
СаСО3-СаС2-С2Н2-СН3-СН2-ОН-СН3-СН2-CI-СН2=СН2
Должно быть так)
а
1) СН4 + Cl2 → СН3С1 + НС1
2CH3Cl + 2Na → СН3—СН3 + 2NaCl
2) СН3—СН3 + С12 → СН3—СН2—Cl + HCl
СН3— СН2—Cl + H2O → СН3—СН2—ОН + НС1
3) CH3—CH2—OH → CH2=CH2 + H2O
CH2=CH2 + H2 → CH3—CH3
б
1) CH3—CH2—OH → CH2=CH2 + H2O
2) СН2=СН2 + H2 → CH3—CH3
3) CH3—CH3+ С12 → СН3—СН2—Cl + НС1
4) СН3—СН2—С1 + H2O → СН3—СН2—ОН + НС1
в
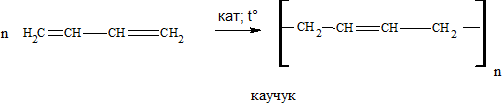
CH3—CH2—OH → CH2=CH—CH=CH2
2СН3—CH2—ОН → СН2=СН—СН=СН2 + 2Н2O + Н2↑
1) CaCO3 → CaO + CO2
CaO + 3C → CaC2 + CO
2) CaC2 + 2H2O → C2H2 + Ca(OH)2
3) CH=CH + H2 → ch2=ch2
CH2=CH2 + H2O → CH3—CH2—OH
4) CH3—CH2—OH + HC1 → CH3—CH2—Cl + H2O
5) CH3—CH2—Cl → CH2=CH2 + HC1
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. 35. Установление молекулярной и структурной формулы веществаФормат ответа: цифра или несколько цифр, слово или несколько слов. Вопросы на соответствие «буква» — «цифра» должны записываться как несколько цифр. Между словами и цифрами не должно быть пробелов или других знаков. Примеры ответов: 7 или здесьисейчас или 3514 Установление молекулярной и структурной формулы вещества При взаимодействии органического вещества массой 14,8 г с металлическим натрием собрали 2,24 л (н.у.) водорода. В ходе исследования химических свойств этого вещества установлено, что при его взаимодействии с оксидом меди (II) образуется кетон. На основании данных условия задания 1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества; 2) установите молекулярную формулу исходного органического вещества; 3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции этого вещества с оксидом меди (II). Кетоны образуются при окислении оксидом меди (II) вторичных спиртов, следовательно, неизвестное вещество – вторичный спирт. Общая формула вещества CxHyOH 1) Составляем уравнение реакции в общем виде и находим количество вещества водорода: 2) Находим молекулярную формулу спирта: по уравнению реакции: вычисляем: х = 4 и у = 9 молекулярная формула спирта C4H9OH 3) Составляем структурную формулу вещества: 4) Уравнение реакции вещества с оксидом меди (II): Установите молекулярную формулу диена, относительная плотность паров которого по воздуху 1,862. Установите структурную формулу вещества, если оно известно как синтетический каучук. Запишите реакцию полимеризации CnH2n-2 – общая формула диенов M (CnH2n-2) = D возд (CnH2n-2) * M (возд) = 1,862 * 29 = 54 г/моль Некоторая предельная одноосновная карбоновая кислота массой 6 г требует для полной этерификации такой же массы спирта. При этом получается 10,2 г сложного эфира. Установите молекулярную формулу этой карбоновой кислоты. Запишите реакцию этой кислоты со спиртом. Если известно, что спирт в реакции с оксидом меди даёт кетон. 1) Уравнение реакции этерификации в общем виде: 2) Масса и количество вещества воды: m(H2O) = (6 + 6) – 10,2 = 1,8 г n(H2O) = 1,8 / 18 = 0,1 моль 3) Формула кислоты: по уравнению реакции n(CnH2n+1COOH) = m / n = 6 / 0,1 = 60 г/моль 12n + 2n + 1 + 12 + 16 ∙ 2 + 1 = 60 Формула кислоты – CH3COOH 4) 4) Так как спирт и кислота имеют одинаковую массу и реагируют в одинаковом соотношении, то исходный спирт – пропанол-1 $\rm CH_3COOH + CH_3CH_2CH_2OH \overset В результате окисления 23 г предельного одноатомного спирта оксидом меди (II) получены продукты реакции общей массой 63 г. Определите молекулярную формулу исходного спирта. Запишите реакцию одновременной дегидратации и дегидрирования в присутствии катализаторов и температуры 400°С 1) Уравнение реакции и количество вещества CuO: По закону сохранения массы n(CuO) = 40 / 80 = 0,5 моль 2 ) Рассчитываем молярную массу спирта: по уравнению реакции n(спирта) = n(CuO) = 0,5 моль М(спирта) = 23 / 0,5 = 46 г/моль 3) Определяем формулу спирта: М(CnH2n+1CH2OH) = 12n + 2n + 1 + 12 + 2 + 16 + 1 = (14n + 32) г/моль 4 )В таких условиях протекает реакция Лебедева с образованием бутадиена-1,3 Определите молекулярную формулу алкена, если известно, что одно и то же количество его, взаимодействуя с различными галогенами, образует соответственно или 5,23 г хлорпроизводного, или 8,2 г бромпроизводного. Запишите реакцию взаимодействия данного алкена с водным раствором перманганата калия при 0°С 1) Уравнения реакций и соотношение реагирующих веществ: 2) Рассчитываем количество вещества хлор- и бромпроизводных: n(CnH2n+1Cl) = 5,23 / (12n + 2n + 1 + 35,5) = 5,23 / (14n + 36,5) моль n(CnH2n+1Br) = 8,2 / (12n + 2n + 1 + 80) = 8,2 / (14n + 81) моль 3) Находим индекс «n» и формулу алкена: 5,23 / (14n + 36,5) = 8,2 / (14n + 81) При взаимодействии органического вещества массой 14,8 г с металлическим натрием собрали 2,24 л (н. у.) водорода. В ходе исследования химических свойств этого вещества установлено, что при его взаимодействии с оксидом меди(II) образуется кетон. 1. установите простейшую молекулярную формулу соединения, 2. составьте его структурную формулу, 3. приведите уравнение реакции этого вещества с оксидом меди (II) Содержание ответа Баллы Общая формула вещества: CxHyOH 1) Составляем урвнение реакции в общем виде и находим количество водорода 2) Находим молекулярную формулу спирта по уравнению рекции: Вычисляем х=4 и у=9 Молекулярная формула спирта: С4Н9ОН Ответ правильный и полный, содержит следующие элементы:
|