Политропный процесс | 20+ важных часто задаваемых вопросов и числовых значений
Content
Политропный процесс
Определение политропный процесс
Политропное уравнение | Политропное уравнение состояния
Политропный процесс можно определить уравнением
показатель степени n называется индексом политропы. Он зависит от материала и варьируется от 1.0 до 1.4. Это метод постоянной удельной теплоемкости, при котором учитывается поглощение тепла газом из-за повышения температуры на единицу.
Политропный индекс
- п nd закон термодинамики. Эти частные случаи используются в тепловом взаимодействии для астрофизики и химической энергии.
- п = 0: Р = С: Представляет собой изобарический процесс или процесс постоянного давления.
- n = 1: PV = C: Согласно предположению об идеальном газовом законе, PV = C представляет постоянную температуру или изотермический процесс.
- 1 0). Как и в циклах сжатия пара, тепло теряется в горячее окружение.
- п = γ: В предположении закона идеального газа, представляет собой постоянную энтропию, изэнтропический процесс или обратимый адиабатический процесс.
- γ
Некоторые важные соотношения между давлением [P], объемом [V] и температурой [T] в политропном процессе для идеального газа
………………………. Соотношение между давлением [P] и объемом [V]
………………………. Связь между объемом [В] и температурой [Т]
………………………. Связь между давлением [P] и температурой [T]
Политропные работы
Уравнение идеального газа для политропного процесса дается формулой
Политропная теплопередача
По данным 1 st закон термодинамики,
Политропный против изэнтропического процесса
Политропный процесс — это термодинамический процесс, который подчиняется уравнению
Этот процесс учитывает потери на трение и фактор необратимости процесса. Это реальный процесс, за которым следует газ в определенных условиях.
Изэнтропический процесс, также известный как обратимый адиабатический процесс, представляет собой идеальный процесс, в котором не происходит передача энергии или тепла через границы системы. В этом процессе предполагается, что система имеет изолированную границу. Т.к. теплопередача равна нулю. дQ = 0
Согласно первому закону термодинамики,
Политропный процесс против адиабатического процесса
Политропный процесс — это термодинамический процесс, который подчиняется уравнению
Этот процесс учитывает потери на трение и фактор необратимости процесса. Это реальный процесс, за которым следует газ в определенных условиях.
Адиабатический процесс — это особое и специфическое состояние политропного процесса, при котором.
Подобно изэнтропическому процессу, в этом процессе также не происходит передачи энергии или тепла через границы системы. В этом процессе предполагается, что система имеет изолированную границу.
Политропная эффективность
«Политропический КПД, точно определяемый как отношение идеальной работы сжатия для изменения перепада давления в многоступенчатом компрессоре к фактической работе сжатия при изменении перепада давления в многоступенчатом компрессоре».
Проще говоря, это изоэнтропическая эффективность процесса для бесконечно малой ступени многоступенчатого компрессора.
Где, γ = индекс адиабаты
Pd = Давление нагнетания
Ps = Давление всасывания
Td = Температура подачи
Ts = Температура всасывания
Политропная голова
Политропный напор можно определить как напор, создаваемый центробежным компрессором при политропном сжатии газа или воздуха. Величина развиваемого давления зависит от плотности сжатого газа, и это зависит от изменения плотности газа.
γ = индекс адиабаты
zсредний = Средний коэффициент сжимаемости
η = политропная эффективность
Pd = Давление нагнетания
Ps = Давление всасывания
S = удельный вес газа
Ts = Температура всасывания
Политропный процесс для воздуха | Политропный процесс для идеального газа
Считается, что воздух является идеальным газом, и поэтому законы идеального газа применимы к воздуху.
………………………. Соотношение между давлением [P] и объемом [V]
………………………. Связь между объемом [В] и температурой [Т]
………………………. Связь между давлением [P] и температурой [T]
Примеры политропных процессов
1. Рассмотрим политропный процесс с индексом политропы. п = (1.1). Начальные условия: P1 = 0, В1 = 0 и заканчивается на P2= 600 кПа, В2 = 0.01 м 3 . Оцените проделанную работу и теплоотдачу.
Ответ: Работы, выполненные политропным процессом, предоставлены
Теплопередача определяется выражением
2. Поршневой цилиндр содержит кислород при 200 кПа объемом 0.1 м. 3 и при 200 ° С. Масса добавляется так, чтобы газ сжимался с PV. 1.2 = постоянная до конечной температуры 400 ° C. Подсчитайте проделанную работу.
Ответ: Выполненная политропная работа определяется
3. Рассмотрим аргон при 600 кПа, 30 ° C, сжатый до 90 ° C в политропном процессе с n = 1.33. Найдите проделанную работу на Газе.
Ответ: Выполненная политропная работа определяется
для аргона при 30 ° C составляет 208.1 Дж / кг. K
Принимая m = 1 кг
4. Предположим, что масса 10 кг ксенона хранится в баллоне при 500 К, 2 МПа, расширение представляет собой политропный процесс (n = 1.28) с конечным давлением 100 кПа. Посчитайте проделанную работу. Учтите, что система имеет постоянную удельную теплоемкость.
Ответ: Выполненная политропная работа определяется
для ксенона при 30 ° C — 63.33 Дж / кг. K
Принимая m = 10 кг
5. Рассмотрим цилиндр-поршень с начальным объемом 0.3, содержащий 5 кг газообразного метана при давлении 200 кПа. Газ сжимают политропно (n = 1.32) до давления 1 МПа и объема 0.005. Рассчитайте теплопередачу во время процесса.
Ответ: Политропная теплопередача определяется
6. Примите во внимание цилиндр-поршень, содержащий 1 кг метана при 500 кПа, 20 ° C. Газ политропно сжимают до давления 800 кПа. Рассчитайте теплопередачу с показателем n = 1.15.
Ответ: Политропная теплопередача определяется
Мы знаем, что R для метана = 518.2 Дж / кг. K
7. 1 кг гелия хранится в системе поршень-цилиндр при 303 К, 200 кПа сжимается до 400 К в обратимом политропном процессе с показателем степени n = 1.24. Гелий является идеальным газом, поэтому удельная теплоемкость будет фиксированной. Найдите работу и теплопередачу.
Ответ: Выполненная политропная работа определяется
R для гелия составляет 2077.1 Дж / кг.
Политропная теплопередача определяется выражением
8. Предположите, что воздух хранится в баллоне объемом 0.3 литра при 3 МПа, 2000 К. Воздух расширяется в соответствии с обратимым политропным процессом с показателем степени n = 1.7, объемное соотношение в этом случае составляет 8: 1. Рассчитайте политропную работу для процесса и сравните ее с адиабатической работой, если процесс расширения следует за обратимым адиабатическим расширением.
Ответ: Нам дается
Соотношение между давлением [P] и объемом [V]
Выполненная политропная работа определяется выражением
Проделанная адиабатическая работа определяется выражением
Для процесса расширения Работа, выполняемая посредством обратимого адиабатического процесса, больше, чем Работа, выполняемая посредством обратимого политропного процесса.
9. В закрытом контейнере содержится 200 л газа при 35 ° C, 120 кПа. Газ сжимается в политропном процессе до температуры 200 ° C, 800 кПа. Найти политропную работу, совершаемую воздухом для n = 1.29.
Ответ: соотношение между давлением [P] и объемом [V]
Выполненная политропная работа определяется выражением
10. Масса 12 кг газообразного метана при 150 ° C, 700 кПа подвергается политропному расширению с n = 1.1 до конечной температуры 30 ° C. Найти теплопередачу?
Ответ: Мы знаем, что R для метана = 518.2 Дж / кг. K
Политропная теплопередача определяется выражением
11. Узел цилиндр-поршень содержит R-134a при 10 ° C; объем 5 литров. Охлаждающая жидкость сжимается до 100 ° C, 3 МПа в соответствии с обратимым политропным процессом. рассчитать проделанную работу и теплоотдачу?
Ответ: Мы знаем, что R для R-134a = 81.49 Дж / кг. K
Выполненная политропная работа определяется выражением
Политропная теплопередача определяется выражением
12. Является ли политропный процесс изотермическим по своей природе?
Ответ: Когда n становится 1 для политропного процесса: согласно предположению об идеальном газовом законе, PV = C представляет постоянную температуру или изотермический процесс.
13. Обратим ли политропный процесс?
Ответ: политропные процессы внутренне обратимы. Вот несколько примеров:
п = 0: Р = С: Представляет собой изобарический процесс или процесс постоянного давления.
n = 1: PV = C: Согласно предположению об идеальном газовом законе, PV γ = C представляет собой постоянную температуру или изотермический процесс.
п = γ: В предположении закона идеального газа, представляет собой постоянную энтропию, изэнтропический процесс или обратимый адиабатический процесс.
n = Бесконечность: Представляет собой изохорный процесс или процесс постоянного объема.
14. Адиабатический политропный процесс?
Ответ: когда п = γ: В предположении закона идеального газа PV γ = C, представляет постоянную энтропию или изэнтропический процесс или обратимый адиабатический процесс.
14. Что такое политропная эффективность?
Ответ: Политропический КПД можно определить как отношение идеальной работы сжатия к фактической работе сжатия при изменении перепада давления в многоступенчатом компрессоре. Проще говоря, это изоэнтропическая эффективность процесса для бесконечно малой ступени многоступенчатого компрессора.
Проще говоря, это изоэнтропическая эффективность процесса для бесконечно малой ступени многоступенчатого компрессора.
Где, γ = индекс адиабаты
Pd = Давление нагнетания
Ps = Давление всасывания
Td = Температура подачи
Ts = Температура всасывания
15. Что такое гамма в политропном процессе?
Ответ: В политропном процессе, когда п = γ: В предположении закона идеального газа PV γ = C, представляет постоянную энтропию или изэнтропический процесс или обратимый адиабатический процесс.
16. что такое политропный процесс?
Ответ: Политропный процесс можно определить уравнением
показатель степени n называется индексом политропы. Он зависит от материала и варьируется от 1.0 до 1.4. Его также называют процессом с постоянной удельной теплотой, при котором тепло, поглощаемое газом, учитываемое из-за повышения температуры на единицу, является постоянным.
17. Какие выводы можно сделать для политропного процесса с n = 1?
Ответ: когда п = 1: PV n = C : Согласно предположению об идеальном газе, закон становится PV = C представляет собой постоянную температуру или изотермический процесс.
18. Что такое неполитропный процесс?
Ответ: Политропный процесс можно определить уравнением PV n = C показатель степени n называется индексом политропы. Когда,
- п 0). Как и в циклах сжатия пара, тепло теряется в горячее окружение.
- п = γ: В предположении закона идеального газа PV γ = C представляет постоянную энтропию или изэнтропический процесс или обратимый адиабатический процесс.
- γn0). Как и в циклах сжатия пара, тепло теряется в горячее окружение. Изменение температуры происходит из-за изменения внутренней энергии, а не подводимого тепла. Произведенная работа превышает количество поданного или добавленного тепла. Таким образом, даже если при политропном расширении добавляется тепло, температура газа снижается.
21. В политропном процессе, когда PV n = константа, температура тоже постоянна?
Ответ: В политропном процессе, когда PV n = постоянная, температура остается постоянной только при показателе политропы n = 1. Для n = 1: PV = C: Согласно предположению об идеальном газовом законе, PV = C представляет постоянную температуру или изотермический процесс.
Политропный процесс: характеристики, применения и примеры
Политропный процесс: характеристики, применения и примеры — Наука
Содержание:
А политропный процесс это термодинамический процесс, который происходит, когда связь между давлением п и объем V данныйП.В. п он остается постоянным. Показатель п является действительным числом, обычно от нуля до бесконечности, но в некоторых случаях может быть отрицательным.
Значение п получает имя индекс политропии и важно подчеркнуть, что во время политропного термодинамического процесса указанный индекс должен поддерживать фиксированное значение, иначе процесс не будет считаться политропным.
Характеристики политропных процессов
Некоторые характерные случаи политропных процессов:
— Изотермический процесс (при постоянной температуре T), в котором показатель степени равен n = 1.
— Изобарический процесс (при постоянном давлении P), в этом случае n = 0.
— Изохорный процесс (при постоянном объеме V), для которого n = + ∞.
— Адиабатические процессы (при постоянной энтропии S), в которых показатель степени равен n = γ, где γ — адиабатическая постоянная. Эта постоянная представляет собой отношение теплоемкости при постоянном давлении Cp к теплоемкости при постоянном объеме Cv:
— Любой другой термодинамический процесс, не входящий в один из предыдущих случаев. но это соответствует П.В. п = ctte с действительным и постоянным индексом политропы п это тоже будет политропный процесс.
Приложения
Одним из основных приложений уравнения политропы является вычисление работы, совершаемой замкнутой термодинамической системой, когда она переходит из начального состояния в конечное квазистатическим образом, то есть следуя последовательности состояний равновесия.
Работа над политропными процессами для разных значений n
Для n 1
Механическая работа W, совершаемая замкнутой термодинамической системой, рассчитывается по выражению:
Где P — давление, а V — объем.
Как и в случае политропного процесса, соотношение между давлением и объемом:
Решение для P из предыдущего выражения, чтобы заменить его в рабочем выражении:
У нас есть механическая работа, совершаемая во время политропного процесса, который начинается в начальном состоянии 1 и заканчивается в конечном состоянии 2. Все это выражается в следующем выражении:
Подставляя значение константы в рабочее выражение, получаем:
В случае, если рабочее тело можно смоделировать как идеальный газ, мы имеем следующее уравнение состояния:
Где m — количество молей идеального газа, а R — универсальная газовая постоянная.
Для идеального газа, который следует политропному процессу с показателем политропии, отличным от единицы, и который переходит из состояния с начальной температурой T1 в другое состояние с температурой T2 у нас есть, что проделанная работа рассчитывается по следующей формуле:
При n → ∞
Согласно формуле для работы, полученной в предыдущем разделе, работа политропного процесса с n = ∞ равна нулю, потому что выражение работы делится на бесконечность и, следовательно, результат стремится к нулю. .
Другой способ получить этот результат — использовать соотношение P1 V1 п = P2 V2 п , который можно переписать следующим образом:
Взяв корень n-й степени в каждом члене, получим:
В случае n → ∞ имеем (V2/ V1) = 1, что означает, что:
То есть объем не изменяется в политропном процессе при n → ∞. Следовательно, перепад объема dV в интеграле механической работы равен 0. Эти типы политропных процессов также известны как процессы изохорный, или процессы с постоянным объемом.
Для n = 1
Снова у нас есть выражение для работы:
В случае политропного процесса с n = 1 соотношение между давлением и объемом:
P V = константа = C
Решив P из предыдущего выражения и сделав замену, мы проделали работу по переходу от начального состояния 1 к конечному состоянию 2:
Поскольку начальное и конечное состояния хорошо определены, то и ctte. То есть:
Наконец, у нас есть следующие полезные выражения для нахождения механической работы замкнутой политропной системы, в которой n = 1.
Если рабочее вещество состоит из м моль идеального газа, то можно применить уравнение состояния идеального газа: P V = m.R.T.
В этом случае, как отмечает П.В.1 = ctte, имеем, что политропный процесс с n = 1 — это процесс при постоянной температуре T (изотермический), так что можно получить следующие выражения для работы:
Примеры политропных процессов
— Пример 1
Представьте цилиндр с подвижным поршнем, наполненный одним килограммом воздуха. Изначально воздух занимает объем V1= 0,2 м 3 при давлении P1= 400 кПа. За политропным процессом следует n = γ = 1,4, конечное состояние которого имеет давление P2 = 100 кПа. Определите работу, проделанную воздухом над поршнем.
Решение
Когда индекс политропии равен адиабатической постоянной, происходит процесс, в котором рабочее вещество (воздух) не обменивается теплом с окружающей средой, и, следовательно, энтропия не изменяется.
Для воздуха, двухатомного идеального газа, мы имеем:
γ = Cp / Cv, где Cp = (7/2) R и Cv = (5/2) R
Используя выражение политропного процесса, можно определить конечный объем воздуха:
Теперь у нас есть условия для применения формулы работы, проделанной в политропном процессе для n 1, полученной выше:
Подставляя соответствующие значения, получаем:
W = (100 кПа 0,54 м 3 — 400 кПа 0,2 м 3 ) / (1 — 1,4) = 65,4 кДж
— Пример 2
Предположим, что в примере 1 такой же цилиндр с подвижным поршнем, заполненным одним килограммом воздуха. Изначально воздух занимает объем V1 = 0,2 м. 3 при давлении P1 = 400 кПа. Но в отличие от предыдущего случая воздух изотермически расширяется до конечного давления P2 = 100 кПа. Определите работу, проделанную воздухом над поршнем.
Решение
Как видно выше, изотермические процессы являются политропными процессами с индексом n = 1, поэтому верно, что:
Таким образом можно легко отделить окончательный объем и получить:
Тогда, используя выражение работы, полученное ранее для случая n = 1, мы получаем, что работа, совершаемая воздухом над поршнем в этом процессе, равна:
W = P1 V1 ln (V2 / V1) = 400000 Па × 0,2 м 3 ln (0,8 / 0,2) = 110,9 кДж.
Ссылки
- Бауэр, В. 2011. Физика для инженерии и науки. Том 1. Мак Гроу Хилл.
- Ценгель, Ю. 2012. Термодинамика. 7-е издание. Макгроу Хилл.
- Фигероа, Д. (2005). Серия: Физика для науки и техники. Том 4. Жидкости и термодинамика. Отредактировал Дуглас Фигероа (USB).
- Лопес, К. Первый закон термодинамики. Получено с: culturacientifica.com.
- Найт, р. 2017. Физика для ученых и инженерии: стратегический подход. Пирсон.
- Serway, R., Vulle, C. 2011. Основы физики. 9-е изд. Cengage Learning.
- Севильский университет. Тепловые машины. Получено с: laplace.us.es.
- Википедия. Политропный процесс. Получено с: wikiwand.com.
Как мотивировать команду на работе: 8 советов
Кто однажды изменил, будет неверным всегда?
Политропный процесс
Политропный процесс
- Обычно фактический процесс работы теплового двигателя происходит при наличии теплообмена, р, в, Т изменений. То есть он не является теплоизолирующим, изобарическим, изобарическим или изотермическим. Для расчета такого процесса соотношение между давлением и объемом обычно выражается уравнениями вида ФВ plvlj p1v Конст. 5. 37. Процесс в соответствии с этим уравнением называется. Политолог. Показатель степени уравнения p НИИ называется политропным indicator. В некоторых процессах величина n постоянна, но в разных процессах политропный показатель может принимать любое число.
Для идеального газа по уравнению pv-rt можно найти уравнение политропного процесса, соединив параметры t, t и t, p. Для этого нужно заменить давление или объем в уравнении 5. 37 соответственно и выразить их с помощью уравнения Клапейрона. После преобразования получены следующие уравнения политропного процесса tv — — t — t2v — const 5. 38 5. 39 ТП т п t2p2. Уравнение 5. 37 5. 38 5. 39 поэтому связь между параметрами в начале и конце политропного процесса может быть легко получена. −1 5.
Поскольку уравнение (16-7) должно быть справедливо также и для воздуха, то одновременно с потоком частиц пара должен существовать и поток частиц воздуха, но в обратном направлении. Людмила Фирмаль
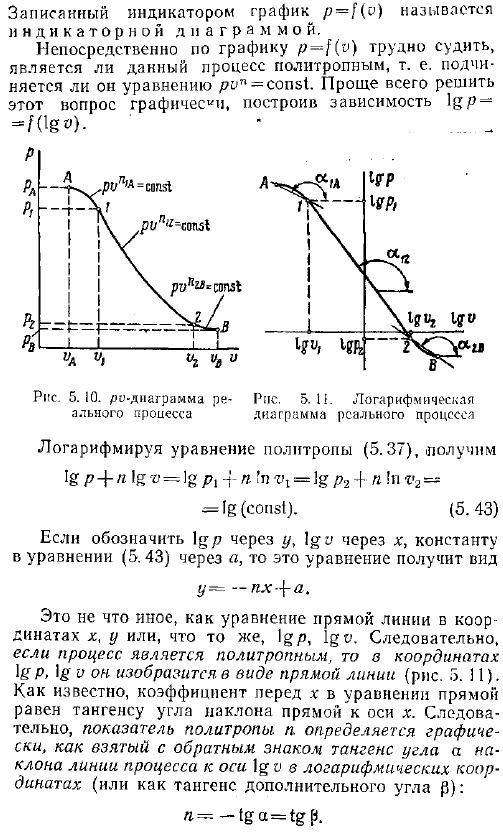
Сорок два. При изучении фактического процесса необходимо установить, является ли процесс политропой, и определить значение индекса политропы. Обычно при изучении работы тепловых машин двигателей, компрессоров и др. , давление и объем рабочей жидкости измеряются в процессе расширения и сжатия. По результатам таких измерений можно построить зависимость p f v рис. 5. 10.
При исследовании работы поршневой машины двигателя внутреннего сгорания, компрессора и др. , такой график рисуют приборы так называемые индикаторы, которые автоматически измеряют изменения давления и объема. Графика р о описывается индикатор называется индикаторной диаграммы. Из графика p-f v трудно непосредственно определить, является ли этот процесс политропой, то есть следует уравнению pon const. Проще всего решить эту проблему графически, построив зависимость lg fog —. — Логарифм уравнения политропа 5. 37, ig p 4-n log-o g pi-i- to r 1 ig p2 4-n in v2— ИГ константа. 5. 43 Если igp обозначается через y, а igo-через x, а константа уравнения 5.
Через a, то это уравнение принимает вид В j -зл-Н. Это то же самое, что и линейные уравнения координат x, y или igp, lgv. So, если процесс представляет собой политропу, то она рисуется в виде прямой линии, с координатами igp, ig рис. 5. 11. Как известно, коэффициент x в уравнении прямой линии равен касательной наклона линии к оси x-axis. As в результате политропный индекс n определяется как тангенс угла a от противоположного знака в логарифмических координатах и как наклон технологической линии к оси МПО или как тангенс дополнительного угла Как будет определено. Обратите внимание, что не все процессы являются политропами.
Например, вы можете видеть, что только процесс at 5. 11, раздел 1-2 процесса at2b, можно считать политропой с равными показателями. Л12 — tga12. Если в координатах лгп фактический процесс МПО не представлен прямой линией, то он разбивается на короткие отрезки, в которых линия практически заменяется прямой segment. In примерный рисунок, раздел 5. 11, al n 2b, также можно считать политропой с индексами n, равными n a — tg u1a и 2b — tg g2b. — Если известно, что процесс является политропным, то значение показателя n можно определить по формуле 2 из значения параметра газа в любой точке этого процесса 5. 43.
Выражает давление по объему из Формулы 3. 2, формулы 5. 37. Эта формула такая же по форме, как и соответствующая формула для процесса термоизоляции, отличающаяся только обозначением индекса теплопроводности. Volume. So, в результате интегрирования вы получите формулу, аналогичную форме 5. Сорок семь Из уравнения состояния pioi этих выражений можно заменить на rt. Выполнив такую замену в выражении 5.
- Мы получим другое выражение, для которого работает политропный процесс. 4 — Г2. 5. 48. Теплотворная способность политропного процесса определяется по следующей формуле 5. 49 Вот, Джей Кг-град — это теплоемкость газа в политропном процессе, то есть процессе, в котором n является постоянной величиной. Теплоемкость газа политропного процесса определяется по общей формуле 4. 3. Для этого необходимо подставить отношение изменения объема к изменению температуры в политропном процессе. Эта зависимость получается путем дифференцирования уравнения 5. 41 политропного процесса переменной Г, о. После логарифма формулы 5.
Отсюда л-т л-1. Подставляя это выражение в выражение 4. 3, вы получаете Если привести их к общему знаменателю с круглыми скобками, то получится формула для теплоемкости газа в политропном процессе. Из этой формулы видно, что было решено учитывать удельную теплоту независимо от температуры удельная теплота идеального газа в политропном процессе будет постоянной. В отличие от теплоемкости cp и c, теплоемкость газа в политропном процессе может быть отрицательной. Это тот случай, когда значение индекса политропа n больше 1 и меньше k, то есть k n.
Так как массосодержание водяного пара иц и воздуха составляют в сумме единицу, градиент массосодержания пара соответствует градиенту маососодержания воздуха. Людмила Фирмаль
Отрицательная теплоемкость означает, что, несмотря на подвод тепла к газу, температура снижается, а при отводе тепла, наоборот, он становится горячим. Это, казалось бы, аномальное поведение температуры объясняется тем, что политропный процесс 1 l, а следовательно, cn 0, получается сильным расширением с небольшим запасом heat. In кроме того, это ln qn, и изменение внутренней энергии отрицательно. Л Несмотря на то, что тепло подается 1 0, когда внутренняя энергия газа уменьшается, температура уменьшается.
В процессе сжатия, если из рабочего тела удаляется меньше тепла, чем выполняется работа, то есть и В случае n избыточная энергия — qn увеличивает внутреннюю энергию газа, и температура повышается. Тепло удаляется н 0. Подставляя давление, выраженное в объеме по уравнению 3. 14 5. 37, показано, что работа газа, имеющаяся в политропном процессе, в n раз больше работы расширения в этом процессе, как это было сделано в адиабатическом процессе 5. 51 Рассмотренные ранее процессы изометрический, изобарный, изотермический, адиабатический-это частный случай политропного процесса. Каждое уравнение может быть представлено в виде swarm const со своим значением индикатора.
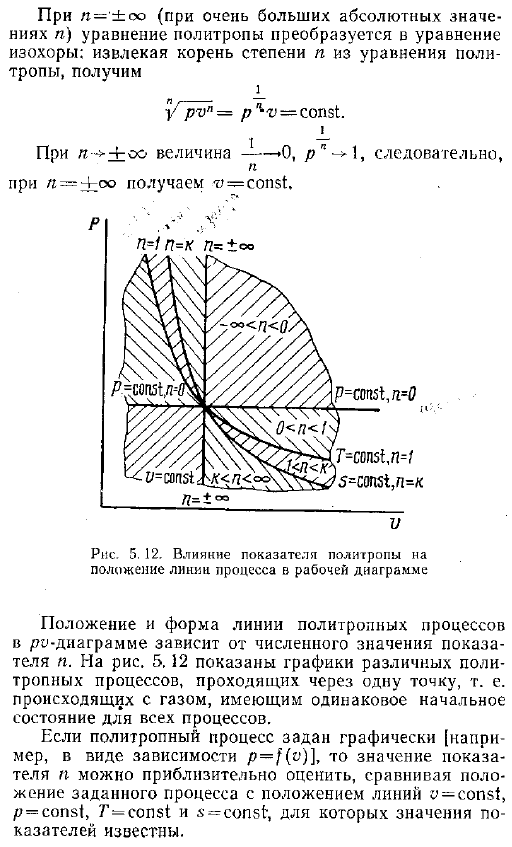
Фактически, в n-0 уравнение политропа принимает следующий вид pr 0 p-1 const или p const изобарный процесс. Если l 1, то политропное уравнение представляет собой изотермический процесс. Рv const и если l a, то политропы соответствуют адиабату. Роль const. В случае n- co где абсолютное значение n очень велико политропное уравнение преобразуется в однородное уравнение. Извлечение корней Порядка n из политропного уравнения дает ПВН Р v пост. Для n — oo значение равно −0 например — — — Лоо, вы получите.
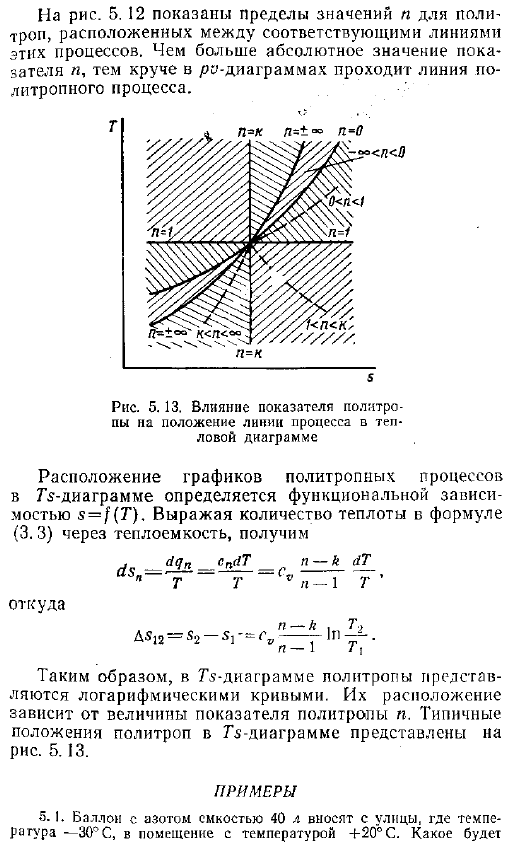
Процесс работы диаграммы расположение и форма линии RO-диаграммы политропного процесса зависит от порядкового номера изделия .На рисунке 5 .12 показан график различных политропных процессов, проходящих через 1 точку .То есть все процессы протекают в одном и том же начальном состоянии газа .Если политропный процесс задан графически например, в виде зависимости p f o, то значение показателя N аппроксимируется путем сравнения положения данного процесса с положениями линий y const, p const, T const и s const .Значение индикатора известно .На рисунке 5 .12 показано ограничение на значение N в политропы между соответствующими линиями этих процессов .Чем выше абсолютное значение показателя, тем круче линия политропного процесса .Рис .
Влияние индекса политропа на расположение технологической линии на диаграмме горячей проволоки Положение графика политропного процесса на диаграмме G определяется зависимостью функции s T .Если величина теплоты уравнения 3 .3 выражается в терминах удельной теплоты, то она выглядит следующим образом Откуда AS12 С2-с — сі, — г п г — Таким образом, в схеме ТС, политроп представлены логарифмические кривые .Их расположение зависит от величины политропного показателя n .на рисунке показано типичное положение политроп на диаграмме G .5 .13 .Пример 5 .1 .Возьмите баллон с емкостью 40 литров азота с улицы, где температура составляет −3 C, в помещение с температурой 20 C .Давление в баке и температура азота равны давлению в баке 98 dir Тепло, и равное cv 742 Дж Кг-град .Решение .О нагревании шара .- Меняйся, Трейс .— 297 Дж кг град- 2 .7 найти 9810S-0 .04 М ря, 7а-Д 5 .45-742 .10-1 293-243 −202 кДж .




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
http://ru1.warbletoncouncil.org/proceso-politropico-1779
http://lfirmal.com/politropnyj-process/