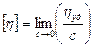«В.Н. Вережников ИЗБРАННЫЕ ГЛАВЫ КОЛЛОИДНОЙ ХИМИИ Учебное пособие для вузов Издательско-полиграфический центр Воронежского . »
Интегрированием уравнения Ньютона может быть получено уравнение, описывающее истечение жидкости через цилиндрические капилляры:
Pr 4 Q= t, (6.3) 8 l где Р – давление, под действием которого происходит течение; r и l – радиус и длина капилляра соответственно; Q – объём жидкости, вытекающей за время t. Это уравнение известно как у р а в н е н и е П у а з е й л я, который впервые получил его эмпирическим путем. Если течение жидкости подчиняется закону Ньютона, для нее справедливо уравнение Пуазейля и наоборот. Такие жидкости называются ньютоновскими, и для них характерно, что вязкость не зависит от приложенного напряжения сдвига.
Уравнение Пуазейля лежит в основе одного из наиболее распространенных методов определения вязкости – метода к а п и л л я р н о й в и с к оз и м е т р и и, который заключается в определении времени истечения определенного объёма жидкости через капиллярную трубку с известным значением радиуса и длины. Рассчитанное по уравнению (6.3) значение вязкости представляет собой а б с о л ю т н у ю вязкость жидкости. Часто измеряют не абсолютную, а относительную вязкость отн = ( 0 ), где 0 – вязкость какой-либо жидкости, выбранной за стандартную. В случае растворов
Величина [] характеризует гидродинамическое сопротивление, которое оказывают течению жидкости отдельные частицы (или макромолекулы в случае растворов полимеров), и связано с размером частиц (молекулярной массой полимера).
Уравнения Ньютона и Пуазейля описывают течение жидкостей, но ничего не говорят о его молекулярном механизме. Представления об этом механизме развиты в работах Я.И. Френкеля, а также Эйринга. Молекулы жидкости находятся в непрерывном теплом движении, совершая скачки из одного положения с минимумом потенциальной энергии в другое. Если отсутствуют внешние силы, перемещения равновероятны во всех направлениях. При наличии внешнего силового поля потенциальная энергия (Е2) после перехода в новое положение в направлении действия силы будет меньше потенциальной энергии (Е1) до перехода, такие переходы энергетически предпочтительнее, чем в обратном направлении и происходят чаще. Хаотическое движение приобретает направленность и возникает перенос вещества, т.е. течение жидкости. При повышении температуры с увеличением средней кинетической энергии теплового движения молекул повышается частота тепловых скачков, уменьшается время «оседлой» жизни частиц, что проявляется в снижении вязкости. Кроме того, с повышением температуры увеличивается число молекул, обладающих энергией, необходимой для преодоления потенциального барьера, разделяющего положения с энергией Е1 и Е2. Наконец, и сама высота этого потенциального барьера снижается вследствие теплового расширения жидкости, увеличения среднего расстояния между молекулами и уменьшения энергии межмолекулярного взаимодействия. Все это объясняет хорошо известный факт заметного с н и ж е н и я в я з к о с т и (и повышения текучести) жидкостей с повышением температуры. В не слишком широкой области температур вязкость снижается при нагревании приблизительно в соответствии с уравнением Аррениуса:
= A exp ( E RT ), где Е – энергия активации вязкого течения – энергия, которую должна приобрести молекула, чтобы преодолеть потенциальный барьер и перескочить в новое положение равновесия, k – постоянная Больцмана, Т – абсолютная температура, А – коэффициент, слабо зависящий от температуры.
6.1.2.1. Зависимость вязкости коллоидных растворов от концентрации дисперсной фазы. Вязкость коллоидных растворов всегда выше вязкости чистой дисперсионной среды вследствие гидродинамического сопротивления, которое оказывают частицы движению слоев при течении жидкости. Эйнштейн (1906 г.), исходя из чисто гидродинамических представлений, вывел уравнение, устанавливающее связь между вязкостью коллоидного раствора (золя) и концентрацией дисперсной фазы:
s = 0 ( 1 + 2,5 ), (6.4) где s и 0 – вязкость золя и дисперсионной среды соответственно; – объемная концентрация (объемная доля) дисперсной фазы. Объемная доля дисперсной фазы численно равна суммарному объему частиц, содержащихся в единице объема системы, так что, если известна весовая концентрация золя с (г/см3) и плотность частиц (г/см3), то = ( с ).
Уравнение (6.4) справедливо при условии, что частицы являются твердыми, имеют сферическую форму, концентрация их невелика, так что между ними отсутствуют взаимодействия.
В общем случае s = 0 ( 1 + ), где – коэффициент, численное значение которого зависит от формы частиц.
В соответствии с уравнением Эйнштейна относительная вязкость золя возрастает прямо пропорционально концентрации дисперсной фазы:
отн = ( 0 ) = 1 + 2.5, (6.5) уд = = 2,5.
Эта закономерность сохраняется в области малых концентраций, но при повышении наблюдается отклонение от линейной зависимости (на рис. 6.3 представлена схематически такая зависимость для относительной вязкости). Подобные отклонения могут быть вызваны различными по физической природе причинами. Это могут быть гидродинамические и механические взаимодействия коллоидных частиц, взаимодействия, связанные с наличием заряда и двойного электрического слоя на поверхности частиц. В последнем случае возникает так называемый э л е к т р о в я з к о с т н ы й эффект, который обнаруживается в том, что вязкость золей, частицы которых несут электрический заряд, выше вязкости золей с незаряженными частицами. Смолуховский вывел уравнение, связывающее удельную вязкость золя с величиной электрокинетического потенциала частиц:
Согласно уравнению Смолуховского, вязкость коллоидных растворов должна с н и ж а т ь с я при введении электролитов, что подтверждается экспериментально. Это происходит как вследствие сжатия ДЭС и понижения -потенциала, так и в результате увеличения электропроводности межмицеллярной жидкости.
Интересно отметить, что вязкость заряженных золей в соответствии с уравнением Смолуховского зависит от радиуса частиц в отличие от золей с незаряженными частицами (в уравнение Эйнштейна размер частиц не входит).
6.1.2.2. Количественная оценка сольватации частиц по вискозиметрическим данны. Явления сольватации (в водных системах – гидратации) охватывают широкий диапазон явлений, обусловленных взаимодействием растворенных или коллоидно диспергированных веществ, а также макроповерхностей с молекулами окружающей жидкой среды. Это сольватация ионов и неионизированных молекул в истинных растворах как низкомолекулярных веществ, так и полимеров, гидратация коллоидных частиц с гидрофилизированной поверхностью, образование полимолекулярных граничных сольватных слоев на макроскопических поверхностях, погруженных в жидкость и др.
Существуют различные способы количественной оценки гидратации, основанные на том, что жидкость в граничных сольватных прослойках, как установлено многочисленными исследованиями, обладает особой структурой и вследствие этого аномальными свойствами, отличающими ее от обычной жидкости в объеме. В частности для сольватно связанной жидкости характерно наличие упругости и прочности на сдвиг, что характеризует ее как твердообразное тело. Сольватные слои, связанные с поверхностью частицы молекулярными силами, в кинетическом отношении образуют вместе с частицей единое целое и перемещаются вместе с нею.
Влияние сольватных слоев на реологические свойства золей проявляется в том, что они увеличивают эффективный объем дисперсной фазы и в соответствии с уравнением Эйнштейна повышают вязкость системы. Этот эффект может быть использован для расчета толщины сольватной оболочки по вискозиметрическим данным.
Пусть сферическая частица радиусом r имеет слой сольватно связанной жидкости толщиной (рис. 6.4), в результате чего эффективная объемная доля дисперсной фазы золя * выше истинной объемной доли, не включающей объём сольватного слоя: *. Отношение этих величин дает величину коэффициента сольватации = ( * ) 1.
* = ( r + ). Разделив почленно эти уравнения одно на другое и решая полученное выражение относительно величины, получим:
= r ( 3 K 1). (6.7) Для расчета К истинную объемную долю находят по формуле = ( с ), величину * рассчитывают, используя уравнение Эйнштейна (5) (заменив в нем величину на * ), или одну из его модификаций. Для полидисперсных систем речь идет о среднем радиусе и об усредненной (эффективной) толщине гидратных слоев.
Найденные из вискозиметрических измерений эффективные толщины гидратных прослоек на поверхности частиц синтетических латексов составляют по данным различных авторов от 3–5 до 15–20 нм.
6.1.2.3. Зависимость вязкости от скорости течения жидкости (напряжения сдвига). Закон вязкого течения жидкостей Ньютона справедлив для течения в ламинарном (послойном) режиме, при условии, что сдвиговые напряжения не вызывают перестройки структуры системы. В таком случае в соответствии с уравнениями (6.2) и (6.2а) между приложенным напряжением сдвига и скоростью течения имеется прямо пропорциональная зависимость (рис. 6.5), а соответствующая прямая выходит из начала координат.
Рис. 6.5. Зависимость (1) скорости течения и (2) вязкости от напряжения сдвига для ньютоновской жидкости Последнее означает, что течение начинается при любой сколь угодно малой величине напряжения сдвига, что является признаком, отличающим жидкое (и газообразное) агрегатные состояния. Величина вязкости характеризуется наклоном прямой = f ( & ) : = ctg.
График в координатах уравнения Ньютона = f ( & ) называется кривой течения (или р е о л о г и ч е с к о й к р и в о й). Критерий, по которому жидкость может быть отнесена к н ь ю т о н о в с к и м (или н о р м а л ь н ы м) – линейная зависимость между напряжением сдвига и скоростью течения и, следовательно, независимость вязкости от напряжения сдвига (при постоянной температуре и сохранении ламинарного режима течения):
= const (см. рис. 6.5). В этом случае вязкость является и н в а р и а н т н о й характеристикой жидкости, она не зависит от условий измерения (типа и размера вискозиметра, диаметра капилляра – от чего может зависеть скорость течения). При достижении достаточно высокой скорости течения линейность зависимости = f ( & ) нарушается, причиной чего является переход к турбулентному течению. Возникающие при этом завихрения, перемешивание слоев «забирают» часть энергии приложенного сдвигового усилия, так что эффективная вязкость жидкости возрастает.
В координатах уравнения Пуазейля реологическая кривая ньютоновской жидкости также имеет линейный характер. В этом случае ее строят в координатах 1 t – Р, где t – время истечения определенного объема жидкости. Величина 1 t характеризует скорость течения, Р – приложенное напряжение (давление). Между этими величинами, согласно уравнению Пуазейля, прямая пропорциональная зависимость: из уравнения (3) следует 8Ql P = C (1 t ), где C =. Заметим, что произведение t характеризует вязr4 кость: Pt = C, так что критерием ньютоновского поведения жидкости в этом случае является независимость величины Pt от P.
К ньютоновским жидкостям относятся чистые жидкости, истинные растворы, а также коллоидные растворы не слишком концентрированные, не содержащие удлиненных (анизометрических) или деформирующихся при течении частиц.
Во многих случаях для коллоидных систем наблюдаются отклонения от ньютоновского закона вязкого течения, т.е. нарушается пропорциональность между напряжением сдвига и скоростью течения, а вязкость перестает быть инвариантной величиной и зависит от скорости деформации (течения).
Такое явление наблюдается, например, для слабо структурированных жидкостей, примером которых могут быть разбавленные водные растворы желатины (менее 0.5 масс. %) или других водорастворимых полимеров. В таких растворах возможно образование поперечных связей между макромолекулами и образование несвязанных между собой «обрывков» малопрочной пространственной структурной сетки, способной разрушаться в результате сдвиговых усилий, возникающих в ламинарном потоке.
Такое рода структурообразование характерно и для малоконцентрированных ( 10 объем. %) суспензий (например, водных суспензий бентонита (глинистый минерал), охры и др. пигментов).
Типичный вид кривой течения подобных жидкообразных слабоструктурированных систем представлен на рис. 6.6 (аналогичный вид имеет кривая и в координатах уравнения Пуазейля). На кривой можно выделить три участка, различающихся по характеру зависимости скорости течения от напряжения сдвига. На участке I жидкость течет как нормальная с постоянной высокой ньютоновской вязкостью 0 = ctg1.
На этом участке в области малых напряжений сдвига структура жидкости не меняется: элементы структуры не разрушаются, попадая в соседние слои, движущиеся с различной скоростью, они перемещаются как целое и создают значительное гидродинамическое сопротивление потоку, что определяет высокое значение начальной вязкости 0 (см. рис. 6.6). На участке II сдвиговые усилия возрастают и вызывают прогрессирующее (по мере роста напряжения ) разрушение структурированных участков, что снижает их сопротивление потоку и приводит к более значительному росту скорости течения, чем это отвечает прямой пропорциональности между & и, т.е.
жидкость течет как неньютоновская. На этом участке значение вязкости, рассчитываемое как отношение &, является эффективной величиной, зависящей от напряжения сдвига. Можно видеть, что на участке II с увеличе
б нием напряжения сдвига эффективная вязкость понижается в связи с изменением структуры жидкости по мере ее разрушения. (Участок II называют ветвью с т р у к т у р н о й в я з к о с т и). В области высоких напряжений сдвига и соответственно – высоких скоростей течения на участке III разрушение структуры полностью завершается, жидкость снова течет как ньютоновская с постоянной минимальной предельной вязкостью, которая определяется наклоном этого участка: = ctg 2.
Помимо структурирования известны и другие причины неподчинения коллоидных систем законам Ньютона и Пуазейля.
Так, описанная выше аномалия вязкого течения характерна также для золей, имеющих вытянутые, палочкообразные частицы. В этом случае причина аномалии вязкого течения заключается в том, что по мере увеличения напряжения сдвига, обусловливающего течение, анизометрические частицы ориентируются своей длинной осью в направлении потока, что снижает гидродинамическое сопротивление и приводит к снижению вязкости.
Аналогичная аномалия наблюдается у эмульсий и других систем с деформирующимися частицами. Капельки дисперсной фазы с возрастанием приложенного напряжения сдвига удлиняются, приобретая эллипсоидальную форму, что облегчает течение и понижает вязкость. То же самое наблюдается при течении растворов высокомолекулярных соединений (даже в отсутствие пространственного структурирования и структурной вязкости).
Свернутые в статистический клубок макромолекулы разворачиваются, принимая вытянутую конформацию, с ориентацией таких макромолекул в направлении потока.
6.1.3. Пластическая вязкость. Ползучесть. Более сложное реологическое поведение обнаруживают системы, обладающие малопрочной сплошной структурной сеткой, способной разрушаться при действии сравнительно малых усилий. К таким системам относятся с т у д н и – твердообразные тела, образующиеся при охлаждении не слишком разбавленных растворов полимеров (например, 1–5%-х водных растворов желатины, агара, полиакриламида и т.д.), а также г е л и – связно-дисперсные системы, в которые превращаются золи (при определенных условиях) в результате молекулярного сцепления отдельных частиц дисперсной фазы с образованием рыхлого каркаса – пространственной сетки, охватывающей весь объем системы. В обоих случаях наличие пространственной сетки (каркаса) приводит к утрате текучести и появлению некоторых свойств, присущих твердому телу, – способности сохранять форму, появлению упругости, прочности на сдвиг.
При этом концентрация дисперсной фазы (или полимера в студне) может быть весьма малой. Так, золи V2O5 c удлиненными игольчатыми частицами могут образовывать прочные гели уже при концентрации дисперсной фазы менее 0.1 мас. %. Такие системы по существу представляют собой утратившие текучесть сильно структурированные жидкости.
Ф.Н. Шведов, а позже Бингам предположили, что течение систем с малопрочной пространственной сеткой начинается лишь тогда, когда напряжение сдвига превысит некоторое критическое значение, т.е. при условии – 0. Такое течение называют п л а с т и ч е с к и м, а предельное напряжение сдвига – п р е д е л о м т е к у ч е с т и (или п р е д е л о м у п р у г о с т и, т.к. при тело обычно проявляет упругую деформацию).
Тела, проявляющие способность к пластическому течению, называют п л а ст и ч н ы м и. Пластическое течение описывается уравнением Бингама:
= ( du dx ), (6.8) где – п л а с т и ч е с к а я в я з к о с т ь (или бингамовская вязкость). При отсутствии структурной сетки = 0 и уравнение Бингама переходит в уравнение Ньютона, а пластическая вязкость – в истинную (ньютоновскую) вязкость. Кривая течения системы, обладающей пластической вязкостью, имеет вид прямой, выходящей из точки на оси абсцисс, которая отвечает пределу текучести (рис. 6.7). Величина пластической (бингамовской) вязкости определяется выражением:
= ( du dx ) и может быть графически найдена по наклону прямой: = ctg. Можно видеть, что пластическая (бингамовская) вязкость, как и ньютоновская вязкость нормальных жидкостей, не зависит от напряжения сдвига (при ).
Систему, точно подчиняющуюся уравнению Бингама, называют идеальным пластическим телом Бингама. Пластичными телами, довольно хорошо подчиняющимися уравнению Бингама, являются консистентные смазки, 5–10%-е пасты глинистых минералов.
Рис. 6.7. Кривая течения идеального пластического тела Однако в большинстве случаев для сильно структурированных систем наблюдается отклонение от закона Бингама, и график течения & имеет вид кривой, представленной на рис. 6.8а. Это так называемая полная реологичеаяская кривая структурированной дисперсной системы. В области очень малых напряжений сдвига (участок I) система ведет себя как твердообразная, деформация имеет упругий характер. При достижении с т а т и ч е с к о г о п р е д е л ь н о г о н а п р я ж е н и я с д в и г а s (предела текучести) начинается процесс медленного вязко-пластического течения, причем в системе с практически неразрушенной структурой – явление, получившее название п о л з у ч е с т ь (Шведов). По Ребиндеру механизм ползучести предполагает, что при любой скорости течения в коагуляционной структуре протекают два противоположных процесса – разрушение и восстановление молекулярного сцепления (контакта) между частицами.
Динамическое равновесие между этими процессами в установившемся потоке характеризуется эффективной вязкостью. При малых напряжениях сдвига системе наносятся незначительные повреждения, так как нарушенные контакты вследствие медленности процесса течения успевают тиксотропно восстановиться. В результате течение происходит практически без разрушения структуры, т.е. наблюдается явление ползучести.
При достижении некоторой величины = d равновесие между разрушением и восстановлением контактов смещается в сторону разрушения и при d наблюдается область течения энергично разрушаемой структуры. Величину d называют предельным д и н а м и ч е с к и м н а п р я ж е н и е м сдвига. После полного разрушения структуры (участок IV) система проявляет свойства ньютоновской жидкости (при условии сохранения ламинарного режима течения).
Полная реологическая кривая также может быть представлена в виде зависимости эффективной вязкости = & от напряжения сдвига (рис. 6.8б); значение min отвечает вязкости системы с полностью разрушенной структурой, max – вязкости в области ползучести. Разность max min может достигать нескольких порядков.
Следует отметить, что величины s, d и (max min ) являются важными реологическими параметрами системы, ими характеризуют ее механические свойства.
6.2. Оптические свойства коллоидных систем
6.2.1. Общая характеристика. При прохождении луча света через дисперсную систему (золь) наблюдается ряд характерных явлений.
1) Ход луча обнаруживается визуально в виде светящейся полосы (эффект Тиндаля). Такие среды называются м у т н ы м и в отличие от чистых жидкостей и истинных растворов, которые являются о п т и ч е с к и п у с т ы м и.
2) Происходит ослабление интенсивности проходящего света Iпр по сравнению с падающим (I0): Iпр I0.
3) В случае разбавленных «белых» золей с неокрашенными (непоглощающими свет) частицами можно заметить неодинаковые оттенки окраски золя в разных направлениях: в проходящем свете – оранжевый, а при наблюдении сбоку – голубоватый.
4) золи металлов обычно имеют яркую окраску, которая зависит не только от природы частиц, но и от степени дисперсности (так, золи золота могут быть красными, синими, коричневыми и др.).
Этот далеко не полный перечень характеризует своеобразие оптических свойств дисперсных систем, связанное с их микрогетерогенностью.
Эти свойства обусловлены взаимодействием светового луча с дисперсными частицами. В грубодисперсных системах, когда d (d – поперечник частицы, – длина волны), происходит отражение луча от поверхности частицы, преломление, полное внутреннее отражение, в результате чего направление распространения луча изменяется (рис. 6.9) – свет распространяется по всем направлениям в пространстве, отличным от первоначального. Этим объясняется мутность грубых взвесей.
Рис. 6.9. Рассеяние света крупными частицами суспензии В случае коллоидно-дисперсных систем ( d ) рассеяние света и мутность имеют другую причину – д и ф р а к ц и ю с в е т а на частицах, малых по сравнению с длиной волны. В этом случае также свет рассеивается по всем направлениям и в результате Iпр I0. Для белых золей это уменьшение интенсивности проходящего света обусловлено только рассеянием и называется ф и к т и в н ы м поглощением (о п а л е с ц е н ц и е й). Золи металлов проявляют наряду с фиктивным также истинное поглощение – избирательную абсорбцию, сопровождающуюся превращением световой энергии в теплоту, и обнаруживают определенную окраску.
В совершенно однородной среде свет не рассеивается. В соответствии с принципом Гюйгенса каждую точку среды, до которой дошел фронт волны, можно рассматривать как новый источник колебаний. Вторичные колебания усиливают друг друга в направлении распространения волны и гасятся в других направлениях. Если на пути распространения волны возникает локальная неоднородность (с другим показателем преломления), то каждая точка ее становится самостоятельным центром колебаний. Если размер неоднородности значительно больше длины световой волны, то наблюдается в основном отражение света. При размере неоднородности меньше длины волы колебания, исходящие от каждой точки неоднородности, не имеют определенных разностей фаз и усиливают друг друга во всех направлениях. Возникает рассеяние света.
6.2.2. Рассеяние света. Уравнение Рэлея. Рассеянный свет характеризуется следующими особенностями.
1) При опалесценции не происходит изменения длины волны; такое рассеяние называют «упругим». Поэтому при освещении золя монохроматическим светом опалесцирующая система имеет тот же цвет, что и падающий луч. Этим данное явление отличается от явлений люминесценции, например, флуоресценции. (Флуоресценция, наблюдаемая в растворах некоторых веществ, представляет собой внутримолекулярный процесс, состоящий в том, что молекулы флуоресцирующего вещества селективно поглощают свет определенной длины волны и трансформируют его в световые лучи с большей длиной волны.)
2) Интенсивность светорассеяния неодинакова по различным направлениям. Наибольшая доля рассеянного света отвечает направлениям 0о и 180о относительно направления падающего света.
3) Рассеянный свет частично поляризован, причем доля поляризованного света также зависит от направления.
Угловое распределение рассеянного света наглядно представляет векторная диаграмма Ми (рис. 6.10). На ней интенсивность неполяризованного и поляризованного (заштриховано) рассеянного света представлена радиусами-векторами соответствующей длины и направления. Cплошная линия, соединяющая концы векторов – и н д и к а т р и с а с в е т о р а с с е я н и я.
Для очень малых частиц (d ) индикатриса симметрична, наибольшее суммарное светорассеяние наблюдается в прямом и обратном направлениях относительно падающего луча, при этом поляризации не наблюдается.
Под углом 90о рассеянный свет полностью поляризован. При увеличении размера частиц (d ) увеличивается доля света, рассеивающегося в «прямом» направлении (индикатриса «вытягивается вперед», в направлении падающего луча).
Рис. 6.10. Угловое распределение света, рассеянного малой (а) и крупной (б) сферическими частицами. Заштрихована область поляризованного рассеянного света Теория светорассеяния частицами, малыми в сравнении с длиной волны, развита Рэлеем. Он вывел уравнение светорассеяния для сферических непроводящих частиц (диэлектриков), концентрация которых достаточно мала, так что отсутствует вторичное рассеяние (когда свет, рассеянный одной частицей рассеивается на соседней частице). При выполнении всех этих условий суммарная интенсивность света Iр, рассеянного по всем направлениям в пространстве единицей объема рассевающей среды, равна
где n и n0 – показатели преломления дисперсной фазы и дисперсионной среды; – численная концентрация (число частиц в 1 см3 коллоидной системы); V – объем одной частицы; – длина волны монохроматического света в данной среде.
V = r 3, а численную концентрацию через весовую с (в г/см ) по формуле = с/(V ), где – плотность дисперсной фазы, то мутность будет выражаться уравнением Рэлея в виде:
I0 Из уравнения Рэлея можно сделать следующие выводы.
1. Для частиц данного размера мутность золя прямо пропорциональна его концентрации. Это положение используется для определения концентрации дисперсной фазы с помощью измерения светорассеяния золя.
2. При данной концентрации дисперсной фазы мутность очень резко возрастает с увеличением размера частиц (пропорциональна кубу их радиуса). Линейная зависимость – r 3 сохраняется лишь в сравнительно узкой области размеров, пока частицы значительно меньше длины волны света. Далее с увеличением размера частиц рост величины замедляется, и для частиц с размером, превышающим, светорассеяние переходит в отражние света и по мере увеличения частиц интенсивность рассеянного света уменьшается. Таким образом, зависимость – r 3 проходит через максимум, что подтверждается опытом.
3. Интенсивность светорассеяния резко возрастает с уменьшением длины волны падающего света. Поскольку величина пропорциональна 1
–, то при освещении бесцветного золя белым светом рассеиваются главным образом короткие волны (сине-фиолетовая часть спектра), так что при наблюдении сбоку такой золь имеет синеватую окраску. В проходящем свете золь имеет красновато-оранжевый оттенок, т.к. спектр проходящего света обогащен длинноволновыми лучами.
Преимущественное рассеяние света с малой длиной волны объясняет ряд природных оптических явлений. Причина голубого цвета неба днем в том, что наблюдатель видит свет, рассеянный в атмосфере Земли, а утром и вечером оранжевый или красный цвет неба обусловлен тем, что наблюдается главным образом свет, прошедший через атмосферу. На зависимости светорассеяния от длины световой волны основано также применение синего света для светомаскировки (он сильно рассеивается в толще воздуха и незаметен с самолета), а красного и оранжевого – для сигнализации (противотуманные фары).
Уравнение Рэлея (6.10) широко используется для определения размера коллоидных частиц по измерениям мутности. Следует иметь в виду, что область его применимости ограничивается условиями «рэлеевского» рассеяния, когда размер частиц не превышает 1/5–1/10 длины волны падающего света. Для частиц большего размера интенсивность рассеянного света изменяется обратно пропорционально не четвертой, а меньшей степени длины волны: d
1 n, где n 4. Для непроводящих сферических частиц с увеличением размера до d величина n уменьшается в пределе до 2.
Геллер предложил выразить мутность формулой:
В поле зрения оптического микроскопа коллоидные растворы представляются оптически пустыми, т.к. размеры частиц меньше длины волны лучей видимой части спектра. Однако с помощью микроскопа можно обнаружить свет, рассеиваемый частицами. Это возможно, если объект (золь) освещается сбоку, таким образом, чтобы проходящий свет не попадал в поле зрения микроскопа. Тогда частицы, будучи сами невидимыми, обнаруживаются как яркие светящиеся точки на фоне темного поля зрения. Это дает возможность подсчитывать число частиц, наблюдать их движение, оценивать средний размер, судить об их форме. Если частицы имеют неправильную форму (анизометричны), то они наблюдаются как мерцающие светящиеся точки, т.к. при вращении в процессе теплового движения они рассеивают разное количество света в зависимости от ориентации относительно направления падающего луча.
Для наблюдений «на фоне темного поля» широко используются так называемые конденсоры темного поля, которые могут устанавливаться на обычный микроскоп (рис. 6.11). В таком конденсоре центральная диафрагма 2 препятствует прямому попаданию света на объект 4, а проходящие боковые лучи 1 отражаются от поверхности зеркальных плоско-выпуклых линз 3, так что они проходят мимо объектива.
Рис. 6.11. Схема хода лучей в конденсоре темного поля С помощью метода ультрамикроскопии были проведены исследования броуновского движения и диффузии в коллоидных системах (Сведберг, Перрен и др.), подтверждена правильность теории этих явлений, развитая Эйнштейном и Смолуховским, показана общность молекулярно-кинетических свойств этих систем и систем молекулярной дисперсности. Все это явилось доказательством правильности молекулярно-кинетической теории в целом, что выходит за рамки собственно коллоидной химии и имеет общенаучное значение.
6.2.4. Рассеяние света в гомогенных средах. Индивидуальные жидкости и газы, казалось бы, не должны рассеивать свет в отсутствие дисперсных частиц, отличающихся от среды по показателю преломления.
Между тем в большой толще таких сред также наблюдается заметное светорассеяние. Теория этого явления (Эйнштейн) исходит из того, что в гомогенных средах оптическими неоднородностями, на которых происходит рассеяние света, являются флуктуации плотности (в газах, жидкостях) и концентрации (в случае истинных растворов). Флуктуации вызывают локальные отклонения оптических свойств (показателя преломления) в отдельных микрообъемах среды от их среднего значения для данной фазы. Для истинных (молекулярных) растворов Эйнштейн получил на основе этой предпосылки следующее выражение для мутности, вызванной флуктуациями концентрации:
Следует отметить, что оптический метод определения молекулярной массы пригоден лишь в случае, когда размер макромолекул меньше 0.1 (это условие обычно соблюдается для растворов полимеров, макромолекулы которых свернуты в клубок).
Описанный метод применяется также для определения средней мицеллярной массы в растворах коллоидных поверхностно-активных веществ.
6.2.5. Абсорбция (поглощение) света в коллоидных растворах. Как отмечалось выше, коллоидные растворы могут иметь определенную окраску, что свидетельствует о способности частиц данной дисперсной фазы селективно поглощать свет, в результате чего интенсивность проходящего через раствор света уменьшается. Определенный вклад в это вносит также рассеяние света на коллоидных частицах.
В случае неокрашенных («белых») золей также наблюдается ослабление проходящего через них света – происходит кажущееся (фиктивное) поглощение света (без изменения его спектрального состава), обусловленное в данном случае лишь светорассеянием.
Пусть через слой белого золя толщиной l проходит луч монохроматического света, начальная интенсивность которого равна I0 (рис. 6.13). Ослабление интенсивности света dI, проходящего через слой исследуемой системы толщиной dx, пропорционально интенсивности света I, падающего на этот слой:
глощения света окраска зависит не только от природы поглощающего вещества (дисперсной фазы), но и от дисперсности. Так, предельно высокодисперные золи золота сильно поглощают свет в сине-фиолетовой части спектра ( 500–530 нм) и имеют красную окраску (рис. 6.14, кривая 1), а с повышением размера частиц максимум поглощения сдвигается в область более высоких длин волн и в пределе золи приобретают синюю окраску (рис. 6.14, кривая 2). Причина этого, по крайней мере, частично связана с тем, что на абсорбцию света золями косвенно (через светорассеяние) оказывает влияние размер частиц.
4. Русанов А.И. Мицеллообразование в растворах поверхностно-активных веществ / А.И. Русанов. – СПб. : Химия, 1992.
5. Ребиндер П.А. Избранные труды. Поверхностные явления в дисперсных системах. Коллоидная химия / П.А. Ребиндер. – М. : Наука, 1978.
6. Сумм Б.Д. Объекты и методы коллоидной химии в нанохимии / Б.Д. Сумм [и др.] // Успехи химии. – 2002. – Т. 57, № 10. – С. 1018–1028.
7. Захарова Л.Я. Факторы, определяющие каталитический эффект супрамолекулярных систем на основе поверхностно-активных веществ в реакциях нуклеофильного замещения в эфирах кислот тетракоординированного фосфора : автореф. дисс. …доктора химических наук / Л.Я. Захарова. – Казань, 2005. – 42 с.
8. Мартинек К. Реакции в мицеллах и мицеллярный катализ в водных средах / К.Мартинек [и др.]. – В кн. : Мицеллообразование, солюбилизация, микроэмульсии / под ред. В.Н. Измайловой. – М. : Мир, 1980.
9. Штыков С.Н. Химический анализ в нанореакторах: основные понятия и применение / С.Н. Штыков // Журн. аналитич. химии. – 2002. – Т. 57. – № 10. – С. – 1018–1028.
Подп. в печ. 11.10.2011. Усл. печ. л. 10,9. Заказ 188.
Издательско-полиграфический центр Воронежского государственного университета.
394000, г. Воронеж, пл. им. Ленина, 10. Тел. (факс): +7 (473) 259-80-26 http://www.ppc.vsu.ru; e-mail: pp_center@ppc.vsu.ru




















2016 www.metodichka.x-pdf.ru — «Бесплатная электронная библиотека — Методички, методические указания, пособия»
Материалы этого сайта размещены для ознакомления, все права принадлежат их авторам.
Если Вы не согласны с тем, что Ваш материал размещён на этом сайте, пожалуйста, напишите нам, мы в течении 1-2 рабочих дней удалим его.
Вязкость дисперсных систем
Важной характеристикой структурно-механических свойств является течение. Течение бывает ламинарным и турбулентным.
Ламинарное течение – движение жидкости в виде параллельных слоев, имеющих различную скорость и не смещающихся между собой. Возникает при низкой скорости течения и малом перепаде давления.
Турбулентное течение – течение, сопровождающееся вихреобразованием.
В соответствие с уравнением Ньютона сила сопротивления при течении F прямо пропорциональна градиенту скорости du и площади поверхности потока S:
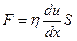
где η – коэффициент пропорциональости или вязкость, зависит от природы жидкости Единицей измерения вязкости является пуаз (пз), 1 пз = Па∙с= Н∙с/м 2 . Единица измерения вязкости названа в честь франц. учёного Пуазейля, который впервые изучал движение жидкости в капиллярах.
Ламинарное течение по трубкам или скорость течения жидкости из капилляра описывается уравнением Пуазейля (1842г.), которое было найдено экспериментальным путём:
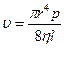
где u — объемная скорость течения;
r – радиус капилляра трубки;
Δp – перепад давления или разность давления на обоих концах трубки;
Η – вязкость жидкости;
l – длина капилляра.
Величина, обратная вязкости 

Жидкости, у которых отсутствует зависимость вязкости от характера взаимодействия частиц, подчиняются законам Ньютона и Пуазейля и называются ньютонскими жидкостями. Уравнение Ньютона и Пуазейля соблюдается, если жидкость движется ламинарно.
Вязкость дисперсных систем всегда превышает вязкость чистой дисперсионной среды. Зависимость вязкости коллоидной системы от концентрации дисперсной фазы выражается уравнением Эйнштейна (1906г.):
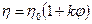
где η – вязкость коллоидной системы;
η0 – вязкость чистого растворителя (дисперсионной среды);
φ – объемная доля частиц дисперсной фазы;
k – коэффициент, характеризующий форму частицы. Для сферической формы k = 2,5.
Для структурированных систем законы Ньютона не выполняются.
Реологические свойства дисперсных систем
Типы структур
Дисперсные системы по кинетическим свойствам дисперсной фазы и дисперсионной среды можно разделить на свободнодисперсные u связнодисперсные. В свободнодисперсных (неструктурированных) системах частицы дисперсной фазы не связаны между собой и могут свободно перемещаться независимо друг от друга. В связнодисперсных системах частицы между собой связаны и образуют структурную сетку. Они не могут перемещаться свободно и совершают только колебательные движения около положения равновесия. Структуры образуются под действием сил Ван-дер-Ваальса и ближнедействующих химических сил в концентрированных суспензиях, эмульсиях, пастах. Переход свободнодисперсной системы в связнодисперсную является результатом потери системой агрегативной устойчивости.
Среди связнодисперсных систем по Ребиндеру, в зависимости от природы действующих сил, различают два основных типа структур: коагуляционные и конденсационно-кристаллизационные.
Коагуляционный тип структуры образуется за счет сцепления частиц ван-дер-ваальсовыми силами. Системы с такой структурой обладают вязкостью и пластичностью, а при действии нагрузки способны к обратимому разрушению, то есть могут восстанавливаться во времени. В рамках теории ДЛФО такие структуры отвечают безбарьерной коагуляции (на дальних расстояниях) и поэтому обратимы. В местах контактов между частицами в структуре имеется тонкая прослойка дисперсионной среды. Наличие этой прослойки придает эластичность структуре, однако снижает ее прочность. Под действием значительной механической нагрузки такую структуру можно разрушить.
Конденсационно-кристаллизацuонный тип структур, образуется за счет не только ван-дер-ваальсовских сил, но и за счет ближнедействующих валентных сил — химических связей. Поэтому связи в местах контакта получаются более прочными, а под действием механической нагрузки они необратимо разрушаются. Для таких систем характерны упругие, но хрупкие свойства. По теории ДЛФО образования этих структур происходит с преодолением потенциального барьера отталкивания частиц ∆U (на ближних расстояниях) и носит необратимый характер. Примерами дисперсных систем такого типа являются: цемент, гипс, глина, известь, стройматериалы.
Переходной формой от коагуляционной к конденсационно-кристаллизационной структуре являются точечные контакты, для которых характерны контакты площадью в один или несколько атомов. Во втором типе структур осуществляются кроме точечных и фазовые контакты, которые образуются на значительно большей площади, соизмеримой с размерами частиц.
Самопроизвольный переход от коагуляционного типа структур к конденсационно-кристаллизационному носит специфическое название синерезис — старение системы. В первый момент времени структурированная система образуется за счет малого количества контактов между частицами. Со временем, за счет теплового движения и стремления системы к уменьшению энергии, количество контактов возрастает. Часть дисперсионной среды, содержащаяся в петлях пространственной сетки, выделяется наружу, сетка стягивается, и происходит упорядочение структуры, а объем системы уменьшается. Явление синерезиса часто наблюдается в технологических процессах. Например, ухудшение качества кондитерских изделий объясняется синерезисом. Синерезис в живых клетках — это, например, старение человека.
Коагуляционные структуры обладают способностью к тиксотропии — самопроизвольному восстановлению структуры во времени после механического воздействия (в изотермичексих условиях), т. е. без нагревания, так как возможно и термическое разрушение структуры — плавление. При тиксотропии восстанавливаются связи, разрушенные вследствие механического воздействия.
Реология — это учение о процессах деформации и течения различных тел. Структурированные системы способны к деформации, простейшие виды которой растяжение и сдвиг. В последнем случае усилие прилагается к верхней грани образца, а нижняя грань его закреплена (рис. 9.4).
Деформация определяется безразмерными величинами 
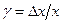
Деформация зависит от приложенного к телу напряжения Р, равного внешней силе F, приложенной к единице поверхности тела В. Зависимость Р от e приводится на рис. 9.5.
На участке I наблюдается прямо пропорциональная зависимость между Р и e, что характерно для упругой деформации. Для упругой деформации справедлив закон Гука:

где Е — модуль упругости Юнга (константа, характеризующая упругость материала).
Особенностью упругой деформации является то, что после снятия нагрузки тело восстанавливает свои первоначальные размеры (Р = 0; e = о).
Возможность дисперсной системы противодействовать внешнему усилию ограничена. При значении Р > Рк (участок II) может произойти разрушение тела или появиться остаточная деформация (Р = 0; e ¹ 0). Величина Рк — предел упругости. На участке III возможен переход упругой деформации в пластическую и течение тел. Величина РТ — это предел текучести. Деформация тел непосредственно связана с их структурой.
Реологические свойства дисперсных систем

Как известно, течение жидкообразных тел подчиняется закону Ньютона: напряжение сдвига пропорционально скорости деформации при сдвиге: 
где h — вязкость жидкости; 
Закон Ньютона можно сформулировать иначе: скорость деформации пропорциональна напряжению сдвига: 
В уравнении (9.3) роль коэффициента пропорциональности играет вязкость (или внутреннее трение), которая является важнейшим свойством, характеризующим структуру любой дисперсной системы. Она является реологuческой константой и определяет способность жидкости сопротивляться течению. Величина, обратная вязкости 
На рис. 9.6 представлены реологические кривые ньютоновских материалов с большей вязкостью h1 и меньшей вязкостью — h2. В координатах h-Р для тех же материалов получаются прямые, параллельные оси абсцисс (рис. 9.7).
Для течения идеальных жидкостей из капилляра Пуазейль предложил уравнение, которое является частным случаем уравнения Ньютона: 
где K – постоянная капилляра;
P – давление течения;
t — время течения из капилляра.
Согласно (9.4) h не зависит от давления, так как с ростом Р во столько же раз уменьшается t.
По законам Ньютона и Пуазейля вязкость не должна зависеть от внешнего давления только в ламинарном потоке. В условиях турбулентности вязкость начинает увеличиваться с ростом давления, и основные законы вязкого течения оказываются не применимыми.
Вязкость дисперсных систем отличается от вязкости дисперсионной среды за счет заполнения части растворителя дисперсной фазой. Вязкость таких систем растет по мере увеличения концентрации дисперсной фазы. Если концентрация дисперсной фазы невелика и столкновение частиц исключается, то для определения вязкости можно пользоваться формулой Эйнштейна:

где h, h0— вязкость дисперсной системы и дисперсионной среды;
a — коэффициент, учитывающий форму частиц (для сферических частиц a = 2,5);
Vоб— объемная концентрация дисперсной фазы ( 
В соответствии с уравнением (9.5), вязкость дисперсной системы увеличивается по мере увеличения объемной концентрации( рис. 9.8, кривая 1). Формула (9.5) справедлива, если концентрация дисперсной фазы не превышает 6 %. При увеличении Vобдо 30 % можно пользоваться формулой, которая отличается от уравнения Эйнштейна последним членом:

Из уравнения (9.6) видно, что, по мере увеличения концентрации дисперсной фазы линейная зависимость h — Vобнарушается в условиях взаимного столкновения частиц, однако при данной концентрации вязкость остается постоянной. Подобные системы, подчиняющиеся уравнениям Ньютона, Пуазейля и Эйнштейна, называются нормальными или ньютоновскuми.
Для структурированных систем наблюдается отклонение от теоретической зависимости уже при малых концентрациях (рис. 9.8, кривая 2). Они не подчиняются законам Ньютона, Пуазейля и Энштейна и называются аномальными или неньютоновскими.

Правильнее деление текучих материалов на ньютоновские и неньютоновские проводить по признаку зависимости или независимости вязкости h от напряжения сдвига Р. По сравнению с обычными (неструктурированными) жидкостями, структурированные системы обладают повышенной вязкостью, хотя вязкость и не является критерием структурообразования. Например, вязкость плазмы крови, являющейся структурированной системой, ниже, чем глицерина, не образующего структур.
Наличие структуры изменяет характер течения жидкости. Поэтому исследование кривых зависимости скорости течения 

Измерение вязкости дисперсных систем, в зависимости от скорости течения, широко используется на практике. В технологическом процессе на различных его стадиях вязкость структурированных дисперсных систем может сильно изменяться. В ряде случаев, например, при транспортировке, необходимо, чтобы продукт имел максимальную вязкость, то есть был структурированным, а для перекачки продукта, напротив, нужно создавать такую скорость течения, которая бы соответствовала его минимальной вязкости.
Вязкость коллоидной системы зависит от
· концентрации дисперсной фазы,
· природы дисперсионной среды и дисперсной фазы,
Вязкостьжидкости – это сопротивление передвижения одного слоя жидкости относительно другого слоя.
Единица вязкости – Пуаз, он характеризует жидкости, в которых слои в одном квадратном сантиметре на расстоянии одного сантиметра движутся относительно друг друга со скоростью одного сантиметра в секунду под действием силы в одну дину 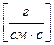

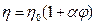
где j — объемная концентрация дисперсной фазы;
h0 — динамическая вязкость дисперсионной среды;
a — коэффициент, зависящий от формы частиц.


Из уравнения следует, что:
1) h пропорциональна концентрации дисперсной фазы;
Для концентрированных систем уравнение Эйнштейна неприменимо. Это объясняется целым рядом причин:
1. В жидкости около частиц возникает макропоток, затрудняющий движение системы;
2. Сольватация частиц. Оно проявляется в увеличении объема частиц за счет адсорбции дисперсионной среды;
3. Проявление сил отталкивания между частицами, несущими одинаковые заряды. Смолуховский показал, что hзаряженных частиц больше, чем hнезаряженных.

где h0 – вязкость среды;
n — удельная электропроводность;
r — радиус частиц;
e — диэлектрическая проницаемость.
Структурная вязкость — вязкость структурированных систем, т.е. систем, где наблюдается явная тенденция образования пространственных молекулярных сеток между частицами дисперсной фазы. Они не подчиняются закону Ньютона и в случае образования структуры течение системы начинается лишь тогда, когда напряжение сдвига Р превысит какое-либо критическое значение PT, необходимое для разрушения структуры, т.е. когда начинает выполняться условие Р > PT. Такое течение Бингам назвал пластическим, а критическое напряжение сдвига (предельное) – пределом текучести.

где h¢ — вязкость, отвечающая пластическому течению системы или пластическая вязкость;
dU/dx – градиент скорости.
Теория Эйнштейна была использована Штаудингером для установления формулы вязкости разбавленных растворов полимеров. Для растворов, содержащих палочкообразные макромолекулы, должно соблюдаться соотношение
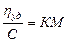

Удельная вязкость прямо пропорциональна концентрации и молекулярной массе полимера; К определяют независимым методом, например, по растворам полимеров с известной молекулярной массой М. Она зависит от данного гомологического ряда и растворителя; С – массовая концентрация полимера.
Уравнение справедливо лишь для полимеров с короткими жесткими цепями, которые могут сохранять палочкообразную форму. Гибкие молекулы с длинными цепями, обычно свертываются в клубок, что уменьшает сопротивление движению. При этом К изменяется и зависимость становится нелинейной.
Широкое распространение для определения молекулярной массы полимера с гибкими и длинными макромолекулами получило уравнение Марка-Куна-Хаувинка:
где К и а – постоянные для данного гомологического ряда и растворителя.
Из уравнения (9.6) видно, что, по мере увеличения концентрации дисперсной фазы линейная зависимость h — Vобнарушается в условиях взаимного столкновения частиц, однако при данной концентрации вязкость остается постоянной. Подобные системы, подчиняющиеся уравнениям Ньютона, Пуазейля и Эйнштейна, называются нормальными или ньютоновскuми.
Для структурированных систем наблюдается отклонение от теоретической зависимости уже при малых концентрациях (рис. 9.8, кривая 2). Они не подчиняются законам Ньютона, Пуазейля и Энштейна и называются аномальными или неньютоновскими.
В данном случае связывают с молекулярной массой полимера характеристическую вязкость [h], так как именно этой величиной оценивается прирост вязкости раствора, вызванный наличием макрочастиц и их вращением
Для разбавленных растворов, полимеров широко используется зависимость удельной вязкости от концентрации.

включающая константу К / , которая характеризует взаимодействие полимера с растворителем. Чем хуже растворитель, тем выше значения К / . Формула удобна для экстраполяции [h] при бесконечном разбавлении.
[h]- характеристическая вязкость, она оценивает прирост вязкости раствора, вызванный наличием макрочастиц и их вращений.

Три наиболее распространенных метода измерения вязкости:
http://helpiks.org/4-72392.html
http://lektsii.org/13-73840.html