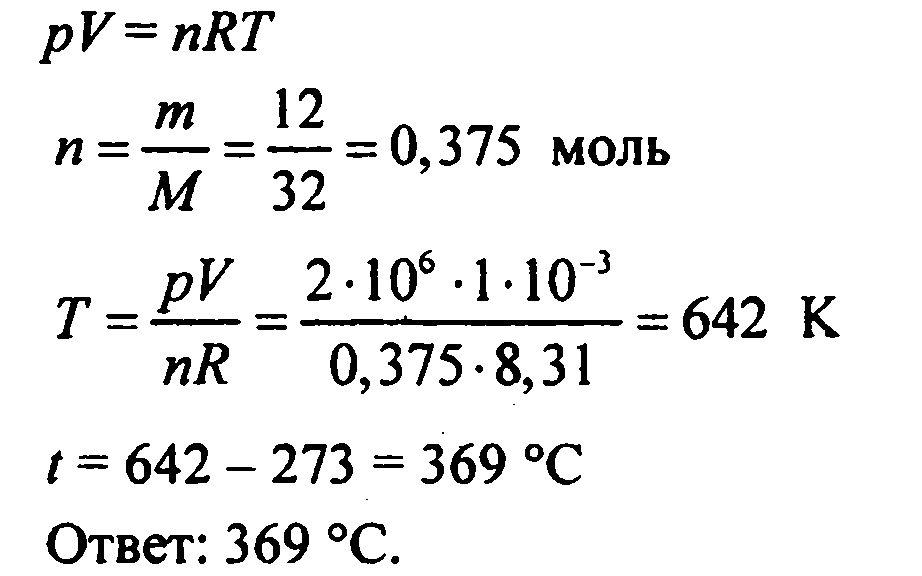Придумать задачу на уравнение менделеева клапейрона
Репетитор
по физике
Репетитор
по алгебре
\( P \) — Давление газа (Паскали)
\( \nu \) — Количество вещества
\( R \) — Универсальная газовая посиоянная
\( T \) — Температура в Кельвинах
В баллоне находится газ под давлением \(P= 8,31 \cdot 10^6 \; Па \), температура газа \(T=300 К \).
Количество вещества газа \( \nu=100 Моль \).
Найти объем баллона
Универсальная газовая постоянная \( R=8,31 \frac<Дж> <Моль \cdot K>\)
Дать ответ в литрах.
Показать ответ Показать решение Видеорешение
Запишем уравнение Менделеева-Клапейрона :
Алгоритм решения задач на уравнение Менделеева — Клайперона
Разделы: Физика
Алгоритм решения задач на применение уравнения Менделеева Клайперона.
Многократное (до 7 и более раз) воспроизведение учащимися логически выверенных строго последовательных пошаговых действий дает возможность глубоко и прочно усвоить учебный материал. Представленный алгоритм апробирован. Он позволяет:
1) научить использовать уравнение МенделееваКлайперона (его варианты);
2) продолжить формирование навыков работы в международной системе единиц “СИ” и культуры оформления решения задач;
3) осуществляет межпредметную связь с алгеброй и химией;
4) воспитывает точность, аккуратность, пунктуальность.
| № шага | Алгоритм | Выполнение |
| 1 | Внимательно прочитайте текст задачи. | Баллон содержит 50 л кислорода, температура которого 27° С, а давление 2МПа. Найдите массу кислорода. |
| 2 | Запишите в “Дано” буквенное обозначение и числовое значение известных по тексту физических величин. Необходимо знать нормальные условия: р=10 5 Па, t°=0° С | Дано: p=2 МПа |
| 3 | Запишите химическую формулу и молярную массу газообразного вещества в “ Дано”, используя систему СИ. М Воздух= 0,029 кг/моль. | О2 М=32•10 3 кг/моль |
| 4 | Под горизонтальной чертой запишите буквенное обозначение неизвестной величины, знак = и? | m= ? |
| 5 | Под словом “ Решение” напишите уравнение МенделееваКлайперона или его вариант: | |
| 6 | Проделайте алгебраические преобразования так, чтобы по одну сторону знака = стояла неизвестная величина, а по другую все известные. | |
| 7 | Проверьте, все ли величины выражены в системе СИ, учитывая, что 1л= 10 3 м 3 , Т=t° +273 , 1 мм рт. ст.= 133 Па | 50 л = 5• 10 2 м 3 Т = 300 К |
| 8 | Подставьте числовые значения вместе с единицами измерения, проведите расчет и работу с единицами измерения, учитывая, что 1 Дж=1 Н? м, 1 Па=1Н/м 2 , 1 Н=1кг? м/с 2 |  |
| 9 | Запишите ответ: | Ответ: m=1,3 кг |
Задачи для закрепления:
1) Определите массу водорода, находящегося в баллоне емкостью 20 л при давлении 830 кПа, если температура газа равна 17° С.
2) Сосуд вместимостью 40 л содержит 1,98 кг углекислого газа и выдерживает давление не выше 3 МПа. При какой температуре возникает опасность взрыва?
3) Определите плотность азота при нормальных условиях.
4) Какое количество вещества содержится в газе при давлении 200 кПа и температуре 240 К, если его объем 40 л?
5) Какой объем занимает воздух массой 2,9 кг при давлении 750 мм рт.ст. и температуре 3° С?
6) Каково давление азота в сосуде объемом 0,25 м 3 при температуре 32° С? Масса газа 300 г.
Таблицу алгоритма и примеры решения задач на закрепление учитель, исходя из методических потребностей, может размещать как на одной, так и на разных сторонах листа формата А4, раздать ученикам для использования на уроке и дома.
1) 0,014 г;
2) 48° С;
3) 1,23 кг/м 3 ;
4) 4 моль;
5) 2,25 м 3 ;
6) 108624 Па.
Помогите придумать задачку 6 § 8 Химия Габриелян 11 класс
Запишите уравнение Менделеева—Клапейрона. Придумайте задачу на его применение и решите её.
Уравнение состояния идеального газа (Менделеева-
Клапейрона) pV = nRT, где р — давление газа (Па), V — его
объем (м 3 ), Т — абсолютная температура (К), n — число мо-
лей газа, R — универсальная газовая постоянная, равная
8,314 Дж/К*моль (R = 0,08206 л*атм/К*моль, если р измеряют
в атмосферах, V — в литрах, n — в молях, Т — в кельвинах).
Расcчитайте температуру 12 г газа с молярной массой
32 г/моль, если он занимает объем 1 л и находится под давлением 2 · 10 6 Па.
http://urok.1sept.ru/articles/103258
http://class.rambler.ru/temy-himiya/pomogite-pridumat-zadachku-6-8-himiya-gabrielyan-11-klass-6964.htm