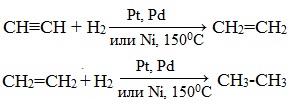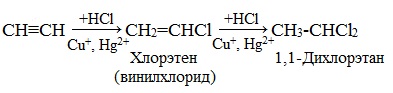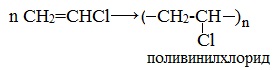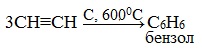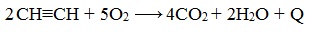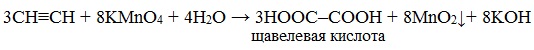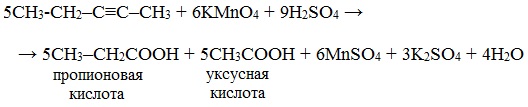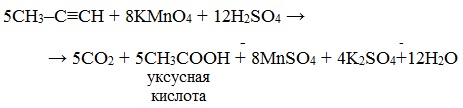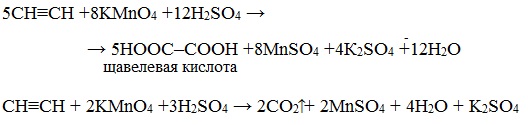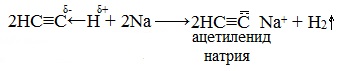Гидратация алкинов по Кучерову
Вы будете перенаправлены на Автор24
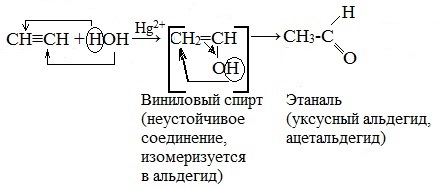
Алкины при наличии катализаторов присоединяют воду и образуют карбонильные соединения. Промышленное значение приобрела реакция гидратации ацетилена, открытая в 1881 г. М. Г. Кучеровым, который установил, что присоединение воды к ацетилену происходит в среде 10%-го раствора $H_2SO_4$ при наличии 5% сульфата ртути. Продуктом реакции является уксусный альдегид:
Механизм гидратации ацетилена
Гидратацию ацетилена называют реакцией Кучерова. Механизм этой реакции еще не полностью выяснен. Считают, что сначала к тройной углерод-углеродной связи присоединяется катализатор и образует с ним продукт присоединения (І). Продукт (І) далее гидролизуется в енол — неустойчивый виниловый спирт (II), который сразу же изомеризуется (таутомеризуеться) в термодинамически устойчивое соединение (в карбонильную форму) — уксусный альдегид (III):
Установлено, что кроме солей ртути гидратацию алкинов катализируют соли трехвалентного золота, одновалентной меди, одновалентного серебра и трехвалентного рутения. Механизм реакций Кучерова достаточно сложен, до конца не изучен и содержит еще много неясных моментов. В частности, неясна роль ионов металлов (йонов ртути в классической реакции) и путь образования винил-катионов в качестве промежуточных частиц.
Енолы
Органические соединения, в молекулах которых $OH$-группа соединена с атомом углерода с двойной связью, как например, в виниловом спирте (II), называют енолами («ен-» означает наличие в молекуле двойной $C = C$-связи, «-ол» — означает $OH$-группы спирта).
А. П. Эльтеков в 1877 сформулировал правило, согласно которому ненасыщенные спирты с группой -$OH$ у атома углерода с двойной связью являются неустойчивыми и самовольно изомеризуются в устойчивые карбонильные соединения. Это правило выполняется преимущественно для простых енольных систем.
Готовые работы на аналогичную тему
Исследования химиков показали, что всегда при извлечении соединения с енольной структурой получают изомерные ей соединения с карбонильной структурой. Между енольной и карбонильной структурами существует равновесие:
Такая перегруппировка енольной структуры в карбонильную происходит особенно легко и поэтому равновесие этого процесса сильно смещено в сторону карбонильной структуры. Причина такой изомеризации заключается в том, что вследствие высокой полярности связи $O-H$ атом водорода этой группы енола может легко отщеплятся от атома кислорода в виде иона. При обратном присоединении этот ион водорода может присоединятся как к атому кислорода, так и к атому углерода с двойной связью. Если $H^+$ присоединится к кислороду, то очень легко сможет снова отщепиться. Если этот ион присоединится к углероду, то уже останется соединенным с ним, поскольку полярность связи $C-H$ достаточно мала. В результате происходит перегруппировка, при которой сильная кислота превращается в значительно более слабую:
Структурные изомеры, между которыми существует равновесие, называют таутомерами, а явление существования такой изомерии называют таутомерия.
Гидратация гомологов ацетилена
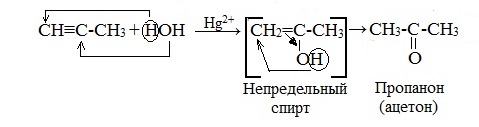
Гидратация гомологов ацетилена приводит к образованию кетонов. Присоединение воды к алкинам-1 происходит по правилу Марковникова. Например, при гидратации пропина образуется диметилкетон (ацетон):
Из терминальных алкинов $R-CHC-H$ при гидратации получают почти всегда метилкетоны $R-CO-CH_3$, а из двцзамещенныих $R»-CH_2-R’$ ($R»$ и $R’$ — различные по строению алкильные группы) — кетоны, образование которых подчиняется такой такой тенденции: для первичного $R$ ($CH_3$- или $CH_3-CH_2-$) и вторичного или третичного $R$ ($-CH(CH_3)_2$ или $-C(CH_3)_3$) карбонильная группа $C =O$ образуется в основном в $\alpha$-положении к вторичному или третичному атому углерода алкиле $R$. Так, при гидратации метилизопропилацетилена в реакционной смеси будет преобладать етилизопропилкетон по сравнению изобутилметилкетоном:
Катализируемые кислотами и ионами ртути (II) реакции присоединения воды по месту тройной связи алкинов протекает строго по правилу Марковникова. Следовательно, гидратация как терминальноых, так и нетерминальных алкинов всегда приводит к кетонам, например для циклических и линейных алкинов:
Присоединение воды к ацетилену уравнение реакции
Алкины во многих реакциях обладают большей реакционной способностью, чем алкены. Для алкинов, как и для алкенов, характерны реакции присоединения. Так как тройная связь содержит две π-связи, реакции присоединения к алкинам могут происходить в две стадии.
Вначале идет присоединение по месту двойной π-связи с образование производных олефинов, а затем по месту второй π-связи с образованием производных алканов.
Реакции присоединения для алкинов протекают медленнее, чем для алкенов. Это объясняется тем, что π-электронная плотность тройной связи расположена более компактно, чем в алкенах, и поэтому менее доступна для взаимодействия с различными реагентами.
Реакции присоединения
1. Гидрирование
Присоединение водорода происходит при нагревании в присутствии металлических катализаторов. Реакция протекает в две стадии: алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем образованием алканов (разрывается вторая π-связь):
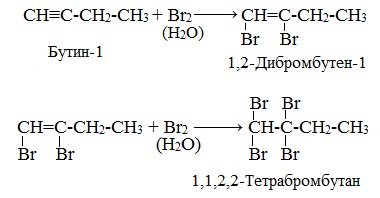
2. Галогенирование
Присоединение галогенов протекает также в две стадии. На первой стадии образуются дигалогеналкены, на второй – тетрагалогеналканы:
Реакция алкинов с бромной водой является качественной реакцией на алкины. Бромная вода обесцвечивается.
Видеоопыт «Взаимодействие ацетилена с бромной водой»
Видеоопыт «Взаимодействие ацетилена с хлором»
3. Гидрогалогенирование
Галогеноводороды присоединяются к алкинам в две стадии. Вторая стадия идет по правилу Марковникова. Присоединение НCl в отсутствии катализатора идет очень медленно. Катализатором этой реакции служат кислоты Льюиса – соли меди (I) и ртути (II):
Получаемый продукт – хлористый винил (винилхлорид) – подобно этилену легко полимеризуется, образуя полимер – поливинилхлорид, который широко применяется в производстве поливинилхлоридных смол:
4. Гидратация (реакция Кучерова)
Присоединение воды протекает в присутствии солей ртути (II) при нагревании – HgSO4, Hg (NO3)2 – с образованием уксусного альдегида (при обычных условиях ацетилен с водой не взаимодействует):
На первой стадии реакции образуется непредельный спирт, в котором гидроксильная группа находится непосредственно у атома углерода при двойной связи. Такие спирты принято назвать виниловыми или енолами.
Отличительной чертой енолов является их неустойчивость. В момент образования они изомеризуются в более стабильные карбонильные соединения (альдегиды или кетоны) — водород гидроксильной группы переходит к соседнему атому углероду. При этом π-связь между атомами углерода разрывается и образуется π-связь между атомом углерода и атомом кислорода. Причиной изомеризации является большая прочность двойной связи С=О по сравнению с двойной связью С=С.
Гидратация гомологов ацетилена протекает по правилу Марковникова, и образующиеся енолы изомеризуются в кетоны:
5. Реакции полимеризации
В присутствии катализаторов алкины могут реагировать друг с другом, причем в зависимости от условий образуются различные продукты.
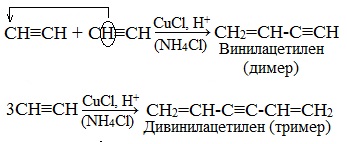
1.Димеризация под действием водно-аммиачного раствора CuCl:
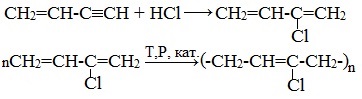
Винилацетилен обладает большой реакционной способностью – присоединяя хлороводород, он образует хлоропрен (2-хлорбутадиен-1,3), используемый для получения искусственного хлорпренового каучука:
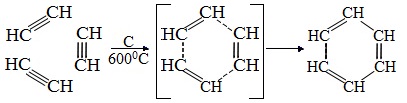
2.Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского):
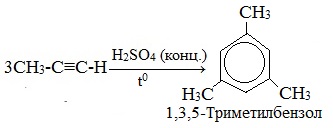
В аналогичные реакции тримеризации могут вступать также и ближайшие гомологи ацетилена, например пропин:
1. Горение
При сгорании алкинов происходит их полное окисление до СО2 и Н2О. Горение ацетилена сопровождается выделением большого количества тепла:
Температура ацетиленово-кислородного пламени достигает 2800- 3000°С. На этом основано применение ацетилена для сварки и резки металла. Ацетилен образует с воздухом и кислородом взрывоопасные смеси.
Видеоопыт «Взрыв смеси ацетилена с кислородом»
В сжатом, и особенно в сжиженном, состоянии он способен взрываться от удара. Поэтому ацетилен хранится в стальных баллонах в виде растворов в ацетоне, которым пропитывают асбест.
2. Неполное окисление
Ацетилен и его гомологи легко окисляются окислителями — КMnO4, K2Cr2O7. Алкины окисляются с разрывом молекулы по тройной связи. Строение продуктов окисления зависит от природы окислителя и условий проведения реакций.
Алкины обесцвечивают разбавленный раствор перманганата калия, что доказывает их ненасыщенность.
а) мягкое окисление
Мягкое окисление алкинов происходит без разрыва σ-связи С─С (разрушаются только π-связи).
Например, при взаимодействии ацетилена с разбавленным раствором КMnO4 при комнатной температуре образуется двухосновная щавелевая кислота:
В нейтральной и слабощелочной средах на холоде образуются соли карбоновых кислот. При взаимодействии ацетилена с водным раствором перманганата калия образуется соль щавелевой кислоты (оксалат калия):
б) Жесткое окисление
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты.
Окисление алкинов перманганатом калия в кислой среде при нагревании сопровождается разрывом углеродной цепи по месту тройной связи и приводит к образования карбоновых кислот:
Окисление алкинов, содержащих тройную связь у крайнего атома углерода, сопровождается в этих же условиях образованием карбоновой кислоты и выделением углекислого газа:
В кислой среде окисление ацетилена идет до щавелевой кислоты или углекислого газа:
Видеоопыт «Взаимодействие ацетилена с раствором перманганата калия»
Реакция КMnO4 является качественной реакцией на алкины. Раствор перманганата калия обесцвечивается.
Образование солей
Особенностью алкинов, имеющих концевую тройную связь (алкины-1), является их способность проявлять слабые кислотные свойства.
Атомы водорода, связанные с sp-гибридизированными атомами углерода в молекулах алкинов, обладают значительной подвижностью, что объясняется поляризацией σ-связи ≡С─Н. В связи с этим атомы водорода могут замещаться атомами металлов, в результате чего образуются соли — ацетилениды.
Ацетилениды щелочных и щелочноземельных металлов используются для получения гомологов ацетилена.
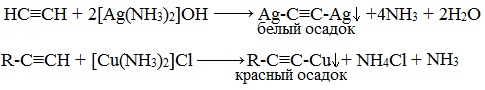
Ацетилениды серебра и меди (I) легко образуются и выпадают в осадок при пропускании ацетилена через аммиачный раствор оксида серебра или хлорида меди (I).
Образование серовато- белого осадка ацетиленида серебра (или красно-коричневого – ацетиленида меди) служит качественной реакцией на концевую тройную связь.
Видеоопыт «Получение ацетиленида серебра»
Видеоопыт «Получение ацетиленида меди»
Ацетилениды серебра и меди как соли слабых очень кислот легко разлагаются при действии хлороводородной кислоты с выделением исходного алкина.
Ацетилиниды серебра и меди в сухом виде взрываются от удара. Однако карбид кальция, который также является ацетиленидом, очень устойчив к удару. Он широко используется для получения ацетилена.
Если тройная связь находится не на конце цепи, то кислотные свойства отсутствуют (нет подвижного атома водорода) и ацетилениды не образуются.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://himija-online.ru/organicheskaya-ximiya/alkiny/ximicheskie-svojstva-alkinov.html http://acetyl.ru/o/a21d2d.php |