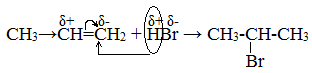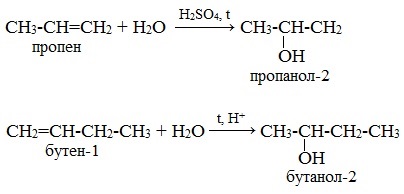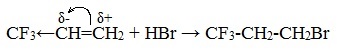Приведите уравнение химической реакции демонстрирующее правило марковникова
Правило Марковникова — при присоединении галогеноводородов или воды к несимметричным алкенам или алкинам атом водорода присоединяется к наиболее гидрогенизированному (гидрированному) углеродному атому (т.е. к атому С, связанному с большим числом атомов Н), а атом галогена (или группа –ОН) – к наименее гидрогенизированному.
Правило, устанавливающее направление реакции присоединения галогеноводородов (гидрогалогенирование) и воды (гидратация), сформулировал русский химик В.В. Марковников в 1869 г.
Правило Марковникова о присоединении по двойной связи объясняется смещением электронной плотности в молекулах несимметричных алкенов.
Механизм присоединения по правилу Марковникова
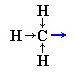
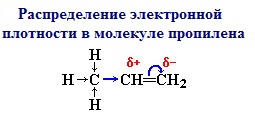
Электронная плотность в молекуле СН3-СН=СН2 до вступления в реакцию распределена неравномерно. Это обусловлено тем, что метильная группа СН3 за счет суммирования небольшой полярности трех С-Н-связей является донором электронов, т.е. проявляет +I-эффект ссылка по отношению к соседним атомам углерода.
Это вызывает смещение подвижности π-электронов двойной связи в сторону более гидрогенизированного атома углерода и появлению на нем частичного отрицательного заряда (δ-).
На другом, менее гидрогенизированном, атоме углерода возникает частичный положительный заряд (δ+). Поэтому атака электрофильной частицы Н+ происходит по более гидрогенизированному углеродному атому, а атом галогена или группа –ОН присоединяются к менее гидрогенизированному атому углерода.
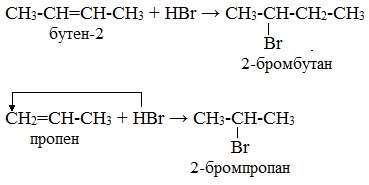
Например, гидробромирование бутена-2 и пропена:
Бутен-2 является симметричным алкеном, оба углеродных атома относительно двойной связи совершенно равноценны. В результате первой реакции образуется один продукт – 2-бромбутан.
Пропен – несимметричный алкен. Один углеродный атом при двойной связи более гидрогенизирован, т.е. содержит большее число атомов водорода. Поэтому продуктом реакции является 2-бромпропан.
Присоединение воды к несимметричным алкенам также происходит по правилу Марковникова.
Например, гидратация пропена и бутена-1:
В результате гидратации пропена образуется пропанол-2, а не пропанол-1. А в результате гидратации бутена-1 – бутанол-2, а не бутанол-1.
Если же в алкене присутствует электроноакцепторный заместитель, т.е. группа, обладающая способностью оттягивать на себя электронную плотность, более стабильным может оказаться первичный катион и реакция пойдет против правила Марковникова, например гидрогалогенирование трифторпропена.
Правило Марковникова — формулировка и примеры использования в химии
Правило Марковникова в химии имеет большое значение в случаях взаимодействия воды или протонных кислот с такими органическими веществами как алкены и алкины. Примером может служить уравнение реакции: пропен + вода.
Суть этого правила в направлении разных типов реакций в зависимости от химического строения с участием реагентов, в структуре которых есть двойная связь. За этим правилом могут протекать реакции присоединения, отщепления, замещения, а также — реакции изомеризации.
Кратко о жизни и деятельности ученого-органика Марковникова
Ученый Владимир Васильевич Марковников занимался исследованиями в таких отраслях как органический синтез, нефтехимия и теоретическая органическая химия.
Марковников Владимир Васильевич (1838-1904)
В период с 1862 по 1867 гг. он смог пополнить багаж знаний человечества об изомерах спиртов и жирных кислот, открыть в ряду олефиновых углеродов оксиды, в первый раз в истории синтезировать оксо- и галогенопроизводные изомеры масляной кислоты.
На основании знаний, полученных в результате этих исследований, учёный смог сформулировать новое учение про взаимное влияние атомов, которое впоследствии получило имя автора. Сделал он это в 1869 г.
Современная формулировка правила Марковникова
Механизм реакции взаимодействия электрофильных реагентов с молекулами органических веществ, в которых есть двойная связь (электрофильное присоединение), происходит с образованием наиболее устойчивых карбокатионов.
Но если в строении алкена есть неконцевая двойная связь, то в этом случае будет иметь место правило Зайцева.
В соответствии с ним — тогда будет менее выражена ориентация присоединения.
Механизм электрофильного присоединения
Направление реакций этого типа происходит благодаря такому явлению как электронный эффект. То есть, благодаря смещению электронной плотности в молекуле.
На первой стадии образуется комплекс в результате взаимодействия электронов двойной связи с электрофильной частицей (чаще всего это ион водорода).
Вторая стадия — стадия гетеролитического разрыва связи — характеризуется образованием ковалентной связи между одним из атомов углерода и электрофильной частицей, в итоге образуется карбокатион.
На третьей стадии происходит образование второй связи за счёт второй электронной пары аниона (карбокатион реагирует с анионом).
Простыми словами, общая схема действия этого правила заключается в том, что присоединение иона водорода происходит к тому атому углерода (он обязательно должен находится возле двойной связи), который заряжен более отрицательно.
Исключение из правила
Вопреки правилу протекают реакции, в которых заместителем, стоящим при двойной связи, производится оттягивание электронной плотности в свою сторону. Этим осуществляется проявление электроноакцепторных свойств.
Пример такой реакции есть взаимодействие хлороводорода с 3,3,3-трихлорпропеном.
Вторым случаем, когда реакция присоединения происходит против этого правила, есть протекание реакций за радикальным механизмом (в реакции присутствуют атакующие свободные радикалы).
Примером может служить присоединение олефинов к бромоводороду. В таких реакциях происходит гомолитический разрыв связи.
Где применяется правило Марковникова
Правило нашло своё применение:
В производстве различных смесей, использующихся как на производствах, так и в быту. Например, оно применяется в изготовлении химического сырья, топлива и каучука.
Также его применяют для упрощения производства масел для смазки, спирта и полимеров.
Кроме всего вышеперечисленного, правило используется для изготовления смесей, входящих в состав горючего для бензинных двигателей самолетов и автомобилей, и для производства сажи, из которой потом делается топографическая краска.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://kupuk.net/uroki/himiya/pravilo-markovnikova-formylirovka-i-primery-ispolzovaniia-v-himii/ http://acetyl.ru/f/r901.php |