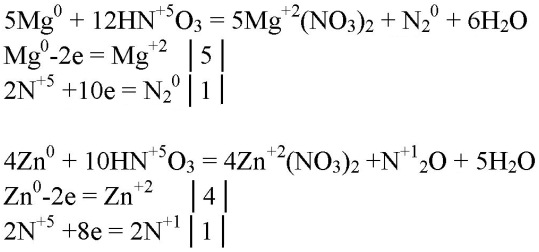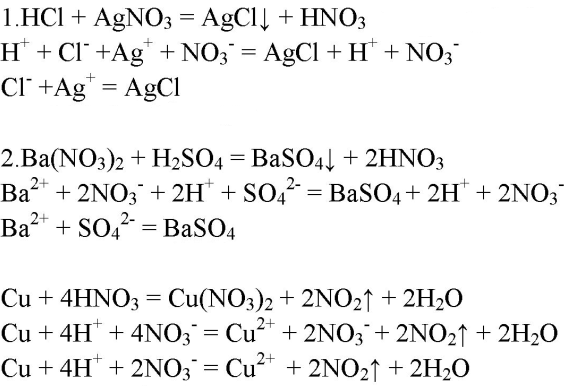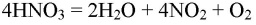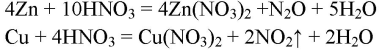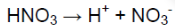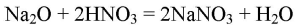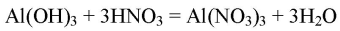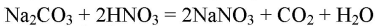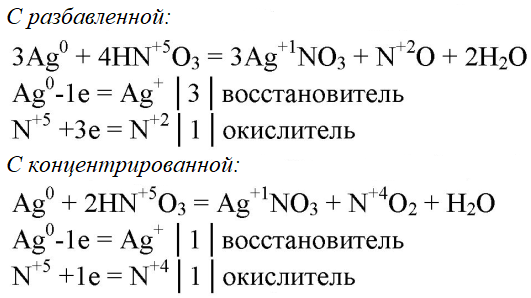Задание 4
Приведите уравнения реакций: а) характерных только для азотной кислоты; б) общих для азотной и других кислот.
Уравнения реакций характерные только для азотной кислоты
При нагревании и под действием света концентрированная азотная кислота разлагается:
4HNO3 t, свет ⟶ 2H2O + 4NO2↑ + O2↑
Азотная кислота по-разному реагирует с металлами. В этих реакциях в зависимости от концентрации кислоты и восстановительной способности металла выделяются различные оксиды азота, иногда азот и даже аммиак:
Cu + 4HNO3(конц.) ⟶ Cu(NO3)2 + 2NO2↑ + 2H2O
3Cu + 8HNO3(разб.) ⟶ 3Cu(NO3)2 + 2NO↑ + 4H2O
Уравнения реакций общих для азотной и других кислот
Азотная кислота является сильной кислотой, поэтому она диссоциирует полностью:
HNO3 ⟶ H + + NO3 —
Реагирует с основными оксидами:
CuO + 2HNO3 ⟶ Cu(NO3)2 + H2O
Реагирует с основаниями:
NaOH + HNO3 ⟶ NaNO3 + H2O
Реагирует с солями более слабых и более летучих кислот:
Na2CO3 + 2HNO3 ⟶ 2NaNO3 + H2O + CO2↑
Приведите уравнения реакций: а) характерные только для азотной кислоты; б) общие для азотной и других кислот.
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,299
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,256
- разное 16,836
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Вопросы к параграфу 27 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 27. Азотная кислота
Вопросы и задания
1. Объясните, почему азотную кислоту относят к кислотам-окислителям. Какие ещё кислоты-окислители вам известны? Можно ли отнести к подобным кислотам соляную кислоту? Обсудите этот вопрос с соседом по парте.
Азотная кислота — кислота-окислитель, потому что она имеет наивысшую степень окисления азота +5. Поэтому атом азота легко принимает электроны и восстанавливается до степени окисления +4, +3, +2, +1, 0, -3.
Другие кислоты-окислители: H2SO4, HClO4, H2Cr2O7.
Соляная кислота имеет наименьшую отрицательную степень окисления хлора -1. Он не может принимать электроны и быть окислителем.
2. При взаимодействии разбавленной азотной кислоты с некоторыми металлами (Mg, Zn) может выделиться оксид азота(I) или азот. Напишите соответствующие уравнения окислительно-восстановительных реакций.
3. Напишите молекулярные, полные ионные и сокращённые ионные уравнения реакций, с помощью которых можно различить соляную, серную и азотную кислоты.
4. Приведите уравнения реакций: а) характерных только для азотной кислоты; б) общих для азотной и других кислот.
Характерные только для азотной кислоты
Общие для азотной кислоты и других кислот
Разлагается при нагревании и под действием света
По-разному реагирует с металлами
В результате реакции концентрированной азотной кислоты с белками образуются вещества ярко-жёлтого цвета.
Взаимодействует с основными оксидами
Взаимодействует с основаниями
Взаимодействует с солями более слабых и летучих кислот
5. Напишите уравнения реакций, протекающих между серебром и разбавленной, а также концентрированной азотной кислотой. Покажите переход электронов и подчеркните окислитель одной чертой, а восстановитель двумя.
6. Используя рисунок 26, подготовьте компьютерную презентацию на тему «Применение азотной кислоты».
При приготовлении презентации можно использовать следующую информацию:
Азотную кислоту применяют:
- В сельском хозяйстве (для изготовления аммиачной селитры — удобрения);
- В промышленности (изготовление взрывчатых веществ, синтетических красителей, искусственных волокон, пластических масс, в цветной металлургии);
- В медицине (изготовление некоторых лекарств, применяется азотная кислота для борьбы с заболеваниями кожи и ЖКТ, применение нитроглицерина людьми с сердечной недостаточностью);
- В полиграфии (травление печатных форм);
- В ювелирном деле (определение золота в золотом сплаве).
http://www.soloby.ru/301414/%D0%BF%D1%80%D0%B8%D0%B2%D0%B5%D0%B4%D0%B8%D1%82%D0%B5-%D1%83%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F-%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B9-%D1%85%D0%B0%D1%80%D0%B0%D0%BA%D1%82%D0%B5%D1%80%D0%BD%D1%8B%D0%B5-%D0%B0%D0%B7%D0%BE%D1%82%D0%BD%D0%BE%D0%B9-%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D1%8B
http://gdzwow.com/answers/9-himiya-uch-rudzitis-vopr-k-par-27.html