).
Продолжите уравнения реакций и уравняйте их. Стрелками укажите продукты, выпадающие
в осадок или выделяющиеся в виде газа.
3AgNO3+FeCl3=3AgCl(осадок)+Fe(NO3)3
Pb(NO3)2+K2S=PbS(осадок)+2KNO3
3Ba(NO3)2+Al2(SO4)3=
=3BaSO4(осадок)+2Al(NO3)3
Na2S+2HCl=2NaCl+H2S
(NH4)2SO4+KOH=реакция не идёт
K2CO3+H2SO4=K2SO4+H2O+CO2(газ)
Ba(HCO3)2+H2SO4=
=BaSO4(осадок)+2H2O+2CO2
SiO2+2NaOH=H2O+Na2SiO3
MgO+HBr=MgBr2+H2O
Если ответ по предмету Химия отсутствует или он оказался неправильным, то попробуй воспользоваться поиском других ответов во всей базе сайта.
Частные реакции катионов второй аналитической группы
Реакции катиона свинца Pb 2+
1. Хлороводородная кислота HCl и растворимые хлориды осаждают из умеренно концентрированных растворов солей свинца (II) белый хлопьевидный осадок хлорида свинца (II), легко растворимый в горячей воде:
Pb(NO3)2 + 2HCl 
Pb 2+ + 2Cl — 
Выполнение реакции. В пробирку помещают 2 капли раствора нитрата свинца (II) Pb(NO3)2 и добавляют 2 капли хлороводородной кислоты. К раствору с осадком добавляют 0,5 мл дистиллированной воды и нагревают смесь на водяной бане. Наблюдают растворение осадка и постепенное его выпадение при охлаждении раствора.
2. Едкие щелочи из растворов солей свинца (II) осаждают гидроксид свинца (II) – осадок белого цвета:
Pb(NO3)2 + 2KOH 
Pb 2+ + 2OH — 
Гидроксид свинца (II) обладает амфотерными свойствами, поэтому он растворяется в разбавленной азотной или уксусной кислотах и в избытке щелочи:
Pb(OH)2 + 2KOH 
Выполнение реакции. К 2 каплям соли свинца (II) прибавляют сначала 1 каплю раствора щелочи, а затем ее избыток и наблюдают выпадение осадка и последующее его растворение в избытке щелочи.
3. Серная кислота H2SO4 и растворимые сульфаты выделяют из свинцовых солей труднорастворимый сульфат свинца – осадок белого цвета:
Pb(NO3)2 + H2SO4 
Pb 2+ + SO4 2- 
Осадок растворим при нагревании в растворах щелочей (10-15%):
PbSO4 + 4NaOH 
Выполнение реакции. К 2 каплям раствора соли свинца (II) прибавляют 2 капли разбавленной серной кислоты и наблюдают выпадение осадка.
4. Иодид калия KI, взаимодействуя со свинцовыми солями, дает желтый осадок иодида свинца (II):
Pb(NO3)2 + KI 
Pb 2+ + 2I — 
Реакция часто применяется для открытия ионов Pb 2+ .
Выполнение реакции. К 2 каплям раствора нитрата свинца (II) Pb(NO3)2 добавляют 2 капли раствора иодида калия. В полученный раствор с осадком добавляют 0,5 мл воды и 3-4 капли разбавленной уксусной кислоты; нагревают смесь на кипящей водяной бане в течение 2 мин, затем охлаждают содержимое пробирки под струей воды. Растворившийся при нагревании осадок иодида свинца вновь выпадает в виде красивых золотистых чешуек.
5. Хромат калия K2CrO4 или хромат натрия Na2CrO4 выделяет из раствора соли свинца желтый осадок соли свинца (II):
Pb(NO3)2 + K2CrO4 
Pb 2+ + CrO4 2- 
Осадок не растворяется в уксусной кислоте, но растворяется в азотной кислоте и щелочах. Реакция чувствительна и является характерной для ионов Pb 2+ .
Выполнение реакции. К 2 каплям раствора соли свинца (II) добавляют 2 капли раствора хромата калия и наблюдают выпадение осадка.
Реакции катиона серебра Ag +
1. Хлороводородная кислота HCl и растворимые хлориды осаждают из нейтральных и кислых растворов солей серебра в виде белого творожистого осадка хлорида серебра:
AgNO3 + HCl 
Ag + + Cl — 
Осадок легко растворяется в избытке аммиака с образованием комплексной соли:
AgCl + 2 NH3 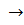
При подкислении аммиачного раствора концентрированной азотной кислотой эта соль разрушается и вновь выпадает осадок хлорида серебра:
[Ag(NH3)2]Cl + 2HNO3 
Эту реакцию обычно используют для открытия иона Ag + . Она является фармакопейной.
Выполнение реакции. В пробирку помещают 2 капли раствора нитрата серебра, добавляют к нему 2 капли разбавленной хлороводородной кислоты. К раствору с осадком добавляют 5 капель концентрированного раствора аммиака и встряхивают смесь до растворения осадка. К полученному раствору добавляют 6 капель концентрированной азотной кислоты. Наблюдают выпадение осадка.
2. Иодид калия KI образует с ионом Ag + светло-желтый осадок AgI:
AgNO3 + KI 
Ag + + l — 
Иодид серебра не растворяется в растворе аммиака в отличие от хлорида серебра.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли иодида калия и наблюдают выпадение осадка.
3. Хромат калия K2CrO4 из растворов солей серебра осаждает кирпично-красный хромат серебра:
2AgNO3 + K2CrO4 
2Ag + + CrO4 2- 
Осадок растворяется в растворе аммиака и азотной кислоте.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли раствора хромата калия и наблюдают выпадение осадка.
4. Едкие щелочи из растворов солей серебра осаждают грязно-коричневый осадок оксида серебра:
2AgNO3 + 2KOH 
2Ag + + 2OH — 
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 2 капли раствора щелочи и наблюдают выпадение осадка.
5. Тиосульфат натрия Na2S2O3 из растворов солей серебра выделяет белый осадок, который быстро желтеет, затем буреет и переходит в черный:
2AgNO3 + Na2S2O3 
Ag2 S2O3 + H2O 
Осадок Ag2 S2O3 растворяется в избытке тиосульфата с образованием комплексных солей, поэтому осадок образуется при избытке ионов серебра. Реакция является фармакопейной.
Выполнение реакции. К 2 каплям раствора нитрата серебра добавляют 1 каплю раствора тиосульфата натрия. Наблюдается изменение цвета осадка.
Реакции катиона ртути (I) Hg2 2+
1. Хлороводородная кислота HCl и растворимые хлориды из растворов солей ртути (I) осаждают хлорид ртути (I), или каломель, — осадок белого цвета:
Hg2(NO3)2 + HCl 
Hg2 2+ +2Cl — 
Водный раствор аммиака окрашивает осадок в черный цвет, обусловленный образованием черной мелкораздробленной ртути:
Hg2Cl2 + 2 NH3 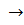
С помощью этой реакции открывают ион Hg2 2+ .
Выполнение реакции. К 2 каплям раствора нитрата ртути (I) Hg2(NO3)2 добавляют 2 капли раствора разбавленной хлороводородной кислоты. К раствору с осадком добавляют 3 капли раствора аммиака. Наблюдают почернение осадка.
2. Иодид калия KI из растворов солей ртути (I) осаждает иодид ртути (I) – осадок болотно-зеленого цвета:
Hg2(NO3)2 + 2KI 
Осадок довольно легко распадается на иодид ртути (II) и металлическую ртуть; при этом цвет осадка изменяется:
Hg2I2 
Выполнение реакции. К 2 каплям раствора нитрата ртути (I) Hg2(NO3)2 добавляют 2 капли раствора иодида калия. Наблюдают выпадение осадка и изменение его цвета при встряхивании.
3. Хромат калия K2CrO4 
Hg2(NO3)2 + K2CrO4 
2Hg + + CrO4 2- 
Осадок не растворяется в щелочах и разбавленной уксусной кислоте.
Выполнение реакции. 2 капли раствора Hg2(NO3)2 , помещенные в пробирку, нагревают на водяной бане и добавляют 2 капли хромата калия.
http://zdamsam.ru/b4833.html
