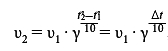Урок 14. Расчеты по уравнениям химических реакций
В уроке 14 «Расчеты по уравнениям химических реакций» из курса «Химия для чайников» мы научимся решать задачи, используя уравнения химических реакций.
Вещества вступают в химические реакции в определенных массовых и количественных соотношениях. Следовательно, при проведении реакций в лабораториях и на химических заводах расходуются определенные массы исходных веществ для получения заданной массы продуктов реакции.
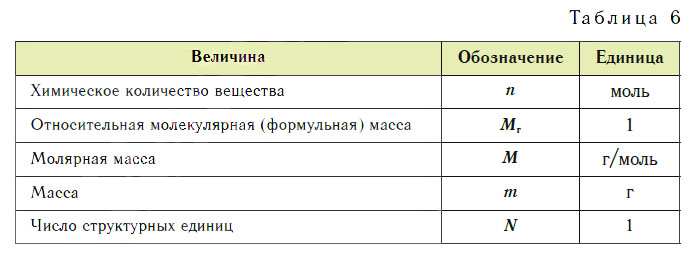
Эти расчеты проводят по уравнениям реакций. Единицы величин, которыми пользуются в химии, представлены в таблице 6.
При проведении любого вычисления по уравнению реакции нужно внимательно прочитать условие задачи. Особое в нимание обратите на расстановку коэффициентов, так как соотношение числа структурных единиц реагирующих веществ и получающихся продуктов реакции выражается в уравнениях коэффициентами так же, как и мольные отношения.
Для решения расчетной задачи необходим определенный порядок действий. Рассмотрим его на нескольких примерах.
Пример 1. Железо масс о й 224 г полностью прореагировало с хлором. Рассчитайте массу образовавшегося вещества FeCl3.
Методические рекомендации для выполнения контрольной работы по дисциплине «теория горения и взрыва» (стр. 4 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 9 10 |
Коэффициенты, стоящие в уравнении реакции, называются стехиометрическими коэффициентами и показывают, сколько молей (кмолей) веществ участвовало в реакции или образовалось в результате реакции.
Стехиометрический коэффициент, показывающий число молей кислорода, необходимое для полного сгорания вещества, обозначается буквой β.
В первой реакции β = 5.
Горение глицерина в кислороде
1. Записываем уравнение реакции горения.
С3Н8О3 + О2 = СО2 + Н2О
2. Уравниваем углерод и водород:
С3Н8О3 + О2 = 3СО2 + 4Н2О.
3. В правой части уравнения 10 атомов кислорода.
В составе горючего вещества есть 3 атома кислорода, следовательно, из кислорода в продукты горения перешли 10 – 3 = 7 атомов кислорода.
Таким образом, перед кислородом необходимо поставить коэффициент 7 : 2 = 3,5
С3Н8О3 +3,5О2 = 3СО2 + 4Н2О.
В этой реакции β = 3,5.
Горение аммиака в кислороде
Аммиак состоит из водорода и азота, следовательно, в продуктах горения будут вода и молекулярный азот.
NH3 + 0,75O2 = 1,5H2O + 0,5N2 β = 0,75.
Обратите внимание, что перед горючим веществом коэффициент 1, а все остальные коэффициенты в уравнении могут быть дробными числами.
Горение сероуглерода в кислороде
Продуктами горения сероуглерода CS2 будут углекислый газ и оксид серы (IV).
CS2 + 3O2 = CO2 + 2SO2 β = 3.
Чаще всего в условиях пожара горение протекает не в среде чистого кислорода, а в воздухе. Воздух состоит из азота (78 %), кислорода (21 %), окислов азота, углекислого газа, инертных и других газов (1 %). Для проведения расчетов принимают, что в воздухе содержится 79 % азота и 21 % кислорода. Таким образом, на один объем кислорода приходится 3,76 объемов азота (79:21 = 3,76).
В соответствии с законом Авогадро и соотношение молей этих газов будет 1 : 3,76. Таким образом, можно записать, что молекулярный состав воздуха (О2 + 3,76N2).
Составление уравнений реакций горения в воздухе
Пример 2.2. Составить уравнение реакции горения водорода, анилина, пропанола, угарного газа, хлорметана, диэтилтиоэфира, диметилфосфата.
Составление реакций горения веществ в воздухе аналогично составлению реакций горения в кислороде. Особенность состоит только в том, что азот воздуха при температуре горения ниже 20000С в реакцию горения не вступает и выделяется из зоны горения вместе с продуктами горения.
Горение водорода в воздухе
Н2 + 0,5(О2 + 3,76N2) = Н2О + 0,5⋅3,76N2 β = 0,5.
Обратите внимание, что стехиометрический коэффициент перед кислородом 0,5 необходимо поставить и в правой части уравнения перед азотом.
Горение пропанола в воздухе
С3Н7ОН + 4,5(О2 + 3,76N2) =3СО2 + 4Н2О +4,5⋅3,76N2 β = 4,5.
В составе горючего есть кислород, поэтому расчет коэффициента β проводят следующим образом: 10 – 1 = 9; 9 : 2 = 4,5.
Горение анилина в воздухе
С6Н5NН2 + 7,75(О2 + 3,76N2) =6СО2 + 3,5Н2О + 0,5N2 +7,75⋅3,76N2 β = 7,75.
В этом уравнении азот в правой части уравнения встречается дважды: азот воздуха и азот из горючего вещества.
Горение угарного газа в воздухе
СО + 0,5(О2 + 3,76N2) =СО2 + 0,5⋅3,76N2 β = 0,5.
Горение хлорметана в воздухе
СН3Сl + 1,5(О2 + 3,76N2) =СО2 + НСl + Н2О +1,5⋅3,76N2 β = 1,5.
Горение диэтилтиоэфира в воздухе
(С2Н5)2 S + 7,5(О2 + 3,76N2) =4СО2 + 5Н2О + SO2 + 7,5⋅3,76N2 β = 7,5.
Горение диметилфосфата в воздухе
(СН3)2НР О4 + 3(О2 + 3,76N2) =2СО2 + 3,5Н2О + 0,5Р2О5 + 3⋅3,76N2 β = 3.
Расчет молей (киломолей) исходных веществ и продуктов реакции по уравнению реакции горения
Пример 2.3. Сколько молей исходных веществ участвовало в реакции и сколько молей продуктов горения образовалось при полном сгорании 1 моля бензойной кислоты С6Н5СООН?
1. Запишем уравнение реакции горения бензойной кислоты.
С6Н5СООН + 7,5(О2 + 3,76N2) =7СО2 + 3Н2О +7,5⋅3,76N2
2. Исходные вещества: 1 моль бензойной кислоты; 7,5 молей кислорода; 7,5⋅3,76 молей азота. Газов воздуха всего 7,5⋅4,76 молей.
Всего (1 + 7,5⋅4,76) молей исходных веществ.
3. Продукты горения: 7 молей углекислого газа;
7,5⋅3,76 моля азота.
Всего (7 + 3 + 7,5⋅3,76) молей продуктов горения.
Аналогичные соотношения и в том случае, когда сгорает 1 киломоль бензойной кислоты.
Смеси сложных химических соединений или вещества сложного элементного состава нельзя выразить химической формулой, их состав выражается чаще всего в процентном содержании каждого элемента. К таким веществам можно отнести, например, нефть и нефтепродукты, древесину и многие другие органические вещества.
2.1. Расчет объема воздуха, необходимого для горения
Расчет объема воздуха, необходимого для горения, предполагает вычисление
а) теоретического объема воздуха Vвтеор и б) практического объема воздуха Vвпр, затраченного на горение (с учетом коэффициента избытка воздуха).
Стехиометрическое количество воздуха в уравнении реакции горения предполагает, что при данном соотношении компонентов, участвующих в реакции горения, воздух расходуется полностью. Объем воздуха в данном случае называется теоретическим (Vвтеор).
Горение может происходить не только при стехиометрическом соотношении компонентов, но и при значительном отклонении от него. Как правило, в условиях пожара на сгорание вещества воздуха затрачивается больше, чем определяется теоретическим расчетом. Избыточный воздух ΔVв в реакции горения не расходуется и удаляется из зоны реакции вместе с продуктами горения. Таким образом, практический объем равен
Vвпр = Vвтеор + ΔVв (2.1)
и, следовательно, избыток воздуха будет равен
ΔVв= Vвпр — Vвтеор (2.2)
Обычно в расчетах избыток воздуха при горении учитывается с помощью коэффициента избытка воздуха (α). Коэффициент избытка воздуха показывает, во сколько раз в зону горения поступило воздуха больше, чем это теоретически необходимо для полного сгорания вещества:

Для горючих смесей стехиометрического состава (т. е. состава, соответствующего уравнению реакции горения) коэффициент избытка воздуха α = 1, при этом реальный расход воздуха равен теоретическому. В этом случае обеспечивается оптимальный режим горения.
Расчёты по термохимическим уравнениям
Теоретический материал представлен на страницах:
Любая химическая реакция сопровождается поглощением или выделением энергии. Термохимические уравнения показывают соотношение между кол-вом веществ, вступающих в реакцию, и кол-вом энергии, которую выделяют, либо поглощают эти вещества в процессе химической реакции.
Главное отличие термохимического уравнения от молекулярного заключается в том, что кроме формул и коэффициентов, в нем указывается еще и кол-во энергии (теплоты реакции), относящееся к числу молей реагирующих веществ, соответствующему коэффициентам в уравнении реакции.
Теплота реакции (тепловой эффект) обозначается буквой Q (измеряется в кДж), и записывается в конце уравнения. Знак «плюс» перед числом обозначает выделившееся кол-во энергии, знак «минус» — кол-во поглощенной энергии.
Реакции, протекающие с выделением энергии, называются экзотермическими; с поглощением энергии — эндотермическими.
Если известна масса одного из двух реагирующих веществ, на основе термохимического уравнения можно определить кол-во теплоты реакции.
Пример 1 . Определить теплоту реакции горения 320 г серы.
- Согласно уравнения реакции, при сгорании 1 моля серы выделяется 297 кДж энергии, нам надо узнать, сколько энергии выделится при сгорании 320 г серы.
- Для решения задачи необходимо составить и решить простую пропорцию:
- Переходим от молей к граммам:
- В пропорции заменяем моли на граммы:
Если известно кол-во выделенной (поглощенной) теплоты в ходе реакции, можно определить массы прореагировавших веществ.
Пример 2 . Определить кол-во сгоревшего угля, если в ходе горения было выделено 33520 кДж энергии.
- Согласно уравнения реакции, при сгорании 1 моль углерода (масса 1 моль С = 12 г) выделилсь 402,24 кДж энергии.
- Составляем и решаем пропорцию:
Пример 3 . При горении 1 л метана (н.у) выделяется 39 кДж энергии. Составить термохимическое уравнение реакции и вычислить тепловой эффект.
Пример 4 . При горении 2,4 г магния (н.у) выделяется 60,12 кДж энергии. Составить термохимическое уравнение реакции.
Пример 5 . Два моля аммиака образуются в результате взаимодействия 1 моля азота с тремя молями водорода. Необходимо составить уравнение термохимической реакции, в ходе которой выделяется 92 кДж тепла, а все вещества, участвующие в реакции, являются газами.
Это очень простая задача, решение которой указано в условии.
Второй вариант записи термохимического уравнения.
Пример 6 . Составить термохимическое уравнение эндотермической реакции образования двухвалентного оксида азота из азота и кислорода с поглощением 180 кДж энергии. Записать это уравнение для образования 1 моля NO.
Первая часть задания не вызывает трудностей:
В этом термохимическом уравнении 2 моля оксида азота образуется при взаимодействии 1 моля азота и 1 моля кислорода. Для того, чтобы переписать данное уравнение для 1 моля оксида азота, необходимо все коэффициенты и кол-во теплоты разделить на 2:
Пример 7 . При образовании 50 г карбоната кальция (CaCO3) выделилось 80 кДж энергии. Определить тепловой эффект реакции разложения одного моля карбоната кальция.
- Определяем кол-во энергии, выделяемое при образовании 1 моля CaCO3 (М(CaCO3)=100 г/моль):
- Термохимическое уравнение реакции образования 1 моль карбоната кальция имеет вид:
- Термохимическое уравнение реакции разложения 1 моль карбоната кальция имеет вид:
- Q=-160 кДж
Пример 8 . Рассчитать кол-во выделенной энергии при образовании 2 л аммиака при н.у.
- Согласно термохимического уравнения — 1 моль аммиака образовался из полумоля азота и полутора молей водорода. Составляем пропорцию:
Пример 9 . Рассчитать тепловой эффект реакции:
- На основании первого следствия из закона Гесса:
- Теплоты образования простых веществ равны нулю:
- Теплоты образования сложных веществ берем из таблицы:
- Подставляем числовые значения в уравнение:
- Термохимическое уравнение реакции будет иметь вид:
Пример 10 . Рассчитать тепловой эффект реакции:
- Тепловой эффект реакции будем рассчитывать по формуле, вытекающей из второго следствия закона Гесса:
- Тепловые эффекты сгорания C2H4 и C2H6 можно взять из приведенных выше термохимический уравнений.
- Тепловой эффект сгорания водорода можно вычислить из термохимического уравнения образования 1 моля воды (теплоту образования воды берем из таблицы):
- Подставляем численные значения в формулу:
- Термохимическое уравнение реакции будет иметь вид:
Пример 11 . Определить скорость изменения реакции синтеза аммиака при а) увеличении концентрации исходных веществ в 2 раза; б) уменьшении давления в реакционной смеси в 2 раза:
- Записываем кинетическое уравнение данной реакции:
- Если концентрации исходных веществ будут увеличены в 2 раза, кинетическое уравнение примет вид:
- Составляем отношение и решаем его:
- Увеличение концентрации исходных веществ в 2 раза приведет к ускорению скорости реакции в 16 раз.
- Исходя из того факта, что концентрации газов пропорциональны давлению (при уменьшении давления в 2 раза концентрации также уменьшатся в 2 раза), логично предположить, что при снижении в 2 раза давления скорость протекания реакции снизится в 16 раз. Убедимся в этом, составив соотношение кинетических уравнений.
- Исхдное кинетическое уравнение:
- Для удобства чтения формул сделаем подстановку:
- Кинетическое уравнение при снижении давления в 2 раза:
- Соотошение:
- При уменьшении давления в реакционной смеси в 2 раза скорость протекания реакции уменьшится в 16 раз.
Пример 12 . Определить скорость изменения реакции с температурным коэффициентом 4 (γ=4) при повышении температуры с 10°C до 30°C.
Для решения задачи воспользуемся правилом Вант-Гоффа, которое выражается следующей математической формулой:
Все, что нам нужно сделать — подставить численные значения в формулу и провести расчеты:
При повышении температуры с 10 до 30 градусов Цельсия скорость реакции увеличится в 16 раз.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://pandia.ru/text/81/137/94086-4.php
http://prosto-o-slognom.ru/chimia_primery/005-termochimicheskie_uravneniya.html