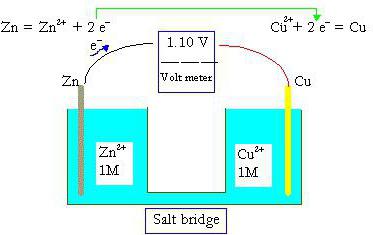
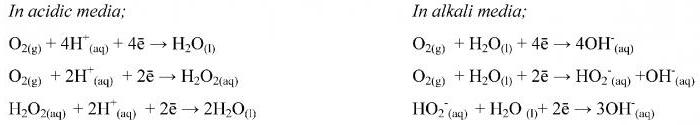Метод электронного баланса и ионно-электронный метод (метод полуреакций)
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение.
Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
Метод электронного баланса
В его основе метода электронного баланса лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
Найдем степень окисления элементов:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6. S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
3) Составить электронные уравнения и найти коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 | 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 | 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
4) Уравнять количества атомов элементов, не изменяющих степень окисления
Соблюдаем последовательность: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
6H + + 3O -2 = 3H2O
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления.
При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде).
При написании полуреакций в ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы:
H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Пример 1.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции:
2) Записать уравнение в ионном виде
В уравнении сократим те ионы, которые не принимают участие в процессе окисления-восстановления:
SO3 2- + MnO4 — + 2H + = Mn 2+ + SO4 2- + H2O
3) Определить окислитель и восстановитель и составить полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
SO3 2- + H2O — 2e — = SO4 2- + 2H +
4) Найти коэффициенты для окислителя и восстановителя
Необходимо учесть, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O |2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + |5 восстановитель, процесс окисления
5) Просуммировать обе полуреакции
Предварительно умножая на найденные коэффициенты, получаем:
2MnO4 — + 16H + + 5SO3 2- + 5H2O = 2Mn 2+ + 8H2O + 5SO4 2- + 10H +
Сократив подобные члены, находим ионное уравнение:
2MnO4 — + 5SO3 2- + 6H + = 2Mn 2+ + 5SO4 2- + 3H2O
6) Записать молекулярное уравнение
Молекулярное уравнение имеет следующий вид:
Пример 2.
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Пример 3.
Составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Еще больше примеров составления окислительно-восстановительных реакций приведены в разделе Задачи к разделу Окислительно-восстановительные реакции. Также в разделе тест Окислительно-восстановительные реакции
Метод полуреакций — составление уравнений ОВР
Любая окислительно-восстановительная реакция состоит из двух «половинок» — в ходе ОВР идут два процесса — процесс окисления вещества-восстановителя и процесс восстановления вещества-окислителя. Оба эти процесса могут быть описаны соответственными ионными уравнениями, которые потом можно суммировать и получить итоговое общее ионное уравнение реакции, а потом записать молекулярное уравнение.
В качестве примера составим уравнение реакции сероводорода с раствором калия перманганата в кислой среде методом полуреакций. Ранее это уравнение было составлено методом электронного баланса.
В ходе реакции происходит разложение молекул сероводорода на серу и водород, о чем свидетельствует постепенное помутнение раствора перманганата калия (сера выпадает в осадок). Процесс окисления сероводорода запишем в виде уравнения полуреакции окисления:
Поскольку в левой и правой частях схемы кол-во атомов серы и водорода равно, то стрелку можно заменить на знак равенства, уравняв предварительно число зарядов в исходном веществе и продуктах реакции:
Параллельно с помутнение раствора идет и смена его окраски — из малинового раствор становится бесцветным,что объясняется переходом ионов MnO4 — , имеющих малиновую окраску, в практически бесцветный катион марганца Mn 2+ . Эта полуреакция восстановления выражается схемой:
А куда же делся атом кислорода? — обязательно спросит внимательный читатель. В кислой среде атом кислорода, входящий в состав иона, соединяется с атомами водорода, выделяющимися в ходе полуреакции окисления, образуя молекулу воды, при этом, поскольку из одного иона освобождается аж 4 атома кислорода, то для их связывания требуется 8 атомов водорода:
Чтобы уравнять заряды в левой и правой части схемы, в левую часть надо добавить 5 электронов (в левой части сумма зарядов +7, а в левой +2):
Для получения суммарного уравнения реакции, необходимо почленно сложить две полуреакции, предварительно уравняв кол-во отданных и полученных электронов, по аналогии с методом электронного баланса:
Проверяем кол-во атомов и заряды в левой и правой частях суммарного уравнения, они равны, значит уравнение составлено правильно (водорода — по 16 атомов; серы — по 5; марганца — по 2; кислорода — по 8; заряды — по +4).
Чтобы перейти от ионного уравнения к молекулярному, надо в левой части подобрать к катионам и анионам их «пары» — анионы и катионы соответственно, после чего подобранные ионы записать и в правую часть уравнения, после этого ионы объединяются в молекулы, и получается молекулярное уравнение.
Результат аналогичен уравнению, полученному методом электронного баланса.
Правила составления уравнений ОВР методом полуреакций
- На первом этапе в ионном виде записывают полуреакцию окисления и полуреакцию восстановления, в которых указывают вещество-восстановитель и вещество-окислитель, с продуктами их реакции.
- Сильные электролиты записываются в виде ионов.
- Слабые электролиты, газы и твердые вещества, выпадающие в осадок — в виде молекул.
- Продукты реакции между восстановителем и окислителем устанавливаются по справочникам или по «шпаргалке», приведенной на странице «Определение продуктов ОВР» (это самый сложный этап для начинающих).
- Записывают схему реакции, в которой многоточием обозначают неизвестные продукты реакции.
- Что делать с кислородом:
- Если в исходном веществе кислорода содержится больше, чем в продуктах реакции, то «лишний» кислород в растворах с кислой средой связывается с катионами водорода, образуя молекулы воды (O -2 +2H + =H2O); в нейтральных растворах — в гидроксид-ионы: O -2 +H2O=2OH — ;
- Если в исходном веществе кислорода содержится меньше, чем в продуктах реакции, то «недостающий» кислород «забирается» из молекул воды (в растворах с кислой и нейтральной средой): H2O=O -2 +2H + ; в щелочных растворах — за счет гидроксид-ионов: 2OH — =O -2 +H2O.
- В левой и правой частях уравнения должны быть равны суммарное число и знак электрических зарядов.
Достоинства метода полуреакций:
- Работают с реально существующими ионами (MnO4 — ), а не виртуальными (Mn +7 ).
- Нет необходимости знать степени окисления атомов.
- Прослеживается роль среды, в которой происходит взаимодействие веществ.
- Не нужно знать все продукты реакции, они выводятся «сами собой» в процессе составления уравнения.
Пример составления уравнения ОВР для кислотной среды
Составление уравнения реакции серы с азотной кислотой:
- S+HNO3
- S 0 → SO4 2- — процесс окисления восстановителя.
- NO3 — → NO — процесс восстановления окислителя.
- Приводим в «порядок» первую полуреакцию окисления:
- S 0 → SO4 2- — отличник должен здесь спросить, откуда справа взялся кислород? Немного терпения, сейчас все станет ясно.
- в правую часть схемы, где присутствует избыток кислорода, добавляется катион водорода:
S 0 → SO4 2- +H + - у внимательного читателя тут же должен возникнуть вопрос — а откуда взялся катион водорода? Отвечаем: из молекулы воды, которая добавляется в левую часть схемы:
S 0 +H2O → SO4 2- +H + - Вот теперь настало время уравнять в обеих частях схемы кислород, который, теперь понятно, откуда взялся:
S 0 +4H2O → SO4 2- +H + - Теперь надо уравнять водород:
S 0 +4H2O → SO4 2- +8H + - С атомами элементов в обеих частях схемы полный порядок, осталось разобраться с зарядами — в левой части заряд нулевой; в правой: (-2)+8(+1)=+6:
S 0 +4H2O-6e — → SO4 2- +8H +
- Делаем аналогичную работу со второй полуреакцией восстановления:
- NO3 — → NO
- Добавляем водород, в левую часть, где присутствует «лишний» кислород:
NO3 — +H + → NO - В правую часть добавляем воду:
NO3 — +H + → NO+H2O - Уравниваем кислород:
NO3 — +H + → NO+2H2O - Уравниваем водород:
NO3 — +4H + → NO+2H2O - Уравниваем заряды:
NO3 — +4H + +3e — → NO+2H2O
- Уравниваем кол-во электронов, которые были отданы и приняты в двух полуреакциях:
- Суммируем левые и правые части, предварительно умножив на коэффициент (2) члены второй полуреакции:
- Проводим сокращение одинаковых членов в левой и правой частях схемы и добавляем в пару к анионам «нужные» катионы, чтобы образовались молекулы, в нашем случае это будут молекулы азотной и серной кислоты, для этого мы добавим катион водорода (2H + ):
- Суммарное молекулярное уравнение:
S+2HNO3 = H2SO4+2NO — в результате взаимодействия серы с азотной кислотой получается серная кислота и оксид азота (II).
Пример составления уравнения ОВР для кислотной среды
«Фокус» уравнивания кол-ва атомов кислорода и водорода для уравнений ОВР в щелочной среде заключается в следующем:
- Вода (H2O) добавляется в ту часть полуреакции, в которой присутствует избыток кислорода.
- Соответственно, в противоположную часть уравнения-схемы добавляется удвоенное число гидроксид-ионов (OH — ).
- Перед формулой молекулы воды ставится коэффициент, уравнивающий разницу кол-ва атомов кислорода в левой и правой частях полуреакции.
- Перед формулой гидроксид-иона ставится удвоенный коэффициент.
- Восстановитель присоединяет атомы кислорода из гидроксид-ионов.
- MnO2+KClO3+KOH → ?
- MnO2 → MnO4 2- оксид марганца является восстановителем, он будет связывать гидроксид-ионы.
- Поскольку в правой части схемы килорода больше (на 2 атома), то вода добавляется сюда же, перед ее формулой ставится коэффициент 2, соответственно, в левую часть схемы полуреакции добавляют 4 гидроксид-иона:
MnO2+4OH — → MnO4 2- +2H2O - Уравниваем заряды:
MnO2+4OH — -2e — → MnO4 2- +2H2O - ClO3 — → Cl — — полуреакция восстановления.
- Избыток кислорода (3 «лишних» атома) находится в левой части схемы полуреакции, сюда же добавляем и 3 молекулы воды, а в правую часть 6 гидроксид-ионов:
ClO3 — +3H2O → Cl — +6OH — - Уравниваем заряды:
ClO3 — +3H2O+6e — → Cl — +6OH — - Уравниваем в полуреакциях кол-во отданных и принятых электронов (6 и 2 сокращаем на 2), и получаем суммарное уравнение, путем сложения двух уравнений полуреакций:
- Проводим сокращение подобных слагаемых и добавляем катионы калия, чтобы перейти к молекулярной форме уравнения реакции:
- Молекулярное уравнение реакции:
3MnO2+6KOH+KClO3 = 3K2MnO4+3H2O+KCl
Пример составления уравнения ОВР для нейтральной среды
Среду нейтральной можно счситать лишь условно, в любом случае, среда будет либо слабощелочной, либо слабокислотной.
Составляя уравнение ОВР методом полуреакций для нейтральной среды, одну полуреакцию составляют, как для кислотной среды — в левую часть схемы добавляют молекулу воды, в правую — катион водорода), вторую — как для щелочной (в левую часть добавляют молекулу воды, в правую — гидроксид-ион).
- Na2SO3+KMnO4+H2O
- SO3 2- → SO4 2- — процесс окисления восстановителя;
- MnO4 — → MnO2 — процесс восстановления окислителя;
- Схема реакции:
SO3 2- +MnO4 — → SO4 2- +MnO2+. - Составляем уравнения полуреакций:
- Молекулярное уравнение:
Еще один пример:
- S+KMnO4 → ?
- S → SO4 2-
- MnO4 — → MnO2
- Первую полуреакцию оформляем, как для кислотной среды; вторую — как для щелочной:
- Сокращаем обе части равенства на 8 молекул воды, и добавляем катионы калия:
- Молекулярное уравнение:
S+2KMnO4 = K2SO4+2MnO2
Более подробно составление уравнений окислительно-восстановительных реакций методом полуреакций в различных средах рассмотрено на странице Влияние среды на протекание ОВР.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Метод полуреакций: алгоритм
Многие химические процессы проходят с изменением окислительных степеней атомов, которые образуют реагирующие соединения. Написание уравнений реакций окислительно-восстановительного типа часто сопровождается трудностью при расстановке коэффициентов перед каждой формулой веществ. Для этих целей разработаны методики, связанные с электронным или электронно-ионным балансом распределения зарядов. В статье подробно описан второй способ составления уравнений.
Метод полуреакций, сущность
Он еще называется электронно-ионным балансом распределения коэффициентных множителей. Основан метод на обмене отрицательно заряженными частицами между анионами или катионами в растворенных средах с разным значением водородного показателя.
В реакциях электролитов окислительного и восстановительного типа участвуют ионы с отрицательным или положительным зарядом. Уравнения молекулярно-ионного вида, в основе которых задействован метод полуреакций, наглядно доказывают суть любого процесса.
Для формирования баланса используют специальное обозначение электролитов сильного звена в качестве ионных частиц, а слабых соединений, газов и осадков в виде недиссоциированных молекул. В составе схемы необходимо указывать частицы, в которых изменяются степени их окисления. Для определения растворяющей среды в балансе обозначают кислые (H + ), щелочные (OH — ) и нейтральные (H2O) условия.
Для чего используют?
В ОВР метод полуреакций направлен на написание уравнений ионных отдельно для процессов окислительных и восстановительных. Конечным балансом будет их суммирование.
Этапы выполнения
Своими особенностями написания обладает метод полуреакций. Алгоритм включает следующие стадии:
— Первым делом следует записать формулы всех реагирующих веществ. Например:
— Затем необходимо установить функцию, с химической точки зрения, каждого составляющего процесса. В данной реакции KMnO4 выступает в роли окислителя, H2S является восстановителем, а HCl определяет кислотную среду.
— Третьим этапом нужно записать с новой строки формулы ионные реагирующих соединений с сильным электролитным потенциалом, у атомов которых наблюдается смена степеней их окисления. В данном взаимодействии MnO4 — выступает в роли окисляющего вещества, H2S является восстанавливающим реагентом, а H + или оксониевый катион H3O + определяет кислотную среду. Газообразные, твердые или слабые электролитические соединения выражают целыми формулами молекулярными.
Зная исходные компоненты, постараться определить, какая у окисляющего и восстанавливающего реагента будет восстановленная и окисленная форма соответственно. Иногда конечные вещества уже заданы в условиях, что облегчает работу. В последующих уравнениях указывают переход H2S (сероводорода) в S (серу), а аниона MnO4 — в катион Mn 2+ .
Для баланса атомарных частиц в левом и правом участке в кислотную среду прибавляют водородный катион H + или молекулярную воду. В раствор щелочной вносят ионы гидроксида OH — или H2O.
В растворе атом кислорода из манганатных ионов совместно с H + формируют молекулы воды. Для выравнивания количества элементов уравнение записывают так: 8H + + MnO4 — → 4H2O + Mn 2+ .
Затем проводят электрическую балансировку. Для этого считают общую сумму зарядов в левом участке, получается +7, а затем в правой стороне, выходит +2. Для уравновешивания процесса к исходным веществам добавляется пять отрицательных частиц: 8H + + MnO4 — + 5e — → 4H2O + Mn 2+ . Получается полуреакция восстановления.
Теперь уравнять по числу атомов следует процесс окисления. Для этого в правую часть добавляют водородные катионы: H2S → 2H + + S.
После проводят уравнивание зарядов: H2S -2e — → 2H + + S. Видно, что от исходных соединений отнимают две отрицательные частицы. Получается полуреакция окислительного процесса.
Записывают оба уравнения в столбик и выравнивают отданные и принятые заряды. По правилу определения наименьших кратных подбирают для каждой полуреакции свой множитель. На него умножается окислительное и восстановительное уравнение.
Теперь можно осуществить суммирование двух балансов, сложив левые и правые стороны между собой и сократив количество электронных частиц.
8H + + MnO4 — + 5e — → 4H2O + Mn 2+ |2
H2S -2e — → 2H + + S |5
16H + + 2MnO4 — + 5H2S → 8H2O + 2Mn 2+ + 10H + + 5S
В полученном уравнении можно число H + сократить на 10: 6H + + 2MnO4 — + 5H2S → 8H2O + 2Mn 2+ + 5S.
Проверяем правильность составления ионного баланса с помощью подсчета числа кислородных атомов до стрелки и после нее, которое равняется 8. Также необходимо сверить заряды конечной и исходной части баланса: (+6) + (-2) = +4. Если все совпадает, то он составлен правильно.
Метод полуреакций заканчивается переходом от ионной записи к уравнению молекулярному. Для каждой анионной и катионной частицы левой части баланса подбирается противоположный по заряду ион. Затем их переносят в правую сторону, в таком же количестве. Теперь ионы можно соединить в целые молекулы.
6Cl — + 2K + → 6Cl — + 2K +
Применять метод полуреакций, алгоритм которого сводится к написанию молекулярного уравнения, можно наряду с написанием балансов электронного типа.
Определение окислителей
Такая роль принадлежит ионным, атомарным или молекулярным частицам, которые принимают отрицательно заряженные электроны. Вещества окисляющие претерпевают восстановление в реакциях. Они обладают электронным недостатком, который легко можно восполнить. Такие процессы включают окислительно-восстановительные полуреакции.
Не у всех веществ имеется способность присоединять электроны. К сильным окисляющим реагентам относят:
- галогеновых представителей;
- кислоту типа азотной, селеновой и серной;
- калий перманганатный, дихроматный, манганатный, хроматный;
- марганцовые и свинцовые четырехвалентные оксиды;
- серебро и золото ионное;
- соединения газообразные кислорода;
- меди двухвалентной и серебра одновалентного оксиды;
- хлорсодержащие солевые компоненты;
- водку царскую;
- водорода перекись.
Определение восстановителей
Такая роль принадлежит ионным, атомарным или молекулярным частицам, которые отдают отрицательный заряд. В реакциях восстанавливающие вещества претерпевают окислительное действие при отщеплении электронов.
- представители многих металлов;
- серы четырехвалентной соединения и сероводород;
- галогенсодержащие кислоты;
- железа, хрома и марганца сульфаты;
- олова двухвалентный хлорид;
- азотсодержащие реагенты типа кислоты азотистой, двухвалентного оксида, аммиака и гидразина;
- природный углерод и его оксид двухвалентный;
- водородные молекулы;
- кислота фосфористая.
Преимущества электронно-ионного способа
Чтобы написать окислительно-восстановительные реакции, метод полуреакций применяют чаще, чем баланс электронного вида.
Связано это с преимуществами электронно-ионного способа :
- Во время написания уравнения рассматривают реальные ионы и соединения, которые существуют в составе раствора.
- Можно изначально не иметь информации о получающихся веществах, их определяют на конечных этапах.
- Не всегда нужны данные об окислительной степени.
- Благодаря методу можно узнать число электронов, которые участвуют в полуреакциях, как меняется водородный показатель раствора.
- По сокращенным уравнениям ионного вида изучается особенность протекания процессов и структура получившихся веществ.
Полуреакции в кислом растворе
Проведение вычислений при избытке водородных ионов подчиняется основному алгоритму. Метод полуреакций в кислой среде начинают с записи составных частей любого процесса. Потом их выражают в форме уравнений ионного вида с соблюдением баланса атомарного и электронного заряда. Отдельно записывают процессы окислительного и восстановительного характера.
Для выравнивания атомарного кислорода в сторону реакций с его избытком привносят водородные катионы. Количества H + должно хватить для получения молекулярной воды. В сторону недостатка кислорода приписывают H2O.
Затем проводят баланс водородных атомов и электронов.
Делают суммирование частей уравнений до и после стрелки с расстановкой коэффициентов.
Осуществляют сокращение одинаковых ионов и молекул. К уже записанным реагентам в суммарном уравнении выполняют добавление недостающих анионных и катионных частиц. Их количество после и до стрелочки должно совпадать.
Уравнение ОВР (метод полуреакций) считается выполненным при написании готового выражения молекулярного вида. Возле каждого компонента должен стоять определенный множитель.
Примеры для кислой среды
Взаимодействие нитрита натрия с кислотой хлорноватой приводит к получению натрия нитрата и кислоты соляной. Для расстановки коэффициентов используется метод полуреакций, примеры написания уравнений связаны с указанием кислой среды.
ClO3 — + 6H + + 6e — → 3H2O + Cl — |1
3Na + + H + → 3Na + + H +
В данном процессе из нитрита получается нитрат натрия, а из хлорноватой образуется соляная кислота. Окислительная степень азота изменяется с +3 до +5, а заряд хлора +5 становится -1. Оба продукта не образуют осадка.
Полуреакции для щелочной среды
Проведение вычислений при избытке гидроксидных ионов соответствует расчетам для кислых растворов. Метод полуреакций в щелочной среде также начинают с выражения составных частей процесса в форме ионных уравнений. Отличия наблюдаются во время выравнивания числа атомарного кислорода. Так, в сторону реакции с его избытком привносят молекулярную воду, а в противоположную часть дописывают анионы гидроксида.
Коэффициент перед молекулой H2O показывает разницу в количестве кислорода после и до стрелки, а для ионов OH — его удваивают. В ходе окисления реагент, выполняющий роль восстановителя, отнимает атомы O от гидроксильных анионов.
Метод полуреакций заканчивается проведением оставшихся этапов алгоритма, которые совпадают с процессами, имеющими кислый избыток. Конечным результатом служит уравнение молекулярного вида.
Примеры для щелочной среды
При смешивании йода с натрия гидроксидом образуется натрия йодид и йодат, молекулы воды. Для получения баланса процесса используют метод полуреакций. Примеры для растворов щелочных имеют свою специфику, связанную с уравниванием атомарного кислорода.
6OH — + I — 5e — → I — + 3H2O + IO3 — |1
I + 5I + 6OH — → 3H2O + 5I — + IO3 —
Результатом реакции является исчезновение фиолетового окрашивания молекулярного йода. Происходит изменение степени окисления данного элемента с 0 до -1 и +5 с образованием йодида и йодата натрия.
Реакции в нейтральной среде
Обычно так называют процессы, проходящие при гидролизе солей с образованием слабокислого (с водородным показателем от 6 до 7) или слабощелочного (с pH от 7 до 8) раствора.
Метод полуреакций в нейтральной среде записывают несколькими вариантами.
В первом способе не учитывают солевой гидролиз. Среду принимают за нейтральную, а слева от стрелочки приписывают молекулярную воду. В таком варианте одну полуреакцию принимают за кислотную, а другую – за щелочную.
Второй способ подходит для процессов, в которых можно установить примерное значение водородного показателя. Тогда реакции для метода ионно-электронного рассматривают в щелочном или кислом растворе.
Пример с нейтральной средой
При соединении сероводорода с натрия дихроматом в воде получается осадок серы, натрия и хрома трехвалентного гидроксиды. Это типичная реакция для нейтрального раствора.
H2S — 2e — → S + H + |3
7H2O +3H2S + Cr2O7 2- → 3H + +3S + 2Cr(OH)3 +8OH — . Катионы водорода и гидроксид-анионы, соединяясь, образуют 6 молекул воды. Их можно убрать в правой и левой части, оставив излишек перед стрелкой.
В конце реакции образуется осадок из гидроксида хрома голубого цвета и желтой серы в щелочном растворе с гидроксидом натрия. Окислительная степень элемента S с -2 становится 0, а хрома заряд с +6 превращается в +3.
http://prosto-o-slognom.ru/chimia_ovr/09_metod_polureaktsij.html
http://fb.ru/article/240526/metod-polureaktsiy-algoritm