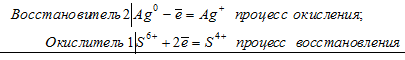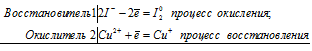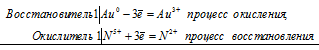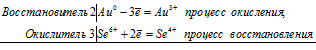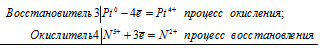Chemicals-el.ru
» Сайт о химических элементах
Аффинаж платины
Растворение «шлиховой платины» в «царской водке» осуществляется при температуре 70–85 оС, причем сырье загружается в предварительно нагретую до указанной температуры соляную кислоту, а затем добавляется рассчитанное количество HNO3. Внешними признаками конца растворения является бурное вспенивание и выделение паров оксидов азота по реакциям:
3HCl + HNO3 = NOCl + Cl2 + 2H2O
Таким образом, не исключено выделение весьма реакционноспособного атомарного хлора, взаимодействующего с благородными и неблагородными металлами. Последние переходят в хлориды (FeCl3, CuCl2 и др.), а платина, палладий и золото – в хлоридные комплексы в соответствии с реакциями:
3Pt + 18HCl + 4HNO3 = 3H2[PtCl6] + 4NO + 8H2O
3Pd + 18HCl + 4HNO3 = 3H2[PdCl6] + 4NO2 + 8H2O
Au + 4HCl + HNO3 = H[AuCl4] + NO + 2H2O.
Палладий даже при растворении в «царской водке» частично переходит в тетрахлоропалладиевую кислоту H2[PdCl4], где проявляет типичную для него степень окисления +2. Некоторое количество платины и иридия образуют соединения H2[PtCl4] и H2[IrCl6], соответственно. Небольшая часть платины может образовывать гексахлороплатинат(IV) железа по реакции:
3H2[PtCl6] + 2FeCl3 = Fe2[PtCl6]3 + 6HCl.
В присутствии азотной кислоты также образуются нитрозохлоридные соединения платиновых металлов, которые выпадают в виде желтого осадка. Образование нитрозохлоридных соединений протекает по реакциям:
H2[PdCl4] + 2NOCl = (NO)2[PdCl4] + 2HCl
H2[PtCl6] + 2NOCl = (NO)2[PtCl6] + 2HCl
H2[IrCl6] + 2NOCl = (NO)2[IrCl6] + 2HCl
Если нитрозохлоридные соединения не разрушать, то они будут оставаться в нерастворимом остатке. Разрушение их осуществляется нагреванием раствора с добавлением воды при температуре 105–110 оС в результате протекания следующих реакций:
(NO)2[PtCl6] + H2О = H2[PtCl6] + NO+ NO2.
Аналогично идут реакции для палладия и иридия. Конец разрушения определяется по прекращению выделения бурых паров оксидов азота и вскипания.
Для растворения «царской водкой» обычно применяются 33%-ная соляная и 65%-ная азотная кислоты. Расход кислот на 100 кг шлиховой платины составляет: HCl – 500 л, HNO3 – 100 л. В результате растворения «шлиховой платины» в «царской водке» в раствор переходит большая часть (90% при первом растворении) платины, почти весь палладий, около 60% родия, 15% иридия, 90% золота и 100% железа и меди. Часть иридия, родия, платины и серебро в виде AgCl остаются в нерастворившемся остатке. Процентное извлечение платиновых металлов при растворении в «царской водке» определяется составом конкретной партии перерабатываемой «шлиховой платины». В зависимости от этого выход первого нерастворимого остатка изменяется от 10 до 15%.
Растворы, полученные после вскрытия в «царской водке», обрабатывают HCl с целью удаления остатков азотной кислоты. Эта операция проводится при постоянной температуре 120–125 оС. После упаривания раствор охлаждается и отфильтровывается от первого нерастворимого остатка, который еще содержит некоторое количество платины. Поэтому, собрав достаточное количество нерастворимого остатка, производят повторное его растворение примерно по тому же режиму, что и основную «шлиховую платину». Полученный второй нерастворимый остаток содержит мало платины и богат редкими платиновыми металлами, на извлечение которых он направляется.
Растворы после растворения «шлиховой платины» и первого нерастворимого остатка и упаривания с соляной кислотой поступают на доводку, цель которой как можно полнее перевести Pd(IV) в Pd(II), Ir(IV) в Ir(III), Au(III) в золото элементарное. Необходимость доводки определяется тем, что последующая операция – это выделение (осаждение) платины в виде гексахлороплатината(IV) аммония (NH4)2[PtCl6] (ХПА), а Ir(IV) и Pd(IV) также образуют однотипные нерастворимые соли. В то же время (NH4)2[PdCl4] и (NH4)3[IrCl6] хорошо растворимы в воде. Необходимо обратить внимание на то, что в процессе доводки как можно большая часть платины должна остаться в степени окисления+4, чтобы обеспечить высокий выход первого гексахлороплатината(IV) аммония (комплексная соль (NH4)2[PtCl4] подобно (NH4)2[PdCl4] хорошо растворима). Родий в процессе доводки степень окисления не меняет. Доводка осуществляется так: раствор при температуре 120–125 оС упаривается до плотности 1.38, затем обрабатывается 15%-ным этиловым спиртом, расход которого – 250–300 мл на 200 кг шлиховой платины. Этиловый спирт расходуется на процесс восстановления по следующим реакциям:
12H2[IrCl6] + C2H5OH + 3H2O = 12H3[IrCl6] + 2CO2
6H2[PdCl6] + C2H5OH + 3H2O = 6H2[PdCl4] + 2CO2+ 12HCl
4H[AuCl4] + C2H5OH + 3H2O = 4Au + 2CO2+ 16HCl.
Смотрите также
Барий (Baryum), Ba
Защитные стенки рентгеновских установок медицинского и научного назначения делают из кирпича, содержащего соединения бария. Прекрасный поглотитель рентгеновских лучей — барий применяется исключительно .
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e2fb3231a81979a • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Составление окислительно-восстановительных реакций соединений серебра, золота и платины
Задание 391
Серебро не взаимодействует с разбавленной серной кислотой, тогда как в концентрированной оно растворяется. Чем это можно объяснить? Составьте электронные и молекулярные уравнения соответствующей реакции.
Решение:
Серная кислота обладает окислительными свойствами (сходными со свойствами азотной кислоты), если её концентрация превосходит 70%. Только тогда можно говорить о специфических свойствах H2SO4, как окислителя. Концентрированная серная кислота, как окислитель восстанавливается активными металлами (от Mg Cr) до H2S, малоактивными металлами (от Fe до Pb) – до свободной серы, а тяжёлыми, инертными металлами (отSb до Au) – до оксида серы (IV). При содержании H2SO4 в растворе менее 70% (разбавленная серная кислота) её поведение описывается в рамках обычных представлений. При взаимодействии разбавленной серной кислоты с металлами, стоящими в электрохимическом ряду напряжений левее водорода, выделяется газообразный водород. С металлами, стоящими в ряду напряжений правее водорода, разбавленная серная кислота не взаимодействует.
В концентрированной серной кислоте элементом-окислителем является атом серы (степень окисления +6), а в разбавленной – водород (степень окисления +1).
Уравнение реакции растворения серебра в концентрированной серной кислоте
2Аg 0 + S 6+ = 2Ag + + S 4+
В данной реакции серебро увеличивает свою степень окисления от 0 до +1, т. е. проявляет свойства восстановителя, а сера уменьшает свою степень окисления от +6 до +4, т.е. проявляет свойства окислителя.
Задание 401
Какую степень окисления проявляют медь, серебро и золото в соединениях? Какая степень окисления наиболее характерна для каждого из них? Иодид калия восстанавливает ионы меди (II) в соединения меди со степенью окисления +1. Составьте электронные и молекулярные уравнения взаимодействия KI с сульфатом меди.
Решение:
Для меди характерна степень окисления +1 (Cu2O, CuCl, CuI, Cu2S) и +2 [CuO, CuSO4 . 5H2O, Cu(NO3)2 . 6H2O, CuS, Cu2(OH)2CO3]; для серебра: +1 (Ag2O, AgNO3, AgCl, AgBr, AgI); для золота: +3 (AuCl3, H[AuCl4]). Как элементы 2-й группы медь, серебро и золото имеют по одному электрону на внешнем энергетическом уровне (ns 1 ), поэтому должны проявлять степень окисления +1. Характерная степень окисления, как у элементов 2-й группы должна быть +2. Для меди наиболее характерна степень окисления +2, для серебра +1, а для золота +3.
Уравнения взаимодействия KI с сульфатом меди
2Сu 2+ +2I — = Cu + + I2 0
Задание 404
Золото растворяется в царской водке и в селеновой кислоте, приобретая при этом высшую степень окисления. Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
а) Золото растворяется в «царской водке» с образованием комплекса H[AuCl4]
Au 0 +N 5+ = Au 3+ + N 2+
3Au + 12HCl + 3HNO3 = 3H[AuCl4] + 3NO + 6H2O
б) Золото растворяется в селеновой кислоте с образованием селената золота(III)
2Au 0 + 3Se 6+ = 2Au 3+ + 3Se 4+
Задание 428
Составьте электронные и молекулярные уравнения реакций: а) растворения платины в царской водке; б) взаимодействия осмия с фтором. Платина окисляется до степени окисления +4, а осмий — до+8.
Решение:
а) Реакция растворения платины в царской водке
3Pt 0 + 4N 5+ = 3Pt 4+ + 4N 2+
б) Реакция взаимодействия осмия с фтором:
http://gomolog.ru/reshebniki/1-kurs/shimanovich-2014/428.html
http://buzani.ru/zadachi/khimiya-shimanovich/987-serebro-zoloto-platina-zadaniya-391-401-404-428