Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Ацетат аммония
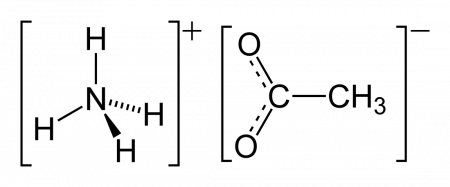
Ацетат аммония — аммониевая соль уксусной кислоты. Пищевая добавка E264 (консервант). СодержаниеПолучениеАцетат аммония получают по реакциям: Химические свойстваПри сравнительно низкой температуре 112 °C (385 K) разлагается на воду и ацетамид: В водном растворе подвергается гидролизу: ПрименениеСоль слабой кислоты и слабого основания, ацетат аммония применяется:
Характеристика свойств соединений азотаЗадача 887. Находим количество щёлочи, пошедшее на реакцию с солью аммония, получим: 1 : 0,5 = 2 : х; х = (0,5 . 2)/1= 1 моль. 1 моль любого газа при нормальных условиях занимает объём равный 22,4 л. Отсюда находим, что объём аммиака, выделившегося при реакции, равен: V(NH3) = VЭ . (NH3) = 22,4 . 1 = 22,4 л. Ответ: 22,4 л. Задача 888. Поэтому они являются осушителями газовых смесей. В обоих случаях образуются кислоты, с которыми взаимодействует аммиак, образуя соответствующие соли: Таким образом, Н2SO4 и Р2О5 нельзя применять в качестве осушителя аммиака, так как при этом происходит химическое взаимодействие аммиака с серной и фосфорной кислотами. а) (NH4)2CO3 б) NH4NO3 2NH4NO3 в) (NH4)2SO4 г) NH4С1 д) (NH4)2HPO4 е) (NH4)H2PO4 ж) (NH4)2Cr2O7 з) NH4NO2 Задача 890. NH4NO3(к) Находим ΔH 1 0 реакции, учитывая закон Гесса, получим: ΔH 1 0 = 2 ΔH 0 (Н2О) + ΔH 0 (N2O) — ΔH 0 (NH4NO3) = ΔG1 0 = 2 ΔG 0 (Н2О) + ΔG 0 (N2O) — ΔG 0 (NH4NO3) = б) Уравнение реакции имеет вид: NH4NO3(к) Находим реакции, учитывая закон Гесса, получим: Находим энергию Гиббса реакции, получим: ΔH2 0 ΔH 1 0 и ΔG2 0 ΔG 1 0 , поэтому вторая реакция, реакция (б) наиболее вероятна при 25 0 С и более зкзотермична, чем реакция (а). Так как обе реакции экзотермичны, то, согласно принципу Ле Шателье, при повышении температуры равновесие обеих реакций сместится влево. Вероятность протекания реакции(б), как наиболее экзотермичной, значительно уменьшится при повышении температуры, чем реакции (а). источники: http://chem.ru/acetat-ammonija.html http://buzani.ru/zadachi/khimiya-glinka/1289-soedineniya-azota-zadachi-887-890 | |||||||||||||||||||||||||||||||||||||||||||




 2NH3↑ + CO2↑ + H2O;
2NH3↑ + CO2↑ + H2O;