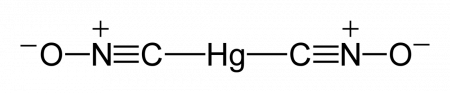Разложение гремучей ртути при взрыве идет по уравнению Hg(ONC)2 = Hg + 2CO + N2 + 364, 2 кДж?
Химия | 10 — 11 классы
Разложение гремучей ртути при взрыве идет по уравнению Hg(ONC)2 = Hg + 2CO + N2 + 364, 2 кДж.
Определите объем выделившихся газов (н.
У. ) и количество теплоты, поглотившейся при взрыве 1, 5 кг Hg(ONC)2.
M(Hg(ONC)2) = 200, 5 + 16 * 2 + 14 * 2 + 12 * 2 = 284, 5 г / моль
U(Hg(ONC)2) = m / M = 0, 005 моль
из уравнения U(N2) = U(Hg(ONC)2) = 0, 005 моль U(CO) = 2U(Hg(ONC)2) = 0, 01 моль
V = U * V молярный
V(N2) = 0, 005 моль * 22, 4 л / моль = 0, 112 л
V(CO) = 0, 01 моль * 22, 4 л / моль = 0, 224 л
Кол — во теплоты 364, 2 кДж.
При разложении оксида ртути (11) HgO образуются ртуть и кислород?
При разложении оксида ртути (11) HgO образуются ртуть и кислород.
Рассчитайте количество вещества, массу и объем кислорода, образующиеся при разложении 43, 4 г оксида ртути.
4c3h4(ono2)3 = 12co2 + 6n2 + 10 h20 + o2 + 5550 кдж рассчитайте какое количество теплоты выделится при взрыве 1 кг?
4c3h4(ono2)3 = 12co2 + 6n2 + 10 h20 + o2 + 5550 кдж рассчитайте какое количество теплоты выделится при взрыве 1 кг.
Взорвали смесь 10 мл водорода с 4 мл кислорода ?
Взорвали смесь 10 мл водорода с 4 мл кислорода .
Какой газ останется после взрыва ?
Какой его объем.
1. Найти количество вещества и массу 2, 4•1023 молекул кислорода?
1. Найти количество вещества и массу 2, 4•1023 молекул кислорода.
2. Какой объем кислорода можно получить при разложении 800 г оксида ртути?
3. Теплота сгорания ацетилена равна 1350 кДж / моль.
Какое количество теплоты выделится при сгорании ацетилена объемом 1 л (в пересчете на н.
В результате разложения карбоната кальция химическим количеством 1 моль поглотилось 157кДж теплоты?
В результате разложения карбоната кальция химическим количеством 1 моль поглотилось 157кДж теплоты.
Укажите сколько теплоты затрачивается на разложение известняка массой 1кг.
На разложении оксида ртути (II) массой 8, 68 г?
На разложении оксида ртути (II) массой 8, 68 г.
Затратили теплоту количеством 3, 64 кДж.
Составьте термохимическое уравнение реакции.
Взорвана смесь 10мл водорода с 4 мл кислорода?
Взорвана смесь 10мл водорода с 4 мл кислорода.
Какой газ останется после взрыва?
Каков его объем?
В результате реакции термохимическое уравнение которой 2AgNo3 = 2Ag + 2No2 + O2 — 317 кДж поглотилось 15, 85 кДж теплоты?
В результате реакции термохимическое уравнение которой 2AgNo3 = 2Ag + 2No2 + O2 — 317 кДж поглотилось 15, 85 кДж теплоты.
Масса выделившегося серебра равна ?
Согласно термическому уравнению реакции H2 + Cl = 2Hcl + 184 кДж при взаимодействии простых веществ выделилось 92 кДж теплоты?
Согласно термическому уравнению реакции H2 + Cl = 2Hcl + 184 кДж при взаимодействии простых веществ выделилось 92 кДж теплоты.
Объем полученного газа составил.
Определите объем при н?
Определите объем при н.
У. и массу выделившегося газа при разложении перманганата калия массой 17, 6 г.
Вопрос Разложение гремучей ртути при взрыве идет по уравнению Hg(ONC)2 = Hg + 2CO + N2 + 364, 2 кДж?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 — 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
Разложение гремучей ртути при взрыве идет по уравнениюHg(ONC)2 = Hg + 2CO + N2 + 364,2 кДж.Определит
Ответы на вопрос
Hg(ONC)2 = Hg + 2CO + N2 + 364,2 кДж решим задачу при помощи этого уравнения. Переведем 1.5 кг в граммы — 1500г тогда уравнение примет вид: V(N2)= 1500г*22.4л(это объем 1 моля азота)/284(M(Hg(OCN)2) = 118,3л. Найдем объем CO2 = 236.6л.
Количество теплоты будет по такому уравнению 284 — 364.2 кДж 1500г — х кДж
Крест на крест и умножаем 1500*284/364,2=1170 кДж
Фульминат ртути II
| Фульминат ртути II | |||
|---|---|---|---|
| |||
| Систематическое наименование | фульминат ртути | ||
| Традиционные названия | гремучая ртуть | ||
| Хим. формула | Hg(CNO)2 | ||
| Рац. формула | Hg(CNO)2 | ||
| Состояние | твёрдое | ||
| Молярная масса | 284.63 г/моль | ||
| Плотность | 4,3 г/см³ | ||
| Температура | |||
| • вспышки | 180 °C | ||
| • самовоспламенения | 130—150 °C | ||
| Рег. номер CAS | 628-86-4 | ||
| PubChem | 11022444 | ||
| Рег. номер EINECS | 211-057-8 | ||
| SMILES | |||
| ChEBI | 39152 | ||
| Номер ООН | |||
| ChemSpider | 9197626 | ||
| Токсичность | Чрезвычайно токсичен для человека | ||
| Пиктограммы ECB |    | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Фульминат ртути (гремучая ртуть) — ртутная соль фульминовой (гремучей) кислоты, инициирующее взрывчатое вещество.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Взрывчатые свойства
- 4 Применение
- 5 История
Получение
По сообщению Кункеля в 1609 году первое получение гремучей ртути состоялось ещё в XVII веке. Однако первенство открытия этого вещества принято считать принадлежащим английскому химику Говарду, который выделил его в 1800 году и впервые исследовал его свойства.
Гремучую ртуть получают взаимодействием нитрата ртути с этанолом в разбавленной азотной кислоте. Реакция протекает по схеме:
Для протекания реакции в реакционной смеси должны быть оксиды азота.
Физические свойства
Белый или серый кристаллический порошок, мало растворим в воде. Имеет сладкий металлический вкус, ядовит. Насыпная плотность 1,22-1,25 г/см³.
Взрывчатые свойства
Теплота разложения 1,8 МДж/кг. Температура вспышки — 180 °C. Нижний предел чувствительности при падении груза 700 г — 5,5 см, верхний — 8,5 см. Гравиметрическая плотность 4,39 г/см³. Легко взрывается при ударе, действии пламени, раскалённого тела и т. п. При осторожном нагревании гремучая ртуть медленно разлагается. При 130—150 °C самовоспламеняется со взрывом. Влажная гремучая ртуть гораздо менее взрывоопасна. Влажность гремучей ртути, запрессованной в капсюль-детонатор, должна быть не более 0,03 %. Гремучая ртуть хорошо растворима в водных растворах аммиака или цианистого калия. Концентрированная серная кислота вызывает взрыв одной каплей. Температура взрыва гремучей ртути равна 4810 °C, объём газов — 315 л/кг, скорость детонации — 5400 м/сек.
Применение
Применяют в капсюлях-детонаторах и капсюлях-воспламенителях. В последнее время гремучая ртуть вытесняется более эффективными инициирующими взрывчатыми веществами — азидом свинца и др.
История
Открыта гремучая ртуть в 1799 году английским химиком Эдвардом Говардом.
http://uznavalka.pro/subject/chemistry/q/7361022/Razlojenie-gremuchey-rtuti-pri-vzryve-idet-po-uravn.html
http://chem.ru/fulminat-rtuti-ii.html