Помогите написать уравнение реакции деполимеризации полиэтилена)?
Химия | 10 — 11 классы
Помогите написать уравнение реакции деполимеризации полиэтилена).
( — CH2 — CH2 — )n — — — > ; nCH2 = CH2.
Помогите пожалуйста?
Полиэтилен получают в результате реакции.
Какой реакцией получают полиэтилен и полипропилен?
Какой реакцией получают полиэтилен и полипропилен?
Напишите последовательность реакций получения полиэтилена из пропана?
Напишите последовательность реакций получения полиэтилена из пропана.
Какая формула реакции деполимеризации полиэтилена?
Какая формула реакции деполимеризации полиэтилена?
Помогите написать уравнения реакций?
Помогите написать уравнения реакций.
Напишите реакцию образования полиэтилена, полистирола?
Напишите реакцию образования полиэтилена, полистирола.
При какой реакции получают полиэтилен и какова его формула?
При какой реакции получают полиэтилен и какова его формула?
Написать уравнения реакций синтеза продуктов на основе : Этилена полиэтилен ^ этилен > ; этанол > ; хлорэтан > ; бутан ↓ ↓ дихлорэтан этановая кислота?
Написать уравнения реакций синтеза продуктов на основе : Этилена полиэтилен ^ этилен > ; этанол > ; хлорэтан > ; бутан ↓ ↓ дихлорэтан этановая кислота.
Напишите все хим?
Напишите все хим.
Реакции полиэтилена полистирола поливинилхлорида.
Напишите уравнение реакции метан — хлорметан — этан — этен — полиэтилен?
Напишите уравнение реакции метан — хлорметан — этан — этен — полиэтилен.
Вопрос Помогите написать уравнение реакции деполимеризации полиэтилена)?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 — 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
K2O — оксид калия (основные оксиды) BaO — оксид бария (основные оксиды) Al2(SO4)3 — сульфат алюминия (средние соли) NaHCO3 — гидрокарбонат натрия (кислые соли).
4P + 5O₂ = 2P₂O₅ P⁰ — 5e = P⁺⁵ 4 фосфор восстановитель, процесс окисления O₂ + 4e = 2O⁻² 5 кислород окислитель, процесс восстановления P₂O₅ + 3H₂O = 2H₃PO₄ P₂O₅ + 3H₂O = 2H⁺ + 2H₂PO₄⁻ H₃PO₄ + 3NaOH = Na₃PO₄ + 3H₂O H⁺ + H₂PO₄⁻ + 3Na⁺ + 3OH⁻ = 3Na⁺ + P..
Fe(OH)3 + 3HCl = FeCl3 + 3H2O n(Fe(OH)3) = 21. 4 / 107 = 0. 2моль по уравнению реакции n(HCl) в 3 раза больше n(fe(oh)3) n(hcl) = 0, 6 моль m = n * M m(hcl) = 0. 6 * 36. 5 = 21. 9г W = m(в — ва) / m(р — ра) m(р — ра) = m(в — ва) / W m(hcl)(ра — ..
HCl + H2O = H3O( + ) + Cl ( — ).
А) по уравнению при восстановлении 1моль оксида выделяется 80кДж теплоты , значит при восстановлении 5 моль = 80 * 5 = 400кДж б)1, 6г это 1, 6 / 64 = 0, 025моль оксида , теплоты будет 80 * 0, 025 = 2кДж.
Mr(SO3) = 32 + 3 * 16 = 80 W(S) = 32 / 80 = 0. 4 = 40% Mr(SO2) = 32 + 2 * 16 = 64 W(S) = 32 / 64 = 0. 5 = 50% В 0, 8 раза.
M(CuSO4) = 64 + 32 + 4 * 16 = 160 г / моль n(CuSO4) = 1. 6 / 160 = 0. 01 моль.
Деполимеризация полиэтилена
РЕФЕРАТ ПО дисциплине «ОСНОВЫ РЕСУРСОСБЕРЕГАЮЩИХ И ПРИРОДООХРАННЫХ ТЕХНОЛОГИЙ В ПЕРЕРАБОТКЕ ПЛАСТМАСС»
Тема: Получение мономеров из полимерных отходов. Виды полимерных отходов пригодные для деполимеризации. Целесообразность этой «химической » переработки.
| Студент группы ХЕМО 11-16 | А. М. Танташев |
| Преподаватель: | О. Б. Ушакова |
Деполимеризация — процесс превращения полимера в мономер или смесь мономеров. Все полимеры подвержены деполимеризации при высоких температурах, как следствие роста энтропии. Это химический процесс, связанный с разрывом молекулярных цепей полимера, который применяется для придания материалу новых свойств.[1]
Для отдельных видов отходов полимеров рациональными являются различные типы химической и термической переработки, заключающейся в конверсии исходных полимеров с образованием сырья для их производства или других ценных продуктов. Деполимеризация может намеренно применяться для утилизации отходов термопластов в целях получения мономеров и возвращения их в цикл синтеза полимеров. Продукты термической деструкции некоторых промышленных полимеров приведены в таблице:

Разрыв химических связей между атомами углерода может проходит по двум механизмам:
1) С внутримолекулярной миграцией атомов водорода, в результате которой образуются два осколка цепи: один с насыщенным концевым звеном, а другой с ненасыщенным. Эти так называемые случайные разрывы химических связей характерны , например для полиэтилена:
2) С разрывом цепи не в случайных местах, а у концов макромолекулы в результате, которого образуются мономеры или продукты, близкие по молекулярному весу к мономерам. Такая деструкция характерна для полистирола. Процесс идет уже при комнатной температуре и при повышении температуры скорость деполимеризации возрастает. [3]
Деполимеризация полиэтилена
Деполимеризация полиэтилена является обратимым процессом и, в ряде случаев, может применяться при изготовлении или соединении различных изделий.Фактически, данный процесс связан с размягчением материала, который затем может приобрести изначальную плотность и твердость. При деполимеризации полиэтилена наблюдается снижение молекулярного веса вещества и исчезновение летучих веществ, к которым относятся водород и двуокись углерода, при протекании данного процесса понижается вязкость вещества, а, в ряде случаев, увеличивается молекулярных вес. Процесс деполимеризации полиэтилена может происходить под воздействием тепла, света или других внешних воздействий. Следует отметить, что в случае не соблюдения условий проведения химической реакции, полимерный материал может разрушиться или потерять целый ряд своих свойств. Далеко не всегда процессы полимеризации могут быть обратимы, поэтому необходимо тщательно соблюдать условия проведения данной реакции. Известно, что под воздействием света различные виды полиэтилена могут довольно быстро разрушаться, при хранении данного вида полимерного материала на свету за 1 — 2 года пластик или пленка могут полностью превратиться в труху, поэтому при изготовлении полиэтилена используются различные присадки, позволяющие предотвратить деструкцию полиэтилена под воздействием света. В настоящее время многие ведущие химические концерны тщательно изучают процессы деполимеризации полиэтилена для того чтобы разработать новые методики защиты полимерных материалов от различных внешних воздействий. Кроме того, изучение данных процессов позволяет получить обилие информации, которая может быть использована при создании новых материалов. При проведении различных экспериментов, связанных с деполимеризацией полиэтилена, применяются разные современные методы исследований, которые могут быть связаны с использованием дорогостоящей аппаратуры. Кроме того, при проведении данных исследований активно применяются различные методы математического анализа и современное программное обеспечение, которое позволяет не только предсказать, но и обработать полученные результаты.
Реакции полимеризации
Синтетические полимеры (произведенные искусственным путем) химическая промышленность получает при помощи реакций полимеризации и поликонденсации.
В основе реакции полимеризации лежит процесс соединения (при помощи ковалентных связей) друг с другом мономеров (молекул низкомолекулярного соединения), которые и формируют высокомолекулярное соединение (синтетический полимер).
В ходе процесса полимеризации происходит раскрытие двойных связей в молекулах непредельных углеводородов, которые затем соединяются друг с другом в одну макромолекулу гигантских размеров. При разрыве двойной связи высвобождается атом с высокой реакционной активностью, называемый радикалом, у которого имеется непарный электрон. После этого, радикал соединяется с другим радикалом (при этом оба они получают парные электроны), давая тем самым старт образованию полимерной цепи.
Полиэтилен
Рассмотреть процесс полимеризации удобнее всего на примере полиэтилена, являющегося самым простым синтетическим полимером.
На первом этапе выполняется реакция дегидрирования, когда при высокой температуре в присутствии металлического катализатора этан превращается в этилен (от молекулы этана отщепляется два атома водорода, в результате чего формируется двойная связь):
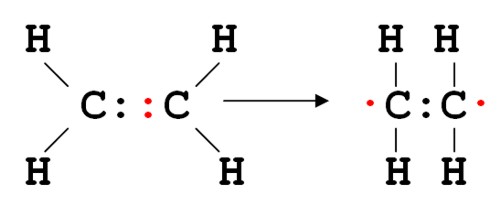
Образовавшийся этилен является мономером, который в дальнейшем будет использован для построения полимера (полиэтилена). Для этого этилен в присутствии катализатора подвергается высокому нагреву без доступа воздуха, что приводит к разрыву двойной углеродной связи, с образованием двух радикалов (на рисунке изображены красным цветом):
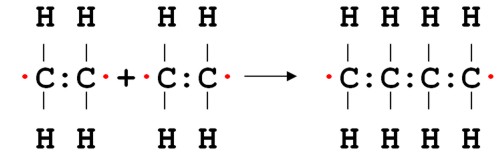
Образовашиеся радикалы тут же начинают «поиск» еще одного электрона, чтобы восстановить разорвавшуюся связь, что приводит к соединению двух радикалов друг с другом с образованием ковалентной связи. Данный процесс идет с обеих концов молекулы, что приводит к росту цепи (молекулярная масса молекулы полиэтилена достигает 10 000 — 1 000 000 г/моль):
Виды полиэтилена, которые можно получить путем реакции полимеризации:
- ПЭВД (полиэтилен высокого давления) или ПЭНП (полиэтилен низкой плотности), молекулярная масса 10 000 — 45 000. Состоит из сложной сети разветвленных полимерных нитей, поэтому, не упакован так плотно, как линейный полимер, являясь мягким и гибким. Основная область применения: упаковочный материал, обладающий высокой химической стойкостью.
- ПЭНД (полиэтилен низкого давления) или ПЭВП (полиэтилен высокой плотности), молекулярная масса 70 000 — 400 000. Состоит из линейных цепей, которые очень тесно упакованы, поэтому, обладает более высокой твердостью и прочностью. Основная область применения: изготовление детских игрушек, различных технических изделий, шлангов, труб и проч.
- ПЭПС (полиэтилен с поперечными связями). Состоит из линейных нитей, состоящих из мономеров, которые соединены друг с другом, что придает материалу высокую прочность. Открывая пластиковую бутылку Кока-Колы, будьте уверены, что крышечка, которой закрыта бутылка, сделана из ПЭПС.
Полипропилен
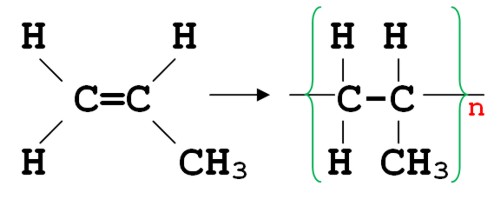
В структурной формуле пропилена один атом водорода замещен метиловой группой. Поскольку молекула пропилена имеет двойную связь, она также может участвовать в реакциях полимеризации (по аналогии с этиленом), образуя полипропилен.
Коэффициент n указывает число мономерных звеньев, из которых образована макромолекула. Говорят, что n выражает степень полимеризации.
В полипропилене CH3 является функциональной группой. Меняя условия полимеризации, можно создавать молекулы с функциональными группами, которые будут располагаться по-разному(с одной стороны молекулы; по обе ее стороны; в случайном порядке), получая, таким образом, молекулы пропилена с различными свойствами. Свойства полипропилена настолько сильно зависят от расположения в его молекуле метиловой группы, что из данного полимера получаются самые разные изделия, используемые для внутренней и внешней отделки помещений, изготовления корпусов для аккумуляторных батарей, бутылок, канатов и проч.
Поливинилхлорид
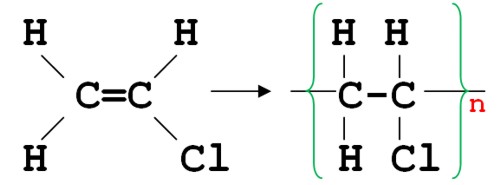
В структурной формуле винилхлорида один из атомов водорода заменен атомом хлора. Из винилхлорида путем реакции полимеризации получают поливинилхлорид (ПВХ):
ПВХ является очень прочным полимером, нашедшим широкое применение при изготовлении линолеума, игрушек, садовых шлангов, различных труб.
Полистирол
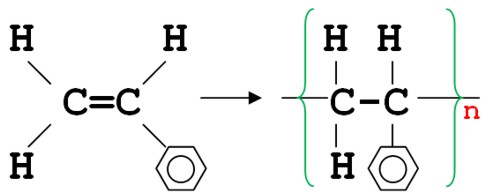
В молекуле стирола один атом водорода заменен бензольным кольцом. Из стирола при помощи реакции полимеризации получают полистирол (бесцветную твердую пластмассу с хорошими диэлектрическими свойствами):
Основное применение полистирола: изготовление посуды, пуговиц, упаковочных и электроизоляционных материалов. Полистирол трудно поддается рециркуляции, поэтому, «зеленые» активно выступают против его применения.
Политетрафторэтилен
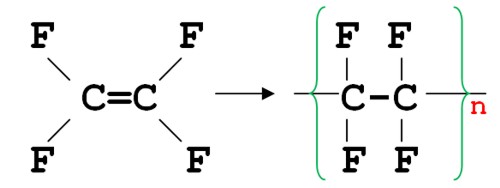
В молекуле тетрафторэтилена вместо атомов водорода присутствуют атомы фтора. При помощи реакции полимеризации из тетрафторэтилена получают политетрафторэтилен (тефлон или фторопласт):
Политетрафторэтилен обладает высокой стойкостью к щелочным и кислым средам, высокой жаропрочностью и очень гладкой поверхностью. Основное применение: изготовление подшипников, в качестве антипригарного покрытия сковородок и кастрюль.
Некоторые другие синтетические полимеры, получаемые при помощи полимеризации:
- Акрилонитрил → Полиакрилонитрил: парики, пряжа, ковры.
- Винилацетат → Поливинилацетат: текстильные покрытия, жевательная резинка, краска, латекс, клеющие средства.
- Метилметакрилат → Полиметилметакрилат: органическое стекло, контактные линзы.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://poisk-ru.ru/s9967t7.html
http://prosto-o-slognom.ru/chimia/39_reaktsii_polimerizatsii.html