Лабораторные органическая химия. Лабораторная работа 1 окси, оксокислоты гидроксикарбоновые кислоты опы Свойства молочной кислоты
| Название | Лабораторная работа 1 окси, оксокислоты гидроксикарбоновые кислоты опы Свойства молочной кислоты |
| Анкор | Лабораторные органическая химия .doc |
| Дата | 22.04.2017 |
| Размер | 0.81 Mb. |
| Формат файла |  |
| Имя файла | Лабораторные органическая химия .doc |
| Тип | Лабораторная работа #5376 |
| страница | 3 из 3 |
| Подборка по базе: Лабораторная работа-раб с вирт машинами.docx, курсовая работа.docx, Конттрольная работа по дисциплине Документирование.docx, Практическая работа.docx, Проектная работа.docx, ПРАКТИЧЕСКАЯ РАБОТА №1 ЗаданиеИностранный язык. Английский. Част, иностранный язык письменная работа.docx, Курсовая работаЭкономика организации.docx, Практическая работа Русский язык.docx, Лабораторная работа №1.pdf Опыт 27. Реакции на гидроксильные группы дисахаридов 27.2. Ацилирование дисахаридов (тяга). В сухой пробирке смешивают 0,5 г безводной лактозы и 0,5 г безводного ацетата натрия. К полученной смеси приливают 2,5 мл уксусного ангидрида, содержимое пробирки перемешивают и нагревают 5 мин при непрерывном встряхивании. Реакционную смесь охлаждают на воздухе и выливают в стакан с водой и льдом при тщательном перемешивании: По какому механизму идет эта реакция? Опыт 28. Реакции дисахаридов по карбонильной группе. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов Схема реакции окисления мальтозы реактивом Фелинга: Положительную реакцию с фелинговой жидкостью дают восстанавливающие дисахариды (мальтоза и лактоза), в водных растворах которых вследствие таутомерных переходов имеются свободные альдегидные группы. Раствор, содержащий сахарозу, при нагревании до начинающегося кипения не изменяет своей окраски, так как сахароза относится к невосстанавливающим дисахаридам и не окисляется реактивом Фелинга. Следует помнить, что длительное кипячение раствора сахарозы в щелочной среде приводит к ее расщеплению, и продукты гидролиза могут восстанавливать реактив Фелинга до оксида меди (I). Напишите уравнение реакции окисления лактозы реактивом Фелинга. 28.2. Получение фенилозазонов мальтозы и лактозы. В две сухие пробирки помещают по 100 мг (на кончике шпателя) смеси солянокислого фенилгидразина и безводного ацетата натрия (1:3). Затем в одну пробирку добавляют 1 мл 1%-ного раствора мальтозы, а в другую — 1 мл 1%-ного раствора лактозы при тщательном перемешивании. Пробирки помещают на кипящую водяную баню на 15—20 мин. При охлаждении на воздухе, а потом в стакане со льдом в реакционной смеси выпадают кристаллы фенилозазонов мальтозы и лактозы.
Напишите уравнение реакции образования фенилозазона лактозы. Кристаллы фенилозазонов мальтозы и лактозы рассматривают под микроскопом. Кристаллы озазона мальтозы имеют форму игл, частично образующих сферические скопления, а кристаллы фенилозазона лактозы — форму пластинок, образующих розетки. Зарисуйте кристаллы фенилозазонов мальтозы и лактозы в рабочий журнал. Опыт 29. Гидролиз (инверсия) сахарозы Для доказательства гидролитического расщепления сахарозы необходимо провести реакции, подтверждающие наличие в содержимом пробирки продуктов гидролиза. Для этого содержимое пробирки делят на две части. Первую часть раствора нейтрализуют 10%-ным раствором гидроксида натрия (контроль по универсальной индикаторной бумаге), а затем добавляют равный объем реактива Фелинга и нагревают верхнюю часть жидкости. Наблюдают образование красного осадка оксида меди (I). Для сравнения нагревают смесь исходного раствора сахарозы с равным объемом реактива Фелинга. Окраска раствора не изменяется. Этот опыт показывает, что в результате гидролиза сахарозы, не способной восстанавливать реактив Фелинга, образуется смесь моносахаридов, окисляющихся фелинговой жидкостью. Со второй частью гидролизата проводят реакцию Селиванова на наличие фруктозы, входящей в состав сахарозы (см. опыт 26.1). Опыт 30. Реакция сахарозы с сульфатами кобальта и никеля 3.3. ВЫСШИЕ ПОЛИСАХАРИДЫ В две пробирки наливают по 1 мл 1%-ных растворов полисаха-Ридов: в первую — крахмала, во вторую — гликогена. Затем добавляют равный объем реактива Фелинга. Жидкости тщательно перемешивают и нагревают верхнюю часть растворов до начинающегося кипения. Цвет растворов не изменяется. Молекулы полисахаридов содержат в своем составе большое число соединенных друг с другом при помощи гликозидных связей остатков моносахаридов. Молекулы крахмала (амилоза и амилопектин) содержат в среднем от 1000 до 300000 остатков D-глюкозы, в гликогене число остатков D-глюкозы доходит до нескольких миллионов. Однако в макромолекулах амилозы и амилопектина содержится всего по одному свободному гликозидному гидроксилу, который в растворе может дать альдегидную группу, поэтому концентрация альдегидных групп в растворе настолько мала, что крахмал не восстанавливает реактив Фелинга. В молекулах гликогена общее число глюкозных остатков выше, чем в молекулах амилопектина, поэтому он, как и крахмал, не обладает восстанавливающими свойствами. Опыт 32. Взаимодействие крахмала и гликогена с иодом Реакция крахмала и гликогена с иодом представляет собой сложный процесс. Синюю окраску с иодом дает амилоза — одна из фракций крахмала. Амилоза — полисахарид линейного строения, состоящий из остатков а, D-глюкопиранозы. Ее молекулы имеют структуру спирали, внутри которой есть свободный канал диаметром около 5 мкм, в него внедряются молекулы иода, образуя окрашенные комплексы («соединения включения») за счет взаимодействия с гидроксильными группами моносахаридных остатков. При нагревании молекулы амилозы теряют свою спиралевидную структуру, и окрашенные комплексы разрушаются, при охлаждении спиралевидная структура амилозы и, следовательно, окрашенные комплексы восстанавливаются. Для полисахаридов с разветвленными цепями (амилопектин и гликоген) наряду с процессами образования комплексов большое значение имеет процесс адсорбции иода на поверхности боковых цепей. Если боковые цепи в молекуле гликогена короткие, то развивается бурая окраска, если они длинные, то темно-красная. Опыт 33. Гидролиз крахмала Реактивы и оборудование: 1%-ный раствор крахмала, 10%-ный раствор серной кислоты, разбавленный раствор иода в иодиде калия (раствор Люголя), 10%-ный раствор гидроксида натрия, реактив Фелинга, универсальная индикаторная бумага; конические колбы на 100 мл, пипетки, мерные цилиндры на 50 и 10 мл, пробирки. Схема гидролиза крахмала: После того как реакционная смесь перестанет давать окраску с иодом, ее кипятят еще несколько минут, охлаждают и нейтрализуют 10%-ным раствором гидроксида натрия (контроль по универсальной индикаторной бумаге). Отливают в пробирку 1—2 мл гидролизата и добавляют равный объем реактива Фелинга. Верхнюю часть жидкости нагревают на пламени горелки до начинающегося кипения. Выпадает красный осадок оксида меди (I), что свидетельствует о наличии в растворе продуктов глубокого гидролиза крахмала — глюкозы и мальтозы. Напишите уравнения реакций окисления продуктов гидролиза крахмала фелинговой жидкостью. Опыт 34. Кислотный гидролиз клетчатки Реактивы и оборудование: концентрированная серная кислота, 10%-ный раствор гидроксида натрия, реактив Фелинга, универсальная индикаторная бумага; мелко нарезанная фильтровальная бумага, стеклянные палочки, водяные бани, пробирки. В сухую пробирку помещают несколько мелко нарезанных кусочков фильтровальной бумаги и приливают 1 мл концентрированной серной кислоты. Содержимое пробирки тщательно перемешивают стеклянной палочкой до полного разрушения бумаги и образования бесцветного вязкого раствора. После этого к нему осторожно при перемешивании по каплям добавляют 1 мл дистиллированной воды. Пробирку ставят на кипящую водяную баню. Смесь нагревают 10—15 мин при регулярном перемешивании. После охлаждения жидкость нейтрализуют 10%-ным раствором гидроксида натрия (контроль по универсальной индикаторной бумаге) и проводят с ней реакцию с фелинговой жидкостью (см. опыт 55.3) для обнаружения в продуктах гидролиза восстанавливающих Сахаров. Напишите уравнение реакции гидролиза целлюлозы и объясните опыт. Лабораторная работа №4 Опыт 35. Получение фурфурола и его свойства Фурфурол образуется из пентозанов, которые вместе с клетчаткой входят в состав древесины: С полученным раствором фурфурола проводят некоторые реакции. 35.2. На полоску фильтровальной бумаги наносят каплю анилина. В это же место добавляют каплю уксусной кислоты, а затем раствора фурфурола. Появляется пятно, окрашенное в красный цвет. 35.3. В пробирку наливают 1 мл аммиачного раствора гидроксида серебра (см. опыт 22.1) и добавляют 1—2 капли раствора фурфурола. Раствор нагревают на горячей водяной бане. Выпадает черный осадок металлического серебра. Напишите уравнение реакции взаимодействия фурфурола с аммиачным раствором гидроксида серебра. Подберите коэффициенты методом электронного баланса. Полоску белой хлопчатобумажной ткани смачивают водой, отжимают, а затем опускают в раствор «белого» индиго. Через несколько минут ткань вынимают, отжимают от избытка раствора и оставляют развешенной на воздухе. Постепенно «белое» индиго окисляется кислородом воздуха, и ткань окрашивается в синий цвет: К капле пиридина осторожно прибавляют концентрированную соляную кислоту. Реакционная смесь сильно разогревается, и выпадает белый осадок. К полученному осадку приливают воду. Наблюдают его растворение. Напишите уравнение реакции пиридина с соляной кислотой. 37.2. Образование солей пиридина. В две пробирки наливают по 1мл 2%-ных растворов хлорида железа (III) и сульфата меди и добавляют по 1—2 капли раствора пиридина, полученного в предыдущем опыте. В пробирке с хлоридом железа (III) выпадает осадок бурого цвета: В пробирке с сульфатом меди сначала выпадает голубой осадок В избытке пиридина осадок гидроксида меди (II) быстро ра- Опыт 38. Мочевая кислота Несколько кристаллов мочевой кислоты растворяют в 1—2 мл соляную кислоту. Сначала выпадают кристаллы малорастворимой Кристаллы мочевой кислоты имеют форму удлиненных призм. Во вторую пробирку добавляют равный объем фелинговой Реакция фелинга с лактозой уравнение
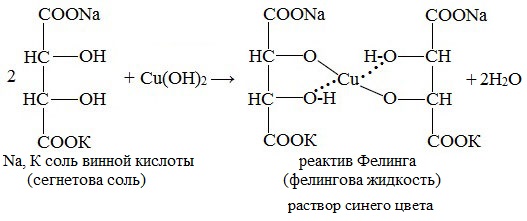
Приготавливается непосредственно перед анализом путем смешения двух растворов. Применяется для качественного и количественного определения альдегидов жирного ряда и в особенности моносахаридов. Действие реактива Фелинга основано на восстановлении иона двухвалентной меди до одновалентной за счёт окисления альдегидных групп исследуемых соединений. При этом на холоде выпадает оранжево-жёлтый осадок гидроксида меди (I) СuОН, а при нагревании – красный осадок оксида меди (I) Сu2O. Впервые был предложен в 1850 году немецким химиком Г. Фелингом. Реакция на моносахаридыГлюкоза окисляется свежеосажденным гидроксидом меди (II) в щелочной среде до глюконовой кислоты, восстанавливая ионы Cu +2 до Cu +1 . Углеводы подобного типа называют восстанавливающими. Эта реакция применяется для количественного определения сахаров в пищевых продуктах. Реакция на альдегидыАльдегиды жирного ряда восстанавливают двухвалентную медь в одновалентную. Ароматические альдегиды эту реакцию не дают. Образование реактива ФелингаРеактив Фелинга используется как качественная реакция для определения альдегидной группы. Характеристика химической активности углеводов.В соответствии с наличием функциональных групп сахара дают реакции характерные для альдегидов и многоатомных спиртов. Однако существование сахаров в различных таутомерных формах приводит к тому, что эти реакции проводят в иных условиях. Реакции на альдегидную группу 1.Реакции окисления( «серебряного зеркала»- (р-в Толленса) и реактивом Фелинга) – проводятся в тех же условиях, что и для альдегидов, но в присутствии очень малого количества щелочи (рН 7-8), т.к. избыток щелочи (рН 9-10) вызывает глубокие изменения в молекуле. Окисление в слабощелочной среде ведет у глюкозы к образованию глюконовой кислоты и окислению только по альдегидной группе:
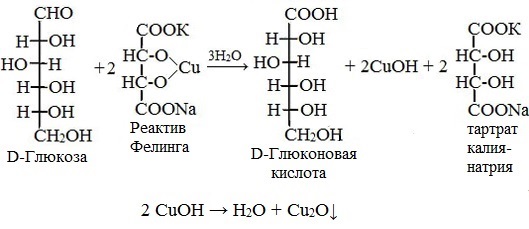
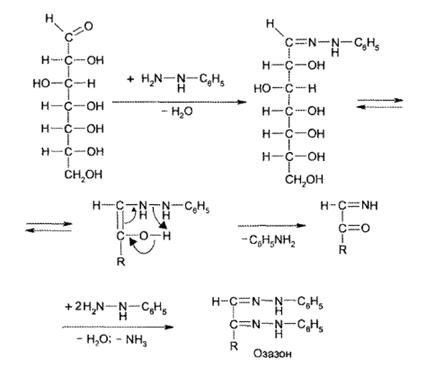
1) С реактивом Толленса (AgNO3 + 2NH4OH) при нагревании выпадает темный осадок серебра (глюкоза, галактоза, лактоза) 2) С реактивом Фелинга (глюкоза, галактоза, лактоза). При длительном стоянии или нагревании до кипения (по ФС) идет окислительно–восстановительная реакция с образованием кирпично-красного осадка Сu2O. (см. ФА альдегиды). Комплекс синего цвета желтый 2CuOH↓ → Cu2O↓ + H2O Желтый кирпично-красный осадок 2.Реакции конденсации. Окрашенные продукты конденсации получают при взаимодействии моносахаридов (или гидролизованных дисахаридов) а) с раствором антрона в концентрированной серной кислоте. Появляется зеленое окрашивание, постепенно переходящее в сине-зеленое. б) с трифенилтетразолия хлоридом (0,5%) в щелочной среде гидроксида натрия при нагревании только восстанавливающие сахара (глюкоза, галактоза, лактоза). Выпадает красный осадок трифенилформазана. в) с фенилгидразином – реакция образования озазонов. Растворы глюкозы, галактозы и лактозы образуют (альдегидная группа) выпадающие в осадок фенилгидразоны в кислой среде. При последующем нагревании на водяной бане в ходе перегруппировки и внутримолекулярной окислительно-восстановительной реакции получается окрашенный в желтый цвет осадок озазона. Озазоны – кристаллические вещества с четкой Т°пл. Реакция широко используется для установления подлинности восстанавливающих сахаров. Глюкоза взаимодействует с тремя молекулами фенилгидразина, а сахароза не дает положительной реакции. Реакции на спиртовую группу 1. Реакции этерификации по спиртовому гидроксилу. 2. Как многоатомные спирты образуют в присутствии эквивалентного количества натрия гидроксида глюкоза, галактоза и лактоза с раствором меди (II) сульфата растворимый комплекс синего цвета, сахароза с раствором кобальта (II) нитрата комплекс фиолетового цвета. источники: http://himija-online.ru/imennye-reakcii/reaktiv-felinga.html http://helpiks.org/5-7224.html |

















 Или
Или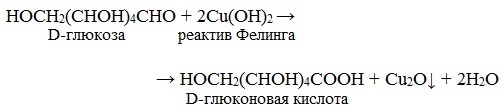
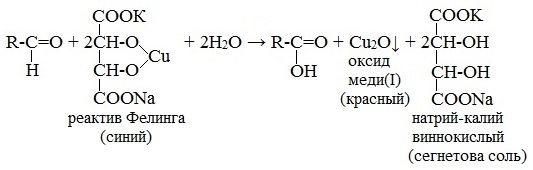
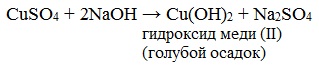




 НОН2С – (СНОН) – С рН 7-8
НОН2С – (СНОН) – С рН 7-8

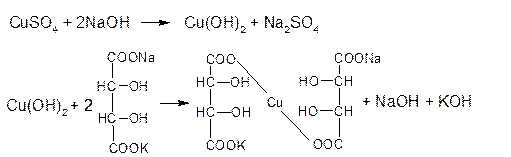



 или
или