Нитроглицерин: получение в лаборатории
Нитроглицерин — одно из наиболее известных взрывчатых веществ, основа состава динамита. Он нашел широкое применение во многих областях промышленности благодаря своим характеристикам, однако до сих пор одна из главных проблем, связанных с ним — вопрос безопасности.
История
История нитроглицерина начинается с итальянского ученого-химика Асканьо Собреро. Он впервые синтезировал это вещество в 1846 году. Первоначально ему было дано название пироглицерина. Уже Собреро обнаружил его большую неустойчивость — нитроглицерин мог взрываться даже от слабых сотрясений или ударов.
Мощность взрыва нитроглицерина теоретически делала его перспективным реагентом в горнодобывающей и строительной промышленностях — он был гораздо эффективнее существовавших на то время видов взрывчатки. Однако упомянутая нестабильность создавала слишком большую угрозу при его хранении и транспортировке — поэтому нитроглицерин отложили в долгий ящик.
Дело чуть сдвинулось с места при появлении Альфреда Нобеля и его семьи — отец и сыновья наладили промышленное производство этого вещества в 1862 году, невзирая на все опасности, связанные с ним. Однако случилось то, что должно было случиться рано или поздно — на фабрике произошел взрыв, и младший брат Нобеля погиб. Отец после перенесенного горя отошел от дел, однако Альфред сумел продолжить производство. Для повышения безопасности он смешивал нитроглицерин с метанолом — смесь была более стабильной, однако очень пожароопасной. Это все еще не было окончательным решением.
Им стал динамит — нитроглицерин, поглощенный кизельгуром (осадочной породой). Взрывоопасность вещества уменьшилась на несколько порядков. Позже смесь совершенствовалась, кизельгур заменяли более эффективными стабилизаторами, однако суть оставалось той же — жидкость поглощалась и переставала взрываться от малейших сотрясений.
Физические и химические свойства
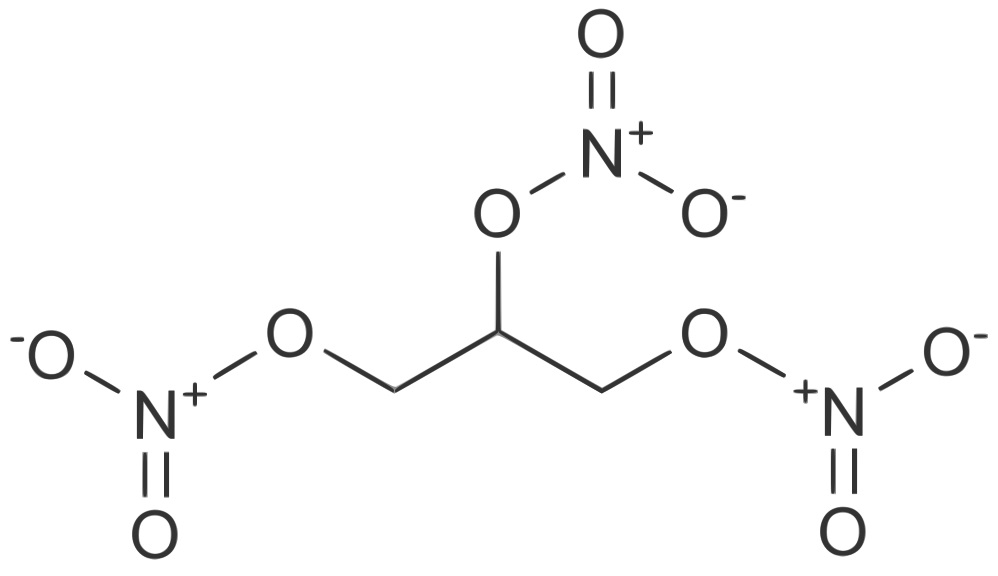
Нитроглицерин — это нитроэфир азотной кислоты и глицерина. В нормальных условиях это желтоватая, вязкая маслянистая жидкость. Нитроглицерин нерастворим в воде. Этим его свойством пользовался Нобель: чтобы после транспортировки подготовить нитроглицерин к применению и освободить его от метанола, он промывал смесь водой — метиловый спирт растворялся в ней и уходил, а нитроглицерин оставался. Это же свойство используют при получении нитроглицерина: водой продукт синтеза промывают от остатков реагентов.
Нитроглицерин гидролизуется (с образованием глицерина и азотной кислоты) при нагревании. Без нагревания идет щелочной гидролиз.
Взрывчатые свойства
Как уже было сказано, нитроглицерин крайне неустойчив. Однако здесь стоит сделать важное замечание: он восприимчив именно к механическому воздействию — взрывается от сотрясения или удара. Если просто поджечь его, жидкость, скорее всего, будет спокойно гореть без взрыва.
Стабилизация нитроглицерина. Динамит
Первым опытом по стабилизации нитроглицерина Нобеля был динамит — кизельгур полностью поглощал жидкость, и смесь была безопасной (до тех пор, конечно, пока ее не активируют в подрывной шашке). Причина, по которой используется именно кизельгур — капиллярный эффект. Наличие микротрубочек в этой породе обусловливает эффективное всасывание жидкости (нитроглицерина) и удержание ее там на долгое время.
Получение в лаборатории
Реакция получения нитроглицерина в лаборатории сейчас все та же, которой пользовался еще Собреро — этерификация в присутствии серной кислоты. Сначала берется смесь азотной и серной кислот. Кислоты необходимы концентрированные, с малым количеством воды. Далее к смеси малыми порциями при постоянном перемешивании постепенно добавляется глицерин. Температура должна поддерживаться низкая, так как в горячем растворе вместо этерификации (образования эфира) будет происходить окисление глицерина азотной кислотой.
Но так как реакция идет с выделением большого количества тепла, смесь необходимо постоянно охлаждать (обычно это делается с помощью льда). Как правило, она держится в районе 0 °С, превышение отметки в 25 °С может грозить взрывом. Контроль температуры осуществляется постоянно с помощью термометра.
Нитроглицерин тяжелее воды, однако легче минеральных (азотной и серной) кислот. Поэтому в реакционной смеси продукт будет лежать отдельным слоем на поверхности. После окончания реакции сосуд необходимо еще охладить, подождать, пока в верхнем слое не скопится максимальное количество нитроглицерина, а потом слить его в другую емкость с холодной водой. Затем идет интенсивная промывка в больших объемах воды. Это необходимо для того, чтобы как можно лучше очистить нитроглицерин от всех примесей. Это важно, потому что в комплекте с остатками непрореагировавших кислот взрывоопасность вещества увеличивается в несколько раз.
Промышленное получение
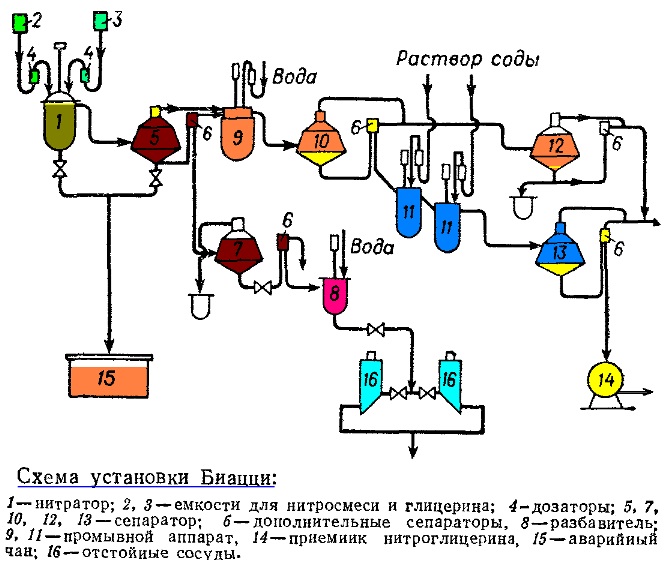
В промышленности уже давно довели до автоматизации процесс получения нитроглицерина. Система, которая используется в настоящее время, в основных своих аспектах была придумана еще в 1935 году Биацци (и так и называется — установка Биацци). Главные технические решения в ней — это сепараторы. Первичная смесь непромытого нитроглицерина сначала в сепараторе под действием центробежных сил разделяется на две фазы — ту, что с нитроглицерином, отбирают для дальнейшей промывки, а кислоты остаются в сепараторе.
Остальные этапы производства совпадают со стандартными. То есть, смешивание глицерина и нитрующей смеси в реакторе (производится с помощью специальных насосов, перемешивается турбинной мешалкой, охлаждение более мощное — с помощью фреона), несколько этапов промывки (водой и чуть подщелоченной водой), перед каждым из которых идет этап с сепаратором.
Установка Биацци достаточно безопасна и обладает достаточно высокой производительностью по сравнению с другими технологиями (однако обычно большое количество продукта теряется при промывке).
Домашние условия
К сожалению, хотя, скорее, к счастью, синтез нитроглицерина в домашних условиях связан со слишком большим количеством трудностей, преодоление которых в основном не стоит результата.
Единственный возможный способ синтеза в домашних условиях — получение нитроглицерина из глицерина (как и в лабораторном способе). И здесь основная проблема — серная и азотная кислоты. Продажа этих реактивов разрешена только определенным юридическим лицам и строго контролируется государством.
Возникает очевидное решение — синтезировать их самостоятельно. Жюль Верн в своем романе «Таинственный остров», рассказывая об эпизоде изготовления главными героями нитроглицерина, опустил конечный момент процесса, однако крайне подробно описал процесс получения серной и азотной кислот.
Действительно заинтересовавшиеся могут заглянуть в книгу (первая часть, глава семнадцатая), однако и тут загвоздка — необитаемый остров буквально изобиловал необходимыми реактивами, поэтому в распоряжении героев оказались серный колчедан, водоросли, много угля (для обжига), калийная селитра и так далее. Будет ли это у среднестатистического увлекающегося человека? Вряд ли. Поэтому домашний нитроглицерин в абсолютном большинстве случаев остается лишь мечтой.
Что такое нитроглицерин? Взрывчатка, спасающая жизнь
Век XIX был веком торжества металлургии и химии. Заводы становились все крупнее, производилось все больше стали, строились новые мосты и дороги, тоннели и все более глубокие шахты. И в рытье новых тоннелей, строительстве новых дорог, выработке новых шахт большую роль сыграл нитроглицерин, а потом и созданный на его основе динамит.
А как обрадовались генералы, узнав, что вместо слабого дымного пороха теперь в бомбы можно положить намного более мощную взрывчатку!
Изобретение

Фото: ru.wikipedia.org
Итальянский химик Асканио Собреро, работавший в Туринском университете, проводил опыты по реакции между глицерином и смесью азотной и серной кислот. Смесь этих кислот сегодня называют «нитрующей смесью», ее воздействие на многие вещества создает новые вещества, часто очень неустойчивые и склонные к самопроизвольной детонации.
Взаимодействие глицерина с нитрующей смесью породило в 1846 году нитроглицерин. В 1847 году автор выступил с докладом об изобретении. В ходе проверки свойств нового вещества произошел взрыв, изуродовавший автору изобретения лицо. А в 1850 году в Турин в лабораторию приехал молодой Альфред Нобель и начал изучать производство нитроглицерина.
В то же время Нобели изучали и работу российских химиков, исследовавших возможность уменьшения чувствительности нитроглицерина. Нобели придумали способ подрыва нитроглицерина, создав капсюли-детонаторы на основе гремучей ртути. 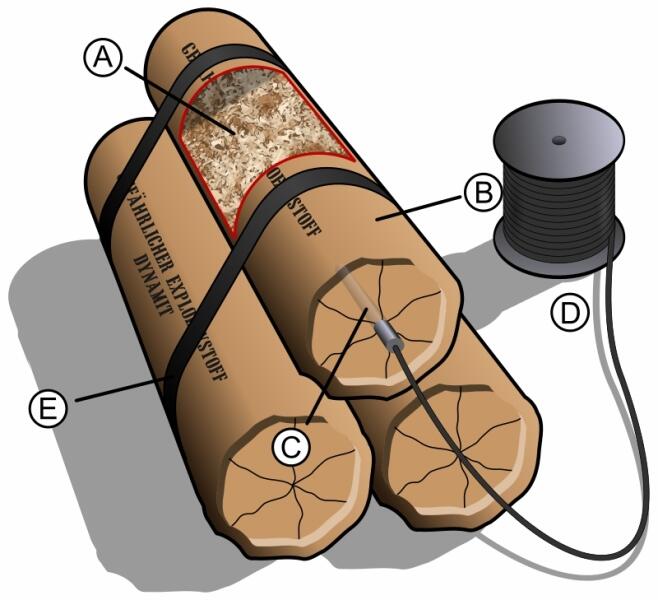
Фото: ru.wikipedia.org
Применение в медицине
При изучении свойств созданного вещества Асканио Собреро установил, что вещество обладает сладким вкусом и вызывает сильную головную боль. Сегодня врачи понимают, что эта боль вызвана снижением артериального давления. Но эти симптомы не были правильно интерпретированы тогдашними врачами.
Лишь в 1858 году в Англии врач Альфред Филд прописал пациентке 68 лет нитроглицерин от стенокардии, чтобы уменьшить боль в груди. Он прописал ей новый препарат «глоноин», как тогда называли в фармакологии нитроглицерин. Однако в жидком виде употреблять препарат было очень неудобно. В том числе и из-за его склонности к детонации при встряхивании: попытался вытряхнуть в стакан каплю — и взрыв разнес в клочья всё в комнате.
Но история лекарства скоро продолжилась: новым препаратом заинтересовался врач из Лондона Вильям Мюррел. Он обратился к химику В. Мартиндейлу, который сумел придать нитроглицерину форму мелких стабильных гранулок. Пациент взял на язык одну гранулку — и боль в груди прекратилась. Если нет, то принять еще одну гранулку, рассосав ее на языке. Первое сердечное лекарство состоялось! 
А понять, что этот нитроглицерин делает и почему сердце перестает болеть, сумели только в самом конце XX века три исследователя из США: Луис Игнарро, Роберт Фёрчготт и Ферид Мьюрэд, за что они и получили в 1998 году Нобелевскую премию по медицине и физиологии.
Оказывается, в организме человека нитроглицерин освобождает оксид азота, который расслабляет гладкомышечные клетки, что приводит к расширению кровеносных сосудов.
Создание динамита
Нобели придумали пропитывать нитроглицерином различные пористые материалы.
Одновременно с ними в других странах, в том числе и в России, проводились аналогичные исследования.
В России полковник Петрушевский создал в 1868 году магнезиальный динамит: нитроглицерин впитывался в пористый порошок магнезии — и получалось мощное взрывчатое вещество, которое можно было провозить к месту применения, не опасаясь встряхнуть ящик с динамитом. А на месте динамитные шашки можно было взорвать с помощью капсюля-детонатора. 
Фото: ru.wikipedia.org
В том же 1868 году динамит на базе кизельгура (кремнистой земли) начали производить и Нобели. И взяли на динамит патент, став официальными изобретателями новой взрывчатки.
Взрывчатые работы при помощи динамита, особенно при подземных работах, были намного безопаснее, чем взрывные работы при помощи пороха. Порох горит намного медленнее и его вспышка часто воспламеняла в шахтах рудничный газ, что влекло подземные взрывы. А мгновенная детонация динамита рудничный газ не успевала поджечь.
Динамит был нарасхват, за первые 8 лет его производство выросло в 800 раз — от примерно 10 тонн в год до 8000 тонн. И на этом производстве уже работала не одна небольшая фабрика, а несколько десятков фабрик. Генералы начали потирать руки в предвкушении боевого применения…
Боевое применение
Попытка заложить динамит в пушечный снаряд провалилась — слишком часто снаряды взрывались при выстреле. Зато для производства мин, для начала — морских, а также для подрыва крепостных стен, мостов, тоннелей — динамит отлично подходил.
Во франко-прусской войне 1870−1871 годов динамит уже использовался в больших масштабах. 
Фото: ru.wikipedia.org
Расширение производства динамита сопровождалось взрывами на производстве. Взрывались заводы, гибли люди, нитроглицерин — все же очень взрывоопасное вещество. А динамит при ненадлежащем хранении или долгом хранении «отпотевает», на его поверхности выступают капельки нитроглицерина — и тут до взрыва всего склада взрывчатки остается совсем чуть-чуть.
Пытаясь уменьшить взрывоопасность динамита, исследователи создали желатин-динамит — при взаимодействии нитроглицерина и желеобразной массы, получаемой при разведении коллодия различными органическими растворителями. Желатин-динамиты, или «гремучие студни», широко использовались при строительстве тоннелей в Альпах. И туннель под перевалом Сен-Готард, и все остальные туннели, пробитые людьми в то время, своей прокладкой во многом обязаны «гремучим студням». 
Фото: ru.wikipedia.org
Триумф и закат эпохи динамита
В конце XIX — начале XX века динамит был главной взрывчаткой мира.
Ручные гранаты — динамит. Террористические акты ирландцев в Великобритании и революционеров в России — динамит. Морские мины — динамит.
Но в самом конце XIX века ученые начали исследовать свойства тринитротолуола и гексогена. Более мощные, чем динамит, хранящиеся намного дольше, намного более стабильные. Эту взрывчатку можно было поместить в артиллерийский снаряд, в торпеду, в мину, в ручную гранату.
Век динамита почти закончился — осталось еще применение при прокладывании тоннелей, при постройке шахт.
Динамит производят и сегодня. Но в общей массе производимой в мире взрывчатки на динамит приходится только 2%.
Зато все до сих пор помнят Нобелей. В основном благодаря Нобелевской премии.
Даже шутливая премия Ignobel получила свое название именно от Нобеля.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://www.shkolazhizni.ru/world/articles/94819/ http://acetyl.ru/f/r199.php |