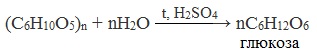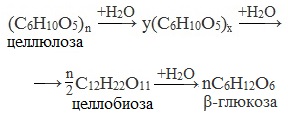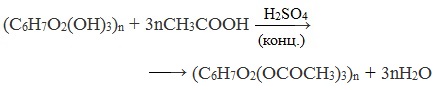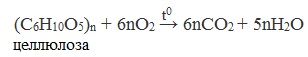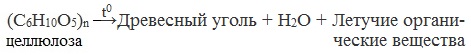Реакция окисления целлюлозы уравнение реакции
Окисление целлюлозы — одна из ее важнейших реакций, представляющая большой научный и практический интерес.
С реакцией окисления целлюлозы мы сталкиваемся при отбелке и облагораживании целлюлозы, при получении вискозного и медно-аммиачногс волокна и в целом ряде других производств целлюлозно-бумажной и текстильной промышленностей.
В процессе окисления в макромолекулу целлюлозы вводятся новые функциональные группы (например, альдегидные), благодаря чему окисленная целлюлоза обладает целым рядом новых свойств, из которых одни являются нежелательными, а другие представляют практический и научный интерес. Наличие в окисленной целлюлозе негидроксильных функциональных групп значительно расширяет возможности синтеза новых производных целлюлозы и модификации ее свойств. Большого внимания заслуживает обработка окисленных целлюлоз боргидридом — сильным избирательным восстановителем, способным восстанавливать карбонильные группы до гидроксильных.
В настоящей главе рассматриваются возможные направления реакции окисления целлюлозы, действие на нее различных окислителей, химизм отбелки целлюлозы и вопросы восстановления окисленных целлюлоз.
Возможные направления реакции окисления целлюлозы
Целлюлоза очень чувствительна к действию окислителей. Причиной этого является наличие в каждом элементарном звене макромолекулы целлюлозы трех гидроксильных групп.
L/oh HL н Л1о- ■■ — — о сн, он 6 1
Положение и свойства этих групп обусловливают многообразие направлений реакции окисления и получаемых в результате реакции продуктов.
Теоретически можно наметить следующие основные направления окислительных реакций £5 2′ 62]:
1. Воздействие окислителя на функциональную группу первого углеродного атома. Это может произойти только у конечного звена цепи и поэтому при обычном окислении имеет второстепенное значение. Оно, однако, может заметно проявиться, когда окисление происхо
дит в сильнокислой среДе, где имеет место одновременное гидролитическое расщепление макромолекул целлюлозы.
Некоторые авторы [3] считают, что окисление по первому углеродному атому имеет большое значение в промышленно важной реакции щелочного старения аркали — целлюлозы (гл. XI), где конечные группы макромолекул являются точками начала реакции.
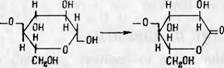
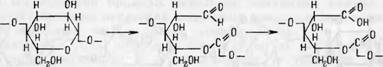
Окисление функциональной группы у первого углеродного атома может привести в конечном итоге к образованию карбоксильной группы
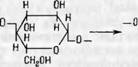
2. Одновременное окисление гидроксильных групп у второго и третьего углеродных атомов с разрывом пиранового кольца и образованием альдегидных групп с дальнейшим возможным окислением образовавшихся альдегидных групп до карбоксильных
-|/ Н н’н — о Y Чон Н0/ i
3. Окисление гидроксильных групп у второго и третьего углеродных атомов без разрыва пиранового кольца с образованием одной или двух кетонных групп
4. Окисление гидроксила у шестого углеродного атома с образованием альдегидной группы и с возможным дальнейшим окислением до карбоксильной группы
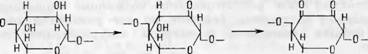
5. Открытие пиранового кольца между первым и пятым углеродными атомами и окисление по первому углеродному атому
TOC o «1-3» h z HxC-0HH0LU
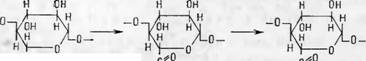
6. Окисление с разрывом углеродной связи между первым и вторым углеродными атомами с образованием группы углекислого эфира
7. Присоединение кислорода к «кислородному мостику» между элементарными звеньями макромолекулы целлюлозы с образованием перекиси и последующим разрывом макромолекулы целлюлозы.
Только немногие из изученных окислителей обладают более или менее специфическим воздействием; в большинстве случаев окисление идет сразу в нескольких направлениях и иногда сопровождается гидролизом.
Благодаря легкости окисления целлюлозы практически все образцы выделенных целлюлоз содержат в небольшом количестве альдегидные и карбоксильные группы.
Международный комитет по анализам целлюлозы приводит следующие результаты анализов 8 «стандартных» целлюлоз [4] (табл. 49)
При первом углеродном атоме и альдегидной группы при втором углеродном атоме, с ее возможным окислением до карбоксильной
Данные анализов «стандартных» беленых целлюлоз
Альдегидные группы, мил — лимоль/г
Карбоксильные группы, милли — моль/г
Хлопковый линтер (для ацетилирования) .
Сульфитная (для ацетилирования) Предгидролизованная сульфатная
(для шинного корда)…………………………
Сульфитная (для целлофана) . . . Сульфитная (березовая, вискозная)
Сульфитная (для бумаги)………………………
0.0050+ 0.0001 0.0067+ 0.0002
0.0072+0.0002 0.0124+0.0001 0.0109+0.0001 0.0167+0.0001 0.0124+0.0001 0.0275+0.0001
0.0050+ 0.0001 0.0162+0.0001
0.0148 + 0.0002 0.0204+0.0004 0.0294+0.0008 0.0442 +0.0016 0.0553+0.0030 0.0726+ 0.0047
820+14 940+7 660+7 820+7 1250+15 1240+7
Примечание. Альдегиды определялись путем окисления целлюлозы КаСЮг; карбоксилы — путем абсорбции метиленовой сини; СП — медноаммиачным методом с пересчетом по формуле Батисты,
Из этих данных видно, что в древесной целлюлозе содержание альдегидных и карбоксильных групп выше, чем в хлопковой. Рэнби считает [5] что более высокое содержание карбонилов и карбоксилов в древесной целлюлозе является основной причиной более высокой скорости гидролиза [19] древесной целлюлозы по сравнению с хлопковой в связи с индуктивным влиянием этих электрофильных групп. Некоторые из этих групп вводятся в процессе очистки, в то время как другие имеют, по мнению Рэнби, естественное происхождение (менее 1 группы на 100 глюкозных единиц). В пользу этого соображения говорит тот факт, что восстановление древесной целлюлозы боргидридом натрия приводит к уменьшению скорости гидролиза почти до значения скорости гидролиза хлопковой целлюлозы f61]. Иванов полагает [6], что строение молекулы целлюлозы должно изображаться структурной формулой, содержащей, кроме неизмененных глюкозных остатков, небольшое количество глюкозных остатков с негидроксильными группами у второго, третьего и шестого углеродных атомов.
Комментирование записей временно отключено.
Реакция окисления целлюлозы уравнение реакции
Целлюлоза (клетчатка) — растительный полисахарид, являющийся самым распространенным органическим веществом на Земле.
Этот биополимер обладает большой механической прочностью и выполняет роль опорного материала растений, образуя стенку растительных клеток.
Состав целлюлозы, так же как и крахмала, выражается формулой (C6H10O5)n .
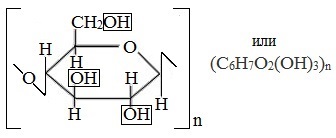
Строение целлюлозы
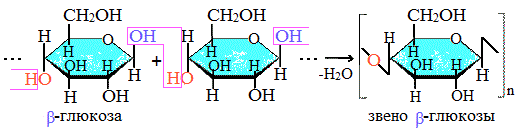
Макромолекулы целлюлозы – это длинные цепи, состоящие из большого числа остатков β–глюкозы, связанных β-1,4-гликозидными связями.
Молекулярная масса целлюлозы — от 400 000 до 2 млн.
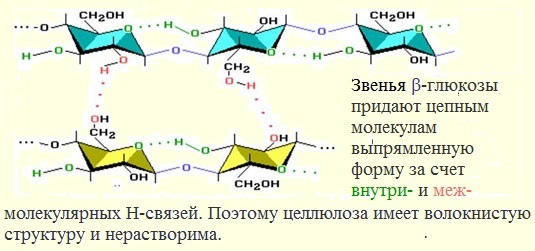
Молекулы целлюлозы, в отличие от крахмала, имеют линейное (неразветвленное) строение, вследствие чего целлюлоза легко образует волокна.
Нахождение в природе
Целлюлоза была обнаружена и описана французским химиком Ансельмом Пайеном в 1838 году.
В большом количестве целлюлоза содержится в тканях древесины (40-60%), в волокнах льна (60-85%) и хлопка (95-98%), в вате и фильтрованной бумаге – до 90%. Основная составная часть оболочки растительных клеток. Образуется в растениях в процессе фотосинтеза.
Древесина состоит на 50% из целлюлозы, а хлопок и лён, конопля практически чистая целлюлоза.
Хитин (аналог целлюлозы) – основной компонент наружного скелета членистоногих и других беспозвоночных, а также в составе клеточных стенок грибов и бактерий.
Физические свойства целлюлозы
Целлюлоза – твердое волокнистое вещество белого цвета, без вкуса и запаха, нерастворимое в воде и органических растворителях, но хорошо растворимое в аммиачном растворе гидрокисда меди (II) (реактив Швейцера). Из этого раствора кислоты осаждают целлюлозу в виде волокон (гидратцеллюлоза).
Волокна целлюлозы обладают высокой механической прочностью, так как она является основной составной частью стенок и клеток растений.
В отличие от крахмала она не может служить человеку пищей, поскольку не расщепляется в его организме под действием ферментов.
Видеоопыт «Растворение целлюлозы в аммиачном растворе гидроксида меди (II)»
Химические свойства целлюлозы
1. Гидролиз целлюлозы
Подобно крахмалу, целлюлоза при нагревании с разбавленными кислотами подвергается гидролизу. Гидролиз целлюлозы происходит при нагревании в кислой среде. Конечным продуктом гидролиза является глюкоза.
При длительном нагревании с минеральными кислотами или под действием ферментов (у жвачных животных) идет ступенчатый гидролиз целлюлозы:
Видеоопыт «Кислотный гидролиз целлюлозы»
Гидролиз целлюлозы, иначе называемый осахариванием, — очень важное свойство целлюлозы, он позволяет получить из древесных опилок и стружек глюкозу, а сбраживанием последней – этиловый спирт. Этиловый спирт, полученный из древесины, называется гидролизным.
2. Образование сложных эфиров (реакция этерификации)
Целлюлоза также не дает реакцию «серебряного зеркала» (нет альдегидной группы), но для нее характерны реакции образования сложных эфиров.
Каждое структурное звено целлюлозы содержит три свободных гидроксила.
Следовательно, целлюлоза может вступать в реакции, характерные для многоатомных спиртов.
Наибольшее практическое значение имеют реакции с азотной кислотой и уксусным ангидридом.
а) Нитрование
При обычной температуре целлюлоза взаимодействует лишь с концентрированными кислотами.
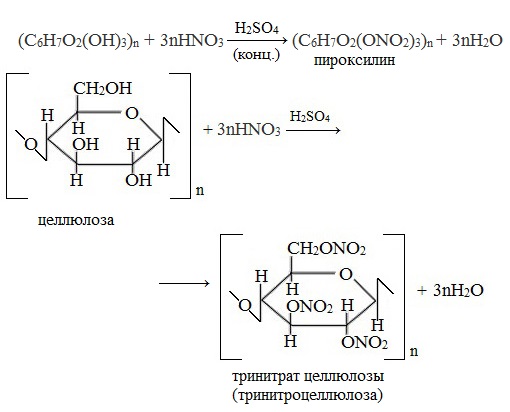
При взаимодействии целлюлозы с концентрированной азотной кислотой в присутствии концентрированной серной кислоты в качестве водоотнимающего средства образуется сложный эфир -тринитрат целлюлозы:
Видеоопыт «Получение и свойства нитроцеллюлозы»
Полностью этерифицированная клетчатка – это тринитрат целлюлозы (пироксилин) – взрывчатое вещество, на его основе изготавливают бездымный порох.
В зависимости от условий нитрования можно получить динитрат целлюлозы, который в технике называется коллоксилином. Он так же используется при изготовлении пороха и твердых ракетных топлив. Кроме того, на основе коллоксилина изготавливают целлулоид.
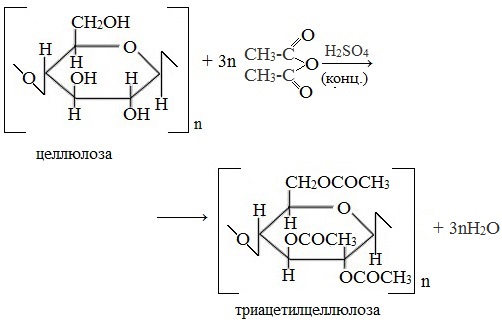
в) Взаимодействие с уксусным ангидридом
При взаимодействии целлюлозы с уксусным ангидридом в присутствии уксусной и серной кислот образуется триацетилцеллюлоза:
Из триацетата целлюлозы изготавливают лаки, кинопленку и ацетатное волокно.
3. Горение – полное окисление
4. Термическое разложение целлюлозы без доступа воздуха
Получение целлюлозы
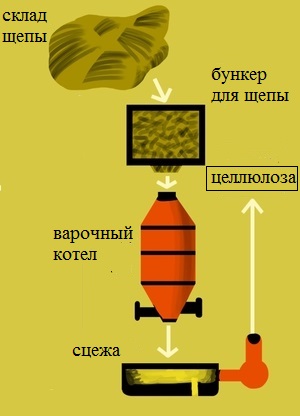
Промышленным методом целлюлозу получают методом варки щепы на целлюлозных заводах, входящих в промышленные комплексы (комбинаты). По типу применяемых реагентов различают следующие способы варки целлюлозы:
- Кислые:
- Сульфитный. Варочный раствор содержит сернистую кислоту и её соль, например гидросульфит натрия. Этот метод применяется для получения целлюлозы из малосмолистых пород древесины: ели, пихты.
- Щелочные:
- Натронный.Используется раствор гидроксида натрия. Натронным способом можно получать целлюлозу из лиственных пород древесины и однолетних растений. Преимущество данного метода — отсутствие неприятного запаха соединений серы, недостатки — высокая стоимость получаемой целлюлозы. Метод практически не используется.
- Сульфатный.Наиболее распространенный метод на сегодняшний день. В качестве реагента используют раствор, содержащий гидроксид и сульфид натрия, и называемый белым щелоком. Свое название метод получил от сульфата натрия, из которого на целлюлозных комбинатах получают сульфид для белого щёлока. Метод пригоден для получения целлюлозы из любого вида растительного сырья. Недостатком его является выделения большого количества дурно пахнущих сернистых соединений: метилмеркаптана, диметилсульфида и др. в результате побочных реакций.
Получаемая после варки техническая целлюлоза содержит различные примеси: лигнин, гемицеллюлозы. Если целлюлоза предназначена для химической переработки (например, для получения искусственных волокон), то она подвергается облагораживанию — обработке холодным или горячим раствором щелочи для удаления гемицеллюлоз.
Для удаления остаточного лигнина и придания целлюлозе белизны проводится её отбелка. Традиционная для 20 века хлорная отбелка включала в себя две ступени:
- обработка хлором — для разрушения макромолекул лигнина;
- обработка щелочью — для экстракции образовавшихся продуктов разрушения лигнина.
Применение целлюлозы
Целлюлоза используется в производстве бумаги и картона, искусственных волокон, пленок, пластмасс, лакокрасочных материалов, бездымного пороха, взрывчатки, твердого ракетного топлива, для получения гидролизного спирта и многое другое.
- Изготовление нитей, канатов, бумаги.
- Получение глюкозы, этилового спирта (для получения каучука).
- Получение ацетатного шёлка – искусственное волокно, оргстекла, негорючей плёнки из ацетилцеллюлозы.
- Получение бездымного пороха из триацетилцеллюлозы (пироксилин).
- Получение коллодия (плотная плёнка для медицины) и целлулоида (изготовление киноленты, игрушек) из диацетилцеллюлозы.
Производные целлюлозы
К важнейшим производным целлюлозы относятся искусственные полимеры/
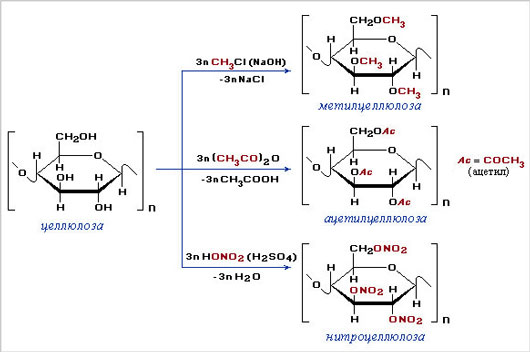
Метилцеллюлоза (простые метиловые эфиры целлюлозы) общей формулы
Ацетилцеллюлоза (триацетат целлюлозы) – сложный эфир целлюлозы и уксусной кислоты
Нитроцеллюлоза (нитраты целлюлозы) – сложные азотнокислые эфиры целлюлозы
Вискозное волокно. Целлофан
Эти полимерные материалы состоят из практически чистой целлюлозы, но для их получения исходную целлюлозу путем химической модификации сначала превращают в растворимую форму, а затем в процессе формования восстанавливают.
Экология СПРАВОЧНИК
Информация
Добавить в ЗАКЛАДКИ
| Поделиться: | Окисленная целлюлозаОкисленные целлюлозы более чувствительны к действию разрушающих агентов и оказываются стабильными в более узком интервале pH и температуры [7, 8].[ . ] Окисление целлюлозы — одна из важнейших ее реакций, имеющая большое теоретическое и практическое значение. Реакции окисления протекают при отбелке и облагораживании технических целлюлоз, при предсозревании щелочной целлюлозы в производстве вискозного волокна и в ряде других производств. При отбелке техническую целлюлозу обрабатывают хлором в присутствии воды, различными соединениями хлора и другими окислителями с целью удаления остаточного лигнина и других окрашивающих целлюлозу примесей. Целлюлоза при этом также подвергается воздействию окислителей. Облагораживание технической целлюлозы заключается в обработке ее разбавленным раствором едкого натра при нагревании с целью удаления примесей гемицеллюлоз и продуктов распада целлюлозы. В щелочной среде целлюлоза легко поддается окисляющему действию кислорода воздуха.[ . ] Целлюлоза подвергается действию окислителя из-за наличия в каждом элементарном звене трех спиртовых гидроксильных групп. В результате их окисления в макромолекулах целлюлозы образуются новые функциональные группы — карбонильные и карбоксильные, что приводит к появлению у окисленной целлюлозы новых свойств.[ . ] Окисление целлюлозы под действием кислорода воздуха в растворе куприэтилендиамина (Сиеп) идет намного медленнее, чем в медноаммиачном растворе. Стабильность самого растворителя также значительно выше, чем медноаммиачного раствора.[ . ] Целлюлоза в медноаммиачном растворе очень чувствительна к окислению кислородом воздуха. В результате окисления происходит деструкция целлюлозы и снижается вязкость ее раствора. Поэтому при определении вязкости медноаммиачных растворов необходимо максимально сокращать время контакта раствора с воздухом. Иногда добавляют к медноаммиачному реактиву различные восстановители, препятствующие окислению целлюлозы кислородом воздуха.[ . ] Окисление целлюлозы некоторыми типами окислителей (йодная кислота и ее соли, тетраацетат свинца, двуокись азота) может быть использовано для синтеза ряда производных целлюлозы, содержащих альдегидные или карбоксильные группы преимущественно у определенных углеродных атомов элементарного звена макромолекулы. Необходимо, однако, отметить, что в некоторых из образующихся при окислении соединений, например в продукте окисления целлюлозы йодной кислотой — диальдегидцеллюлозе и ее производных, пиранозный цикл, наличие которого является характерной особенностью химической структуры целлюлозы, разрушен в процессе окисления.[ . ] Окисление целлюлозы — обычно нежелательная реакция, однако в ряде случаев ее проводят преднамеренно, например, для снижения вязкости при отбелке вискозной целлюлозы; для снижения степени полимеризации и повышения молекулярной однородности целлюлозы (предсозревание щелочной целлюлозы в вискозном производстве); для получения продуктов с повышенными ионообменными свойствами; для синтеза новых производных целлюлозы.[ . ] Для окисления целлюлозы могут быть применены газообразная двуокись азота 02, жидкий азотноватый ангидрид К204, или раствор азотноватого ангидрида в индифферентном органическом растворителе. Способы проведения окисления также могут быть различны. Ниже приводится методика окисления целлюлозы так называемым статическим способом — в закрытом сосуде; этот способ значительно проще динамического, при котором окислитель непрерывно циркулирует через целлюлозу [3].[ . ] При окислении целлюлозы перйодатом, а затем двуокисью азота [133, 134] получен продукт, названный «трикарбоксилцеллю-лозой». Этот продукт содержал 50,8% карбоксильных групп (около 75% от теоретически возможного максимального количества). Трикарбоксилцеллюлоза растворима в разбавленных растворах щелочи; обменная емкость ее— 11,4 мэкв/г.[ . ] При окислении целлюлозы окислителями (шпохлорбитами, хлором, перманганатом калия и многими другими) образуются продукты, получившие название оксицеллюлозы. В химическом отношении они также являются сложной смесью разных продуктов окислительного и гидролизного распада.[ . ] Частично окисленная целлюлоза, представляющая собой смесь продуктов различной степени окисления, называется оксицеллюлозой.[ . ] Продукты окисления целлюлозы всегда химически и физически неоднородны. В процессе окисления обычно получается смесь исходной целлюлозы с продуктами ее окисления, называемая оксицеллюлозой.[ . ] Механизм окисления [841 N2O4 является, по-видимому, результатом окислительной денитрации ранее образовавшегося нитрата. Денитрация идет за счет двуокиси азота, а азотная кислота играет роль катализатора. Детальное рассмотрение химических реакций, происходящих при образовании оксицеллюлоз путем окисления целлюлозы двуокисью азота, приведено в главе VII.[ . ] Механизм окисления целлюлозы двуокисью азота исследован рядом авторов. На основании изучения ультрафиолетовых спектров продуктов окисления целлюлозы двуокисью азота Павлюченко, Ермоленко и Капуцкий [120] сделали вывод об образовании на начальной стадии реакции нитритов целлюлозы, распад которых по радикальному механизму и последующая стабилизация радикала приводит к образованию продуктов окисления. Позднее эта схема была несколько уточнена в работе [121].[ . ] Разложение целлюлозы в аэробных условиях осуществляется рядом бактерий, актиномицетами и грибами. Чаще всего это бактерии из poflaCytophaga, а также бактерии рода Cellvibrio. Из акти-номицетов способностью к окислению целлюлозы обладают роды Micromonospora, Streptomyces, из,грибов — Fusarium, Aspergillus и некоторые другие. Грибы медленно разлагают целлюлозу и часто при этом наблюдается неполное окисление с образованием лимонной, щавелевой, уксусной, муравьиной и других кислот.[ . ] По окончании окисления целлюлозу извлекают из раствора, промывают дистиллированной водой и погружают на 1—2 ч в 0,1 н. соляную кислоту. Затем оксицеллюлозу вновь промывают для удаления кислоты дистиллированной водой и высушивают на воздухе. Определяют выход оксицеллюлозы, содержание в ней карбонильных и карбоксильных групп, а также поглощение кислорода при окислении. Для определения количества кислорода, поглощенного целлюлозой, необходимо учесть самопроизвольное разложение гипохлорита во время реакции. С этой целью параллельно с рабочим проводят холостой опыт с таким же количеством раствора гипохлорита. Сразу же по окончании обоих опытов определяют концентрацию гипохлорита в каждом растворе. Для этого отбирают 20 мл раствора, вводят в него 20 мл 10%-ного йодистого калия, 25 мл 2 н. серной кислоты и титруют 0,04 н. раствором тиосульфата натрия в присутствии крахмала.[ . ] Наиболее часто окисление целлюлозы протекает гетерогенно. На ход такого процесса значительное влияние оказывает надмолекулярная структура целлюлозы и строение волокна в целом. Окисление начинается с поверхности волокна, а затем постепенно продвигается в более глубокие слои, при этом сначала окисляется аморфная часть, а затем кристаллические участки. Механическая прочность волокна постепенно понижается, оно становится ломким. После глубокого окисления целлюлозу можно даже растереть в порошок.[ . ] Пиролиз нитратов целлюлозы. Характер и количество продуктов деструкции зависели от остаточного давления при нагревании. При остаточном давлении 2—3 мм образовывался твердый остаток нитрованной окисленной целлюлозы. При более высоком давлении выделялась жидкая смесь, состоящая в основном из воды, муравьиной кислоты, формальдегида, глиоксаля и небольших количеств других карбонилсодержащих соединений. Используя метод меченых атомов (14С), авторы установили, что углерод в положении 1 превращается преимущественно з двуокись углерода, муравьиную кислоту и глиоксаль [112, 113], а С образует в основном формальдегид и небольшие количества муравьиной кислоты и двуокиси углерода. Атомы С(2> и С(5> входят в состав некоторого количества образующейся двуокиси углерода и муравьиной кислоты и очень небольшого количества формальдегида.[ . ] Хотя способность окисления целлюлозы еще мало изучена, все же нет сомнения в том, что степень окисления находится в большой зависимости от окислителя. Двуокись азота [57, 58, 59] и водная соль йодной кислоты [29, 32, 40] в конечном итоге окисляют практически все глюкозные единицы в волокне, которое набухает в диаметре и сжимается по длине, но.мало меняет свою форму. Выход оксицеллюлозы практически остается количественным и поэтому при вторичном окислении до водорастворимых фрагментов теряется немного материала. В связи с этим такие окислители способны проникать в целлюлозные кристаллиты со скоростью гораздо меньше той, которая присуща аморфным зонам. Разрыв в кривой скорости окисления с солыо йодной кислоты достаточно заметен, чтобы его удалось использовать в качестве меры доступности [314]. В соответствии с ее пермутоидной природой ион соли йодной кислоты по мере проникновения в кристаллиты вызывает постепенное исчезновение диффракционной рентгенограммы целлюлозы, но окисление двуокисью азота почти заканчивается, прежде чем можно заметить уменьшение интенсивности и первоначальной рентгенограммы. Эта аномалия заставляет предполагать, что активным окислительным агентом вместо объемистой молекулы четырехокиси азота является двуокись азота или ион нитрония, Nüf» которые, вероятно, не могут повлиять на кристаллическую решетку, так как достаточно малы, чтобы проникнуть в нее [159].[ . ] Основное направление окисления целлюлозы двуокисью азота — окисление первичных гидроксильных групп до карбоксильных.[ . ] При получении растворов целлюлозы приходится сталкиваться с весьма нежелательной при определении молекулярного веса окислительной деструкцией целлюлозы. Целлюлоза в щелочной среде легко окисляется даже кислородом воздуха; окисление сопровождается снижением молекулярного веса. Из применяемых для определения молекулярного веса растворов целлюлозы особенно чувствительны к окислительному воздействию кислорода воздуха медноаммиачные растворы. При использовании этих растворов приходится применять специальные меры защиты от соприкосновения с воздухом — не допускать контакта раствора с внешней средой, работать в атмосфере азота или вводить в раствор вещества, препятствующие окислению целлюлозы. В значительно меньшей степени целлюлоза подвержена окислению кислородом воздуха в растворах купри- и кадмийэтилендиамина, почти не окисляется она в растворе железовиннонатриевого комплекса. В фосфорной кислоте целлюлоза кислородом не окисляется, но концентрированная фосфорная кислота вызывает медленный гидролиз целлюлозы.[ . ] Реакционная способность целлюлозы тесно связана с плотностью упаковки, упорядоченностью или доступностью макромолекул целлюлозы. Для определения этого показателя используются различные методы, такие, как рентгенография, поглощение воды, обменная реакция с тяжелой водой, определение удельного веса, окисление, гидролиз, этанолиз и т. д. Однако доступность целлюлозы может меняться при различных обработках; поэтому для получения результатов, сопоставимых со скоростью этерификации целлюлозы, необходимо определять доступность в условиях, максимально приближающихся к условиям этерификации. Так, например, метод определения доступности целлюлозы путем ее окисления трехокисью хрома хорошо согласуется с непосредственным измерением скорости ацетили-рования. Это во многом обусловливается тем, что окисление целлюлозы трехокисью хрома проводится в смеси уксусной кислоты и уксусного ангидрида, т. е. доступность целлюлозы определяется в условиях, близких к условиям ацетилирования [4].[ . ] Характер и скорость реакции окисления определяются в первую очередь pH среды. В среде, близкой к нейтральной, при pH от 6 до 8, в растворе находятся как хлорноватистая кислота, так и ионы гипохлорита. Скорость окисления целлюлозы в этих условиях наибольшая; полученная оксицеллюлоза обладает как кислыми, так и восстанавливающими свойствами. Окисление целлюлозы гипохлоритом в нейтральной среде применяют часто для получения оксицеллюлозы. Глубину окисления при этом регулируют изменением концентрации гипохлорита, температуры и продолжительности обработки.[ . ] Основные закономерности реакций окисления целлюлозы рассмотрены в ряде монографий (см., иапример, [83—85]). Поэтому ниже приводятся лишь некоторые данные о механизме и направлении реакций избирательного окисления.[ . ] Часто применяют также метод избирательного окисления альдегидных групп хлористой кислотой НС102. Содержание альдегидных групп при этом определяют либо по расходу реагентов, либо по увеличению содержания в окисленной целлюлозе карбоксильных групп [6].[ . ] Большинство процессов химической переработки целлюлозы основывается на реакциях гидроксильных групп целлюлозных макромолекул. Получающиеся производные целлюлозы могут быть разделены на три основных класса: молекулярные соединения, продукты замещения и продукты окисления. Молекулярные соединения являются нестабильными продуктами, образованными за счет водородных связей между гидроксилами целлюлозы и некоторыми сильно полярными реагентами. Продукты замещения образуются путем химической реакции между гидроксилами целлюлозы и реагентами, которые связываются с кислородом гидроксила ковалентной связью. К ним относятся сложные и простые эфиры целлюлозы. Эти продукты имеют наибольшее техническое значение. Продукты окисления целлюлозы обычно деструктированы. Они долгое время не имели широкого практического применения. В настоящее время в промышленных масштабах уже производится целлюлоза, окисленная двуокисью азота. Этот продукт применяется в медицине, в первую очередь, как хорошее кровоостанавливающее сред-л ство, а также в текстильной и других отраслях промышленности. Окисленные целлюлозы, кроме того, представляют интерес как волокнистые ионообменники. Ведутся интенсивные исследования с целью введения в целлюлозные макромолекулы новых реакционноспособных функциональных групп, использования их для химических превращений, описанных в классической органической химии, синтеза привитых сополимеров целлюлозы и так называемых сендвич-полимеров целлюлозы с другими полимерными веществами. Исследования в области модификации целлюлозы в ближайшие годы безусловно приведут к широкому использованию препаратов модифицированной целлюлозы в различных отраслях народного хозяйства.[ . ] Хотя проведены многочисленные исследования по окислению целлюлозы щелочным, нейтральным и кислым гипохлоритом [66, 77—84], гипоброми-том [66, 76, 79, 85], перекисью водорода [78, 86—89], озоном [90, 91, 92], перманганатом [70, 79, 87, 88, 91, 93—98], кислородом и щелочью [98— 102], азотной кислотой [4, 47, 85, 87], сернистой кислотой при 150° [103] и другими агентами, результаты не дали достаточного представления о подробном строении получающихся при этом продуктов. Многие из них при кипячении с минеральной кислотой дают наибольшие количества фурфурола и двуокиси углерода [76, 96, 104] и, по-видимому, содержат структурную единицу (11), содержащую не более 40% карбоксильных групп в окси-целлюлозе, полученной с щелочным гипобромитом [76], а остаток, вероятно, представляет собой структуру формулы (7, И=СООН). Этот остаток может возникнуть при окислении соответствующего диальдегида, но его также можно получить при дальнейшем окислении кетонов (16) и (17), и поэтому появление этого остатка не доказывает, что начальное окисление происходит по избирательному периодатному пути.[ . ] В этом разделе будет рассмотрено взаимодействие целлюлозы (или окисленной целлюлозы) с раствором щелочи (или с гидроксильным ионом вообще). Окисление молекулярным кислородом в щелочной среде не рассматривается, однако следует подчеркнуть, что этот процесс может являться первой стадией получения окисленных целлюлоз, содержащих карбонильные группы, которые затем деструктируются под действием щелочи, как описано ниже.[ . ] Уже более 80 лет известно, что солнечный свет разрушает целлюлозу и целлюлозные материалы. В 1883 г. Уитц [1] впервые установил, что свет может вызывать химические изменения целлюлозы. Позднее Харрисон [2] показал, что при разрушении целлюлозы под действием света образуется окисленная целлюлоза (ок-сицеллюлоза) и органическое соединение, обладающее сильными восстановительными свойствами. Продолжительное облучение кварцевой ртутной лампой превращает целлюлозу в мелкий порошок [3]. Вигноп [4] обнаружил, что в процессе фотодеструкции целлюлозы участвуют влага и кислород. Затем появились сообщения о том, что на свету пряжа или ткань теряют прочность [5], а в макромолекуле целлюлозы появляются карбоксильные и карбонильные группы [6—10].[ . ] Препараты тщательно, но осторожно очищенной хлопковой целлюлозы имеют очень низкие медные числа (0,13—0,17), обычный хлопок 0,25—0,30, древесная беленая целлюлоза до 2,0—3,0, а иногда и выше. К повышению медных чисел приводит гидролиз целлюлозы в условиях варки и окисление при неосторожной отбелке. Медные числа гидроцеллюлозы и оксицеллю-лозы — продуктов частичного поверхностного гидролиза и окисления целлюлозы иногда очень сильно возрастают по сравнению с медными числами исходной целлюлозы.[ . ] Кроме метода хлорирования, в настоящее время для определения целлюлозы часто применяется азотнокислотный способ. В первоначальных исследованиях наблюдалось очень сильное окисление целлюлозы азотной кислотой и поэтому считали, что азотная кислота мало пригодна для количественного выделения целлюлозы. Однако разработанные позднее методы позволили уменьшить деструкцию целлюлозы и получить удовлетворительные результаты. Из ряда предложенных методов в практике наиболее часто используется метод Кюршнера и Хоффе р а [2], основанный на применении спиртового раствора азотной кислоты. При обработке древесины смесью концентрированной азотной кислоты и этилового спирта лигнин нитруется и частично окисляется и переходит в раствор спирта. Гемицеллюлозы в большей своей части гидролизуются. Спиртовая среда умеряет окисляющее и гидролизующее действие азотной кислоты на целлюлозу. Предложенный метод нашел сравнительно широкое применение благодаря быстроте и простоте проведения опыта, хотя выход и качественные показатели целлюлозы, выделенной этим методом, ниже, чем для целлюлозы, полученной методом хлорирования. Предварительная экстракция древесины органическими растворителями не требуется, так как экстрактивные вещества удаляются спиртом в ходе проведения опыта.[ . ] При сравнении вязкости растворов химически модифицированных целлюлоз (главным образом различных препаратов окисленной целлюлозы) в куоксаме, куэне и трех модифицированных растворителях ЖВНК, а также нитратов целлюлозы в этилацетате был сделан вывод [125], что введение новых функциональных групп в макромолекулу целлюлозы приводит к дополнительному понижению ее устойчивости к действию щелочей и вызывает значительное снижение СП, определенной в щелочных растворителях. Поэтому целесообразно определять СП модифицированных целлюлоз только после обработки этих препаратов боргидридом натрия.[ . ] Жирар [2], который в 1875—1881 гг. систематически изучал деградацию целлюлозы под действием кислот, назвал образующиеся при этом продукты гидроцеллюлозами, так как он думал, что к целлюлозным молекулам химически присоединены молекулы воды. В настоящее время известно, что присоединение является ничтожным, неощутимым, пока деградация не достигла крайней степени. В 1883—1884 гг. Витцу [3] удалось установить различия между повреждениями хлопковых материалов, вызванными окислительными агентами, и повреждениями, вызванными кислотами. Частично разрушенные, но еще волокнистые продукты он назвал оксицеллюлозами. Этот термин почти одновременно был применен к продуктам, настолько жестко окисленным азотной кислотой, что волокнистая структура была разрушена, а белые или бледно-желтые порошки были частично растворимы в воде. Как и термин «гидроцеллюлоза», термин оксицеллюлоза является неточным. Его употребляют только по привычке, так как оксицеллюлоза чаще образуется путем отщепления водорода от целлюлозной молекулы, а не путем присоединения кислорода к ней. Более точным названием было бы — окисленная целлюлоза.[ . ] Появление в целлюлозном звене, особенно у шестого углеродного атома, окисленных групп резко снижает устойчивость глю-козидной связи к действию щелочей, что ведет к деструкции целлюлозной цепи в щелочной среде. Деструкция, происходящая в результате окисления целлюлозы, носит название окислительной. Появление новых функциональных групп изменяет и другие свойства целлюлозы. Даже небольшое количество карбонильных или карбоксильных групп увеличивает растворимость целлюлозы в щелочах, ускоряет ее пожелтение, снижает термостойкость. С появлением карбоксильных групп целлюлоза становится также активным ионообменным соединением и приобретает способность удерживать катионы.[ . ] При определении медного числа, которое проводится в щелочной среде, происходят побочные реакции окисления, увеличивающие восстановительную способность целлюлозы. Особые трудности возникают при определении медных чисел окисленных целлюлоз. Кроме того, сами реагенты, применяющиеся при определении медных чисел, например фелингова жидкость, не являются достаточно устойчивыми и в процессе определения медного числа целлюлозы выделяют некоторое количество закиси меди. Это требует строгого соблюдения условий анализа и должной оценки полученных абсолютных значений при определении восстановительной способности целлюлозы. На восстановительную способность химически измененной целлюлозы значительное влияние оказывает не только количество альдегидных групп, но и их положение в молекуле целлюлозы [9]. Несмотря на все эти недостатки, определение медного числа оказывается полезным при исследовании целлюлозных препаратов, особенно при серийных анализах, с целью сравнения степени деструкции, а также для качественной характеристики целлюлозы.[ . ] Шмидт и др.180] путем потенциометрического титрования определяли содержание карбоксильных групп в окисленной целлюлозе. Они установили, что в целлюлозах различного происхождения содержание карбоксильных групп является постоянным (0,28% в пересчете на СО2) и соответствует степени полимеризации 96 глюкозных единиц. Ниэл [81] не смог получить таких результатов и сомневался в том, чтобы целлюлозы различного происхождения обладали одинаковой степенью полимеризации. Другими авторами с помощью мягкого гидролиза была найдена такая же степень полимеризации.[ . ] Этот метод может применяться для определения карбоксильных групп типа групп уроновых кислот в обычной и окисленной целлюлозе. Из уроновых кислот СОг образуется с большой первоначальной скоростью, которая затем постепенно понижается до нуля. Из целлюлозы СОг образуется медленно, сохраняя постоянную скорость реакции на протяжении длительного времени. Таким образом, форма кривой скорости реакции может служить признаком присутствия или отсутствия уроновых кислот. Содержание групп уроновых кислот в целлюлозе с учетом поправки на выход СОг из чистой целлюлозы позволяет определять метод Уистлера и Невеля [1].[ . ] В ранних исследованиях для делигнификации древесины применяли азотную кислоту и другие сильные окислители, которые, однако, вызывали сильный гидролиз и окисление целлюлозы. Более плодотворными явились исследования с применением галогенов: хлорной и бромной воды и газообразного хлора. Впоследствии были найдены более совершенные методы делигнификации, минимально влияющие на углеводную часть, основанные на использовании модифицированного способа хлорирования и на применении двуокиси хлора и хлорита натрия (последние применяются для выделения холоцеллюлозы). Также был разработан сравнительно мягкий способ определения целлюлозы с применением азотной кислоты.[ . ] Детальное исследование условий восстановления было осуществлено Хидом [101]. Как было показано в работе [101], восстановление альдегидных групп в гидроксильные повышает устойчивость гликозидиой связи к действию щелочных реагентов.[ . ] Простой и эффективный метод применен при разделении активных компонентов неочищенного кортикотропного гормона, выделенного из передней доли гипофиза свиньи, на окисленной целлюлозе, причем компоненты выделены почти количественно и с высокой степенью чистоты [70]. Специально окисленную фильтровальную бумагу используют для разделения гистина, лизина и аргинина [71]. С помощью ионообменной бумаги с успехом разделяют свинец, висмут, серебро.[ . ] В воде соединения брома являются гораздо более сильными окислителями, чем аналогичные соединения хлора, но последние представляют собой более активные галогенирующие агенты. Например, окисление целлюлозы бромноватистой кислотой происходит более быстро, чем хлорноватистой [33]. Окисление глюкозы в гликолевую кислоту с бромноватистой кислотой происходит в 1360 раз быстрее, чем с хлорноватистой [34]. Вследствие того, что эффективные окислительные потенциалы у бромных систем ниже, чем у аналогичных хлорных систем, относительная окислительная сила этих галогенидных соединений, измеренная их окислительными потенциалами, не является верным показателем их химической активности [35]. Аномальное поведение, когда соединения брома неожиданно дают более высокие скорости окисления, показывает, что на скорость окисления сильнее влияют такие факторы, как механизмы реакций, сила связей и стерические препятствия, чем окислительные потенциалы.[ . ] Обычно обработку пероксидом водорода ведут в интервале температур 60 — 80 °С. Повышение температуры приводит к снижению числа Каппа и повышению белизны. Ограничение по температуре определяется вязкостью целлюлозы, т.к. повышение температуры более 80°С усиливает щелочную деструкцию окисленной целлюлозы.[ . ] Применяя спектральные приборы с большой дисперсией, можно увеличить точность анализа целлюлозных материалов. Так, Поляк [168], применяя призму СаЕ2, показал возможность раздельного определения карбоксильных и карбонильных групп в окисленной целлюлозе спектроскопическим методом. Спектроскопическим методом изучают процессы кристаллизации три-ацетилцеллюлозы [169] и других эфиров целлюлозы [81, 122]. Всестороннее изучение окисленных целлюлоз проведено Ермоленко [141]. Многочисленные соединения целлюлозы с новыми функциональными группами и различные сополимеры целлюлозы исследованы Жбанковым и сотр. [81, 122].[ . ] Для прививки применяют некоторые другие окислители, например систему марганец — перманганат-ион, соли ванадия и бро-мат калия. Однако большинство этих исследований описано лишь в патентах и кратких заметках. До некоторой степени аналогичная методика основана на применении для окисления целлюлозы перйодата натрия, приводящего к разрыву углерод-углеродной связи гликолевых групп [16].[ . ] Способность этих красителей действовать, как сенсибилизаторы, когда они стимулируются видимым или ультрафиолетовым светом, может быть показана графически [341 ] на примере хлопчатобумажной ткани, увлажненной перекисью водорода, или 0,1 н. гипохлоритом натрия при pH 7 и облученной полным ртутным спектром. Окисленные части становятся видимыми благодаря количеству и месторасположению металлического серебра, осажденного при кипячении волокон в воде, содержащей 0,296 азотнокислого серебра, 1% едкого натра и 1% тиосульфата натрия. Когда вместо хлопка используют вискозную пленку, то при помощи микрофотометра можно нанести на диаграмму месторасположение и интенсивность серебряных пятен. Эти диаграммы показывают, что сильное окисление целлюлозы наблюдается только у частей, подверженных действию линий спектра 365, 334, 313, 302 ми и меньше в ультрафиолете, тогда как синие и желтые линии 405, 436, 546 и 578 м;а не активны. Однако окисление происходит у всех линий, когда хлопок или целлофан сперва пропитывается активным красителем, подобным каледону желтому в, 2й или 50, цибанону желтому И и оранжевому Я, но не при пропитке неактивным красителем, подобным каледону нефритовому зеленому X. Общее действие сенсибилизирующих или защитных красителей, протрав и других текстильных агентов на вискозный шелк было описано Хенком [342], который отмечал, что обыкновеннее оконное стекло не является достаточной защитой от солнечного света. Сообщают, что окись хрома в протравах обладает защитным влиянием 1343]. Деградация хлопчатобумажных изделий в промышленных районах летом в большинстве случаев является следствием фотохимических изменений, а зимой происходит главным образом от кислотных туманов, вызванных сжиганием топлива.[ . ] источники: http://himija-online.ru/organicheskaya-ximiya/uglevody/cellyuloza.html http://ru-ecology.info/term/24327/ |