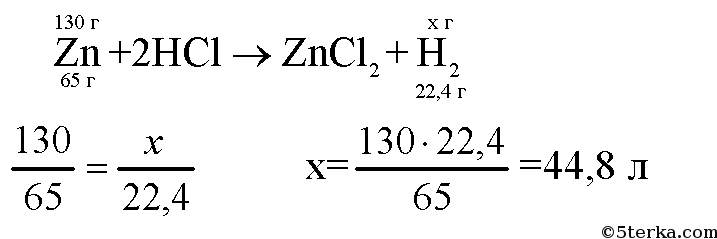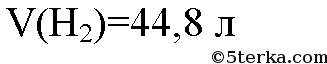Тема III. Работа 1. Получение и свойства водорода. Вариант 3
Вопросы:
1. Напишите уравнения реакций: а) водорода с кислородом; б) водорода с оксидом железа(II); в) алюминия с соляной кислотой.
2. Какими способами можно собирать водород в пробирку? На каких свойствах водорода основаны эти способы?
3. Рассчитайте массу водорода, образующегося при взаимодействии 48 г магния с соляной кислотой.
Уравнение реакции: Mg + 2HCl = MgCl2 +H2↑
Решения и ответы:
2. Водород собирают в перевернутый вверх дном сосуд, т.к. водород легче воздуха.

задача №3
к главе «Тема III. Водород. Кислоты. Соли. Работа 1. Получение и свойства водорода».
Реакция водорода с кислородом уравнение реакции


Что получается из водорода и кислорода, мы уже знаем:
Теперь учтем, что атомы химических элементов в химических реакциях не исчезают и не появляются из ничего, не превращаются друг в друга, а соединяются в новых комбинациях, образуя новые молекулы. Значит, в уравнении химической реакции атомов каждого сорта должно быть одинаковое количество до реакции (слева от знака равенства) и после окончания реакции (справа от знака равенства), вот так:
Это и есть уравнение реакции — условная запись протекающей химической реакции с помощью формул веществ и коэффициентов.
Это значит, что в приведенной реакции два моля водорода должны прореагировать с одним молем кислорода, и в результате получится два моля воды.
Взаимодействие водорода с кислородом — совсем не простой процесс. Он приводит к изменению степеней окисления этих элементов. Чтобы подбирать коэффициенты в таких уравнениях, обычно пользуются методом «электронного баланса«.
Когда из водорода и кислорода образуется вода, то это значит, что водород поменял свою степень окисления от 0 до +I, а кислород — от 0 до −II. При этом от атомов водорода к атомам кислорода перешло несколько (n) электронов:

Водород, отдающий электроны, служит здесь восстановителем, а кислород, принимающий электроны — окислителем.

Посмотрим теперь, как выглядят процессы отдачи и приема электронов по отдельности. Водород, встретившись с «грабителем»-кислородом, теряет все свое достояние — два электрона, и его степень окисления становится равной +I:
Получилось уравнение полуреакции окисления водорода.
А бандит-кислород О2, отняв последние электроны у несчастного водорода, очень доволен своей новой степенью окисления -II:
Это уравнение полуреакции восстановления кислорода.
Остается добавить, что и «бандит», и его «жертва» потеряли свою химическую индивидуальность и из простых веществ — газов с двухатомными молекулами Н2 и О2 превратились в составные части нового химического вещества — воды Н2О.
Дальше будем рассуждать следующим образом: сколько электронов отдал восстановитель бандиту-окислителю, столько тот и получил. Число электронов, отданных восстановителем, должно быть равно числу электронов, принятых окислителем.
Значит, надо уравнять число электронов в первой и второй полуреакциях. В химии принята такая условная форма записи уравнений полуреакций:
 |
 |
 |
При этом получается фтороводород HF или аммиак NH3.
В обоих соединениях степень окисления водорода становится равной +I, потому что партнеры по молекуле ему достаются «жадные» до чужого электронного добра, с высокой электроотрицательностью — фтор F и азот N. У азота значение электроотрицательности считают равным трем условным единицам, а у фтора вообще самая высокая электроотрицательность среди всех химических элементов — четыре единицы. Так что немудрено им оставить бедняжку-атом водорода без всякого электронного окружения.
Но водород может и восстанавливаться — принимать электроны. Это происходит, если в реакции с ним будут участвовать щелочные металлы или кальций, у которых электроотрицательность меньше, чем у водорода.
При встрече молекул водорода с такими металлами он сам становится «бандитом» и «охотником за электронами» и отнимает у металлов их электронное «достояние»:

 |
В обоих случаях получаются гидриды металлов — гидрид натрия NaH и гидрид кальция СаН2, в которых водород имеет степень окисления −I. Таким образом, мы выяснили, что водород в окислительно-восстановительных реакциях может быть и охотником за электронами, и жертвой.

Реакция взаимодействия водорода и кислорода
После написания статьи о получении кислорода в домашних условиях у одного из читателей возникли сомнения в том, что реакцию взаимодействия кислорода и водорода изучали в школе.
В комментариях я ответила ему, что это не так. Взаимодействие водорода с кислородом всегда изучали и продолжают изучать и по сей день, а также делают лабораторные и практические работы. Чтобы не быть голословной, привожу несколько отсканированных страниц школьных и университетских учебников разных лет издания.
В каждом скане вы можете увидеть реакцию, формулы, уравнения — то есть все, что положено для любого нормального учебника химии и любой химической реакции.
Учебник химии за 1966 год:
Вот страница из него по соответствующей теме:
Учебник химии за 8 класс под редакцией Наиля Сибгатовича Ахметова, по университетским учебникам которого выучилось не одно поколение студентов (и я в том числе):
Это — соответствующее уравнение:
Учебник авторов Г.Е. Рудзитиса и Ф.Г. Фельдмана, по которым школьники начали заниматься в конце 80-х (могу ошибаться, говорю приблизительно) и занимались, наверное, до начала двухтысячных (тоже приблизительно). Я сама в 1991—1995 годах занималась по учебникам их авторства. А позже, в 1999—2001 преподавала в школе по этим учебникам.
Соответствующая тема из этого учебника:
Вот страница моей школьной тетради за 1991 год:
А это — соответствующая лабораторная работа:
Для примера приведу и университетский учебник за 1978 год под редакцией Н.Л. Глинки. Тоже классическая книга для химиков:
А это — глава из него, посвященная водороду:
Думаю, теперь ни у кого не будет сомнений, что в школе всегда изучали и продолжают изучать эту интересную химическую реакцию?
Удачи всем в изучении химии!
KidsChemistry теперь есть и в социальных сетях. Присоединяйтесь прямо сейчас! Google+ , В контакте , Одноклассники , Facebook , Twitter
http://www.alhimik.ru/teleclass/glava4/gl-4-3.shtml
http://kidschemistry.ru/reakciya-vzaimodejstviya-vodoroda-i-kisloroda.html