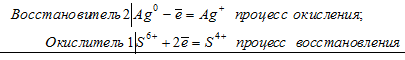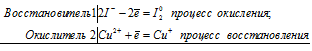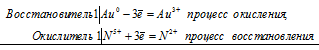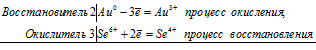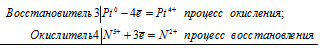Составление окислительно-восстановительных реакций соединений серебра, золота и платины
Задание 391
Серебро не взаимодействует с разбавленной серной кислотой, тогда как в концентрированной оно растворяется. Чем это можно объяснить? Составьте электронные и молекулярные уравнения соответствующей реакции.
Решение:
Серная кислота обладает окислительными свойствами (сходными со свойствами азотной кислоты), если её концентрация превосходит 70%. Только тогда можно говорить о специфических свойствах H2SO4, как окислителя. Концентрированная серная кислота, как окислитель восстанавливается активными металлами (от Mg Cr) до H2S, малоактивными металлами (от Fe до Pb) – до свободной серы, а тяжёлыми, инертными металлами (отSb до Au) – до оксида серы (IV). При содержании H2SO4 в растворе менее 70% (разбавленная серная кислота) её поведение описывается в рамках обычных представлений. При взаимодействии разбавленной серной кислоты с металлами, стоящими в электрохимическом ряду напряжений левее водорода, выделяется газообразный водород. С металлами, стоящими в ряду напряжений правее водорода, разбавленная серная кислота не взаимодействует.
В концентрированной серной кислоте элементом-окислителем является атом серы (степень окисления +6), а в разбавленной – водород (степень окисления +1).
Уравнение реакции растворения серебра в концентрированной серной кислоте
2Аg 0 + S 6+ = 2Ag + + S 4+
В данной реакции серебро увеличивает свою степень окисления от 0 до +1, т. е. проявляет свойства восстановителя, а сера уменьшает свою степень окисления от +6 до +4, т.е. проявляет свойства окислителя.
Задание 401
Какую степень окисления проявляют медь, серебро и золото в соединениях? Какая степень окисления наиболее характерна для каждого из них? Иодид калия восстанавливает ионы меди (II) в соединения меди со степенью окисления +1. Составьте электронные и молекулярные уравнения взаимодействия KI с сульфатом меди.
Решение:
Для меди характерна степень окисления +1 (Cu2O, CuCl, CuI, Cu2S) и +2 [CuO, CuSO4 . 5H2O, Cu(NO3)2 . 6H2O, CuS, Cu2(OH)2CO3]; для серебра: +1 (Ag2O, AgNO3, AgCl, AgBr, AgI); для золота: +3 (AuCl3, H[AuCl4]). Как элементы 2-й группы медь, серебро и золото имеют по одному электрону на внешнем энергетическом уровне (ns 1 ), поэтому должны проявлять степень окисления +1. Характерная степень окисления, как у элементов 2-й группы должна быть +2. Для меди наиболее характерна степень окисления +2, для серебра +1, а для золота +3.
Уравнения взаимодействия KI с сульфатом меди
2Сu 2+ +2I — = Cu + + I2 0
Задание 404
Золото растворяется в царской водке и в селеновой кислоте, приобретая при этом высшую степень окисления. Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
а) Золото растворяется в «царской водке» с образованием комплекса H[AuCl4]
Au 0 +N 5+ = Au 3+ + N 2+
3Au + 12HCl + 3HNO3 = 3H[AuCl4] + 3NO + 6H2O
б) Золото растворяется в селеновой кислоте с образованием селената золота(III)
2Au 0 + 3Se 6+ = 2Au 3+ + 3Se 4+
Задание 428
Составьте электронные и молекулярные уравнения реакций: а) растворения платины в царской водке; б) взаимодействия осмия с фтором. Платина окисляется до степени окисления +4, а осмий — до+8.
Решение:
а) Реакция растворения платины в царской водке
3Pt 0 + 4N 5+ = 3Pt 4+ + 4N 2+
б) Реакция взаимодействия осмия с фтором:
Растворение золота в царской водке: очистка, пропорции раствора кислот, осаждение золота в домашних условиях и его переплавка в слитки
Царская водка – вода царей — Aqua Regia на латыни – смесь двух кислот, соединенных вместе. Азотная и соляная кислоты берутся в пропорции один к трем. Это баланс по массе, при пересчете на чистые вещества один к двум. Издает неприятный хлорный запах. Уникальная особенность состава – возможность растворять ряд драгоценных металлов – золота, платины и др. Используется для очищения золота от примесей путем фильтрования и осаждения металла.
Царская водка: история названия, пропорция кислот и химические свойства
Свойства Aqua Regia была описаны еще до того момента, как была открыта соляная кислота в 14 веке. Состав получил широкое распространение и свое название в эпоху расцвета алхимии на Европейском континенте. Алхимик из Германии Альберт Великий (Кельнский), который был наставником Фомы Аквинского, назвал ее aqua secunda как производное от aqua prima, азотной кислоты.
В переводе с латыни «вторичная водка» и «первичная водка».
Представители алхимической когорты начали именовать ее царской тогда, когда кардинал Бонавентура, относимый католичеством к отцам церкви, установил, что вещество, которое объединило две кислоты способно растворять «царя металлов». Ранее этого момента считалось, что благородный металл не может быть ничем изменен. Взаимодействие царской водки и золота доказало обратное. В России М.В Ломоносов называл раствор «королевской водкой».
Символ Aqua Regia, принятый у алхимиков: ▽R. перевернутый треугольник — знак воды.
Химические продукты, соединяясь, взаимодействуют и образуют состав продуктов, который отличается высокой активностью. Это проявляется в сильном запахе с оттенками хлора и диоксида азота. Газообразная двуокись азота желтого цвета напоминает дым такого тона.
Сначала царская водка не имеет цвета, но постепенно приобретает желто-оранжевый оттенок, становясь очень сильным окислителем. Если ее хранить некоторое время, постепенно разлагается, выделяя газообразные вещества.
Скорость травления, то есть окисления, или уровня растворимости, золота — около 10 мкм/мин. Другие благородные металлы требуют для прохождения реакции нагрева до определенных температур. Это относится к родию и иридию. Иными свойствами отличается такой металл, как серебро. Растворение в Aqua Regia не наступает, на поверхности образуется слой AgCl, хлорида драгоценного металла.
4 способа растворить золото в домашних условиях: в чем лучше + пошаговая инструкция
Промышленный метод
При добыче золота из так называемых золотоносных песков приходится работать со взвесью примерно одинаково мелких частиц золота и песчинок, которые нужно отделить друг от друга. Можно сделать это с помощью промывания, а можно использовать цианид натрия или калия — разницы нет. Дело в том, что золото образует растворимый комплекс с цианид-ионами, а песок не растворяется и остается как есть.
Ключевым моментом в этой реакции является наличие кислорода (того, что содержится в воздухе, достаточно): кислород окисляет золото в присутствии цианид-ионов и получается комплекс. При недостаточном количестве воздуха или сама по себе без цианида реакция не идет.
Сейчас это наиболее распространенный способ промышленного получения золота. Конечно, до получения конечного продукта еще много стадий, но нас интересует конкретно этот этап: растворы цианидов — то, в чем растворяется золото.
Методика применения реактивов
Реактивы для золота могут достаточно точно определить их пробу, их удобно использовать в больших масштабах, а не в домашних условиях. Их применение для апробирования начинается с осмотра изделия. Иногда хватает одного взгляда на пробу, чтобы определить подделку. Клеймо может содержать асимметричные символы, кривые формы и изображения. Следующим шагом идет определение принадлежности сплава к группе низкопробного или высокопробного золота.
Поверхность изделия в определенном месте зачищается. Это помогает узнать, есть ли под золотым слоем другой металл или это единый сплав. Дальнейшая методика зависит от типа выбранного реактива.
Хлористое золото не одинаково действует на разные составы. Для проверки чистоты реагент наносят на поверхность украшения. Сплавы от 585 до 999 пробы никак не отреагируют на химическое соединение. На изделиях, в которых драгметалла содержится половина от общей массы, хлорное золото оставит темное пятно. Если же в материале ничтожно малое содержание желтого металла, менее 50%, реактив вызовет реакцию в виде сильного потемнения и появления осадка. Чем ниже проба, тем насыщенней будет цвет и сильнее осадок.
При использовании хлорного золота нужно быть очень внимательным и соблюдать время выдержки препарата на золотой поверхности. Капля должна быть небольшой и четко лежать на своем месте, не растекаясь по всему изделию. После завершения работ химикат сразу же убирают.

Перед применением реактивов поверхность изделия в определенном месте зачищается
Азотная кислота считается самым доступным и распространенным способом апробирования ювелирных украшений. На защищенную поверхность с помощью пипетки капают реактив и выжидают пару минут. Попадая на сплав ниже 583 пробы, кислота вызывает выделение газа. Чем ниже содержание золота, тем сильнее будет происходить пузырение под каплей. После проверки реагент сразу вытирают небольшим кусочком ткани или бумажной салфеткой.
Йодистый калий применяется аналогичным способом, как и предыдущие реактивы. Единственно, что нужно помнить, препарат действует только на сплавы с содержанием основного металла выше 80%.


Амальгама
Процесс амальгамации также применяют в промышленности, только уже при работе с рудами и твердыми породами. Суть его заключается в способности ртути образовывать амальгаму — интерметаллическое соединение. Строго говоря, ртуть в этом процессе не растворяет золото: оно остается в амальгаме в твердом виде.
При амальгамации идет смачивание породы жидкой ртутью. Однако процесс «вытягивания» золота в амальгаму долгий, опасный (пары ртути ядовиты) и малоэффективный, поэтому этот метод уже редко где применяют.
Чистка салфеткой
Самым доступным, но от этого не менее эффективным является способ чистки, предусматривающий использование соответствующей ткани. Подходящим является материал с небольшой ворсистостью (например, флис). Необходимо качественно натирать им золото, пока оно снова не приобретет блеск и чистоту. Данный метод является механическим, при этом щадящим и подходящим к любым изделиям.
При регулярной чистке таким методом необходимость использования тех или иных жидкостей отпадает полностью, в том числе и профессиональных средств.
Специалисты отмечают, что использовать ткань для очистки золота не рекомендуется, если загрязнения слишком устарели. Таким способом темная оксидная пленка не удалится, труднодоступные места также останутся загрязненными.
Царская водка
Есть много кислот, способных разъедать живые ткани и оставлять страшные химические ожоги (вплоть до летального исхода). Однако нет такой одиночной кислоты, в какой растворяется золото. Из всех кислот подействовать на него может только знаменитая смесь — царская водка. Это азотная и соляная (хлороводородная) кислоты, взятые в соотношении 3 к 1 по объему. Замечательные свойства этого адского коктейля обусловлены тем, что кислоты берутся в очень больших концентрациях, что сильно повышает их окислительную способность.
Царская водка начинает действовать с того, что азотная кислота начинает окислять сперва соляную, и в ходе этой реакции образуется атомарный хлор — очень реакционноспособная частица. Именно она идет на атаку золота и образует с ним комплекс — золотохлористоводородную кислоту.
Это очень полезный реактив. Очень часто золото хранят в лаборатории именно в виде кристаллогидрата такой кислоты. Нам же оно служит лишь подтверждением того, что золото растворяется в царской водке.
Стоит еще раз обратить внимание на то, что окисляет металл в этой реакции не одна из двух кислот, а продукт их взаимной реакции. Так что если взять, например, одну лишь «азотку» — известную кислоту-окислитель — ничего не выйдет. Ни концентрация, ни температура не смогут сделать так, чтобы золото растворилось в азотной кислоте.


Что потребуется для процесса и за счёт чего металл растворяется?
Прежде чем приступить к непосредственной процедуре, следует знать, как растворить золото. Также необходимо заранее подготовить:
Азотную кислоту.
Многие удивляются, как так происходит, что смесь кислот растворяет царя металлов. На самом деле при соединении двух видов кислот и драгоценного металла, появляется новый продукт.
Вас может заинтересовать: Что такое сусальное золото и для чего его применяют?
Называется он тетрахлораурат водорода, или если по иному — золотохлористоводородная кислота.
Сам процесс реакции происходит следующим образом — Au + HNO3 + 4 HCl = HAuCl4 + NO + 2 H2O.
Это своеобразное уравнение дает объективно понять, что для процесса растворения 1 гр.
Драг металла потребуется не менее 5 мл реактивной жидкости. Что самое интересное, в качестве растворителя выступает не азотная кислота, а серная.
Азотная кислота в данном случае требуется лишь для того чтобы выступить в роли катализатора.










Хлорка
В отличие от кислот, в частности хлороводородной кислоты, отдельные вещества могут стать тем, в чем растворяется золото. Широко известная бытовая хлорка — раствор газообразного хлора в воде. Конечно, обычным магазинным раствором ничего не сделаешь, нужны концентрации повыше.
Хлорная вода действует следующим образом: хлор диссоциирует на соляную и на хлорноватистую кислоты. Хлорноватистая кислота под светом разлагается на кислород и соляную кислоту. В таком разложении выделяется атомарный кислород: как и атомарный хлор в реакции с царской водкой, он очень активен и окисляет золото за милую душу. В итоге опять получается комплекс золота с хлором, как и в предыдущем способе.
Пошаговая инструкция по растворению золота
Растворение металла — трудоемкий процесс. Действенный способ — использование цинка. Он применяется химиками для выделения чистейшего металла высокой пробы.
Существует множество видео, на которых наглядно показана бурная реакция с цинком.
Необходимые материалы и инструменты
Требуются следующие инструменты:
- емкость для нагрева;
- большой пинцет;
- плита;
- огнеупорная колба;
- колпак с щелью;
- аппарат для плавления металлов.
- чистый тетраборат натрия (бура);
- азотная кислота концентрированная;
- соляная кислота средней концентрации;
- цинк.
Процесс растворения
Емкость для нагрева из огнеупорного стекла или фарфора с небольшим углублением в центре необходимо избавить от влаги и нагреть на плите. В углубление емкости добавить тетраборат натрия. Золотой лом опустить в емкость и нагреть. Убедившись, что лом покраснел, посыпать его тетраборатом.
Золото начинает плавиться, а значит, необходимо добавить к нему небольшие кусочки цинка.
Полученный раствор нужно прокипятить. После остывания добавить в колбу чистую прохладную воду, чтобы промыть осадок. Взболтать колбу для оседания хлопьев желтого оттенка, осторожно слить воду и промывать до того момента, пока вода в колбе не перестанет быть мутной.
Отделить осадок от воды с помощью марли, отжать лишнюю воду и присыпать тетраборатом натрия. Завязать марлю в тугой узел, поместить в колбу и нагревать до тления марли и расплавления тетрабората. На дне колбы должен образоваться золотой ком.
Как только слиток металла затвердеет, его нужно вытащить, очистить от остатков соединения буры с окисленными металлами, прокипятив пять минут в растворе азотной и соляной кислот. Должен получиться гладкий и блестящий золотой слиток.



Другие галогены
Кроме хлора, золото также неплохо окисляют и другие элементы седьмой группы таблицы Менделеева. В полной мере сказать о них: «то, в чем растворяется золото» — трудно.
С фтором золото может реагировать по-разному: при прямом синтезе (с температурой 300-400°С) образуется фторид золота III, который в воде немедленно гидролизуется. Он настолько неустойчив, что разлагается даже при воздействии плавиковой (фтороводородной) кислоты, хотя среди фторид-ионов ему должно быть комфортно.
Также действием сильнейших окислителей: фторидов благородных газов (криптона, ксенона) можно получить и фторид золота V. Такой фторид вообще взрывается при контакте с водой.
С бромом дела обстоят несколько проще. Бром в обычных условиях — жидкость, и золото неплохо рассеивается в его растворах, образуя растворимый бромид золота III.
С йодом золото также реагирует при нагревании (до 400°С), образуя йодид золота I (такая степень окисления объясняется меньшей активностью йода по сравнению с другими галогенами).
Таким образом, золото, несомненно, реагирует с галогенами, однако растворяется ли золото в них — спорное утверждение.
Чистка драгоценностей с камнями
Золотые украшения с камнями требуют особого ухода. Например, если камешек посажен на клей, то его нельзя погружать в жидкость, иначе клейкое вещество растворится. Кроме того, некоторые инкрустации попросту не переносят механического воздействия.
Что же делать? Как почистить золото с камнями? Всё зависит от вида самоцвета.
- Цирконы, алмазы, топазы, изумрудные камни, гранатовые изделия, синие сапфиры относятся к группе твёрдых камней. То есть их можно чистить практически любым способом, не забывая, впрочем, о виде крепления.
- Коралловые, жемчужные, бирюзовые и опаловые драгоценности относятся к категории мягких камней. При их очищении нельзя прибегать к щёткам, абразивным материалам (сухая соль и сода). Избыток влаги также противопоказан для них. Отказаться стоит и от кислоты – лимонной и уксусной.
Осталось понять, какие составы и способы разрешены и допустимы. Самый простой и универсальный метод – использование тёплого мыльного раствора. А чтобы удалить застарелый налёт, твёрдые камешки можно потереть мягкой зубной щёткой, а мягкие самоцветы – войлочной тряпочкой.
А как почистить золото с бриллиантами? Попробуйте вариант с нашатырным спиртом и шампунем, о котором мы писали в самом начале статьи. Только не кладите драгоценности в неразведённый аммиак. Чтобы избавиться от жирного налёта, алмазы и изумруды можно протереть войлоком, смоченным в бензине.
Раствор Люголя
На самом деле, йод (обычный йод I2) в воде нерастворим. А растворим его комплекс с йодидом калия. Это соединение называется раствором Люголя — и он умеет растворять золото. Между прочим, им же часто смазывают горло болеющим ангиной, так что не все так однозначно.
Эта реакция также идет через образование комплексов. Золото образует с йодом комплексные анионы. Используется, как правило, для травления золота — процесс, при котором взаимодействие идет только с поверхностью металла. Раствор Люголя удобен в этом случае, потому что в отличие от царской водки и цианидов, реакция идет заметно медленнее (и реактивы доступнее).
Как отполировать золото до блеска
Полировка драгоценностей – ещё один способ добиться натурального блеска. Как мы уже говорили, с этой целью можно использовать пасту ГОИ (№№ 1, 2 и 3). Тереть нужно легкими движениями, не допуская избыточного давления и образования царапинок.
Можно изготовить полировочную пасту и своими руками.
Нам понадобятся следующие компоненты (в равных пропорциях):
- обычная зубная паста (без абразивных включений);
- вазелиновая мазь;
- растолчённый мел;
- измельчённое хозяйственное мыло;
- тёплая вода.
Все ингредиенты хорошенько перемешивают, добиваясь пастообразной консистенции. Этот состав накладывают на украшение, тщательно протирают с помощью мягкой тряпочки. Затем драгоценность промывают под проточной водой, избавляясь от вазелина. Останется только выложить на бумажную салфетку и просушить.
Категорически нельзя использовать для полировки абразивные материалы, например, соду, соль (даже мелкую), зубной порошок. Все эти составы могут попросту поцарапать изделие, в результате вы не только не избавитесь от грязи, но и получите новую проблему, от которой будет практически невозможно избавиться.
Бонус
Говоря о том, что одиночные кислоты — это то, в чем золото не растворяется, мы немного соврали — на самом деле такие кислоты есть.
Хлорная кислота — одна из самых сильных кислот. Ее окислительные свойства чрезвычайно высоки. В разбавленном растворе они проявляются плохо, однако в больших концентрациях творят чудеса. При реакции образуется ее соль перхлорат золота — желтый и неустойчивый.
Из кислот, в каких растворяется золото, есть еще горячая концентрированная селеновая кислота. В результате также образуется соль — селенат золота красно-желтого цвета.
Как почистить белое золото – полезные советы

Фото: https://pixabay.com/photos/rings-wedding-rings-white-gold-ring-3813522/
Сегодня большой популярностью пользуются ювелирные изделия из белого золота – сплава привычного нам жёлтого драгоценного металла с серебром, палладием либо никелем. Именно эти «добавки» и придают готовому материалу характерный белый цвет.
Такие украшения требуют более бережного ухода, чем изделия из жёлтого золота.
Какие способы подойдут в этом случае?
- Смесь нашатырного спирта с перекисью водорода. Приготовьте состав по описанному выше рецепту, оставьте золото на полчаса, прополощите и просушите.
- Состав из аммиака и шампуня (самый первый рецепт). Только держать в этой смеси белое золото нужно не 2 часа, а всего 30 минут.
- Содовый раствор (если есть камни, то от этого варианта стоит отказаться).
- Зубная паста. Только не стоит тереть изделия из белого золота зубной щёткой, пусть даже с мягкой щетиной.
Ещё один народный рецепт подразумевает приготовление смеси из 1 желтка и 40 мл обычного пива. Этим составом пропитывают мягкую тряпочку и чистят золотые изделия.
Физические показатели
Наряду с химическими, у золота есть и физические свойства, к которым относят:
- Невысокую твердость, по шкале Мооса от 2,5 до 3 единиц.
- Пластичность и ковкость.
- Желтый цвет.
Au не обладает высокой твердостью. В то время как алмазу присваивают 9 баллов по шкале Мооса, этот элемент удостоился всего 3. Чтобы повысить твердость Au, его сплавляют с другими металлами, в результате чего возникает лигатура, используемая для создания украшений. Драгоценности из чистого золота практически не встречаются, они тяжелые и легко деформируются при носке.
Для того чтобы идентифицировать металл, достаточно попробовать его на зуб. Можно укусить изделие, если оно легко поддается деформации и меняет форму, на поверхности остаются следы от зубов, то можно не сомневаться в его подлинности.
Au отличается ковкостью и пластичностью. Можно разрезать слиток ножом, не прилагая особых усилий, а также превратить кусок благородного металла в тонкий лист. Благодаря этому создают сусальное золото, которое используют в качестве декоративного материала: им покрывают купола церквей, защищая их от воздействия факторов окружающей среды.
Золото — единственный металл, который обладает желтым цветом. Этот оттенок повлиял на характеристики элемента, его ассоциировали с силой солнца. Металлу присваивали различные свойства, теплый оттенок свидетельствовал и о таинственном происхождении элемента.
Испокон веков Au ассоциируется у людей с богатством, высоким положением в обществе. В старину обычным людям не дозволялось носить золотые украшения, поскольку этой прерогативы были достойны только представители высшего общества.
Вода с сахаром
В воду добавляется сахар и размешивается до полного растворения. После в сладкую жидкость опускаются украшения из золота. Оставить их следует на три часа – так эффект будет максимальным. Благодаря сахару металл вновь заблестит, как новый. Только специалисты акцентируют внимание на том, что после процесса очищения украшения следует вымыть под проточной теплой водой, что избавит их от липкости.
Также немаловажно, что данный способ не подходит для украшений, которые загрязнены слишком сильно. Если требуется ликвидировать пыль и жир, сладкий раствор станет прекрасным вариантом.
Основным преимуществом этого варианта борьбы с загрязнениями на золоте считается его безопасность для металла. Очень важно не столько почистить ювелирные украшения, сколько не нанести им вред и еще более усугубить ситуацию.
Нахождения золота в природе
Среднее содержание его в земной коре 4,3•10-7 (по А. П. Виноградову). По возрастающей концентрации золото выстраивается в следующий ряд природных образований: морская вода, осадочные породы, кислые изверженные породы, средние изверженные породы, основные и ультраосновные изверженные породы, хромиты базальтоидных пород, гидротермальные руды.
В гидросфере содержание золота 1,0•10-9%, т.е. более чем на два порядка ниже среднего для земной коры. Однако общее количество в гидросфере огромно и составляет около 5-6 млн. т. Среднее содержание золота для всех видов пресных вод около 3,0•10-9%. Содержание золота в морской воде непостоянно: в полярных морях 5,0•10-9%, у берегов Европы 1-3,0•10-7%, в прибрежных зонах Австралии до 5,0•10-6%. Содержание золота в осадочных породах относительно низкое (1,79-4,57•10-7%). Вместе с тем с осадочными образованиями связано формирование промышленных концентраций (золотоносные россыпи). В изверженных породах среднее содержание золота отвечает величине 3,57• 10-7%, при этом имеется тенденция к повышению среднего содержания золота от кислых пород к основным.
Подвижность золота в геологических процессах главным образом связана с воздействием водных растворов. Наиболее реально нахождение золота в гидротермальных растворах в форме различных простых и смешанных моноядерных комплексов Au+1. К ним относятся гидроксильные, гидроксохлоридные и гидросульфидные комплексы. При повышенных содержаниях сурьмы и мышьяка возможно образование гетероядерных комплексов золота с этими элементами. Возможен перенос золота в атомарном виде. В низкотемпературных гидротермальных условиях, а также в поверхностных водах возможна миграция золота в виде растворимых металлоорганических комплексов, среди которых наиболее вероятны фульватные и гуматные комплексы. В гипергенных условиях миграция золота осуществляется в виде коллоидных растворов и механической взвеси. Для золота характерно разнообразие факторов, приводящих к его концентрированию и фиксации. Наряду с изменением температуры, давления и величины pH большую роль в концентрировании золота играет изменение окислительно-восстановительного потенциала среды. В процессах концентрирования золота значительна роль соосаждения и сорбции.
В природе золото главным образом встречается в виде золота самородного, а также в виде твёрдых растворов с серебром (электрум), медью (купроаурид), висмутом (бисмутоаурид), родием (родит), иридием (ирааурид) и платиной (платинистое золото). Известны теллуриды золота AuTe2 (калаверит) и AuTe3 (монтбрейит). Природные сульфиды золота не обнаружены, однако в ряде мест встречен сульфид золота и серебра утенбогардит (Ag3AuS2). Известен также ряд золотосодержащих теллуридов и сульфидов. Основные генетические типы месторождений золота смотреть в статье Золотые руды. Наиболее древний метод выделения золота — гравитационный — является ведущим процессом получения золотосодержащего концентрата. Начиная с 1-го тысячелетия до н.э. при извлечении золота из концентратов использовалось амальгамирование (растворение металлической ртутью с последующей отгонкой ртути). В конце 18 в. и в течение большей части 19 в. распространился метод хлорирования. Хлор пропускался через измельчённый рудный концентрат, и образующийся при этом хлорид золота вымывался водой. В 1843 П. Р. Багратионом предложен цианидный способ выделения золота, который широко используется и позволяет практически полностью выделить золото даже из самых бедных руд. Для извлечения золота рудный концентрат обрабатывается при доступе воздуха разбавленным раствором NaCN. При этом золото переходит в раствор, из которого затем выделяется действием металлического цинка. Очистка полученного тем или иным путём золота от примесей производится обработкой его горячей серной кислотой. Экономическое значение золота определяется его ролью основного валютного металла. В технике его используют в виде сплавов с другими металлами. Покрытие золотом применяют в авиационной и космической технике, для изготовления некоторых отражателей, электрических контактов и деталей проводников, а также в радиоаппаратуре. В электронике из золота, легированного Ge, In, Ga, Si, Sn и другими, изготовляют контакты. Значительная часть золота идёт на ювелирные изделия. Золото применяется также в медицине; радиоактивное золото (обычно 198Au) помогает диагностировать опухоли.
http://dragomet.com/zoloto/rastvorenie-zolota-v-tsarskoj-vodke-ochistka-proportsii-rastvora-kislot-osazhdenie-zolota-v-domashnih-usloviyah-i-ego-pereplavka-v-slitki/
http://tokyostreet.ru/dragocennye-kamni/chto-rastvoryaet-zoloto.html