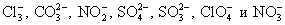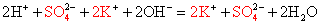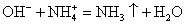Урок по теме «Реакции ионного обмена». 9-й класс
Класс: 9
Презентация к уроку
Учебник: Рудзитис Г.Е, Фельдман Ф.Г. Химия: учебник для 9 класса общеобразовательных учреждений / Г.Е. Рудзитис, Ф.Г. Фельдман. – 12-е изд. – М.: Просвещение, ОАО “Московские учебники”, 2009. – 191 с.
Цель: сформировать представление учащихся о реакциях, протекающих межу ионами, условий протекания реакций ионного обмена до конца, обратимых реакциях, полных и сокращенных ионных уравнениях.
Задачи:
- способствовать систематизации понятийного аппарата: ион, растворы, электролиты и неэлектролиты, основные типы реакций в неорганической химии, обратимые реакции, условия протекания реакций ионного обмена до конца
- “5” — обосновать, доказать;
- “4” — характеризовать, применить;
- “3” — рассказать;
- способствовать совершенствованию специальных предметных умений: составлять полные и сокращенные ионные уравнения;
- способствовать формированию общеучебных умений:
- а) учебно-интеллектуальных (анализировать факты, устанавливать причинно-следственные связи; выдвигать гипотезу; сравнивать соли и химические реакции, классифицировать, делать выводы);
- б) учебно-информационных (работать с текстом);
- в) учебно–организационных (понимать смысл задания, распределять время для выполнения заданий планировать работу по организации работы, осуществлять самоконтроль);
- способствовать формированию критического мышления учащихся (критически оценивать собственные знания по теме и сопоставлять их с научными);
Форма проведения: урок с использованием ИКТ, включением парных, индивидуальных форм организации учебно-познавательной деятельности учащихся.
Продолжительность учебного занятия: 45 минут.
Использование педагогических технологий: метод эвристического обучения, обучение в сотрудничестве
I. Организационный момент – 1 мин: мобилизующее начало (приветствие, проверка готовности к уроку, организация внимания учащихся), информация о цели и ходе урока, мотивация
Фронтальная беседа (3 мин)
- Что такое реакции обмена? (это реакции между двумя сложными веществами, при которых они обмениваются своими составными частями).
- Что такое ионы? (это заряженные частицы, которые отличаются от атомов числом электронов)
- На какие группы делятся ионы? (катионы – положительные ионы; анионы – отрицательные ионы)
- Что такое электролитическая диссоциация? (процесс распада молекул электролитов на ионы при растворении в воде или расплавлении)
- На какие ионы распадаются при электролитической диссоциации кислоты (ионы водорода и ионы кислотного остатка)
- На какие ионы распадаются при электролитической диссоциации растворимые основания? (ионы металла и ионы ОН -1 групп)
- На какие ионы распадаются при электролитической диссоциации соли? (ионы металла и ионы кислотного остатка)
- Таким образом, какие ионы выделяют при электролитической диссоциации? (Н +1 , ОН -1 , Ме +n , кислотный остаток -n )
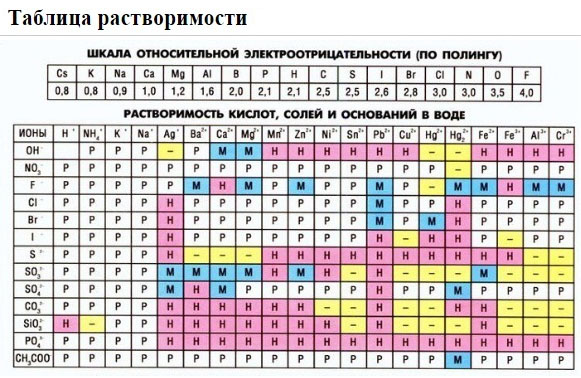
- Именно эти ионы находятся в таблице растворимости: (Работа с таблицей растворимости – определение растворимых и нерастворимых веществ)
II. Изучение нового материала. Объяснение учителя. 15 мин.
Реакции обмена протекают между ионами, поэтому называются реакции ионного обмена Выводится определение (слайд 2):
Реакции ионного обмена идут до конца в трех случаях:
- если образуется осадок – нерастворимое вещество после реакции)
- если выделяется газ
- если образуется вода
В остальных случаях реакции обмена являются обратимыми
Разберем эти случаи поподробнее (случаи разбираются на слайдах и на доске, проводится фронтальная беседа: почему реакция идет, что и почему образуется, как определить образование осадка, газа, воды и т.п.):
1) Если образуется осадок (слайд 3):
а) CuSO4 + 2NaOH 
б) 2AgNO3 + CaCl2 
в) Na2CO3 + Ca(NO3)2 
г) BaCl2 + K2SO4 
2) Если выделяется газ (слайд 4):
а) CaCO3 + 2HNO3 

б) Na2SO3 + 2HCl 

в) CuS + 2HCl 
3) Если образуется вода (слайд 5):
а) CuO + H2SO4 
б) Fe(OH)3 + 3HCl 
в) NaOH + HNO3 
4) Если НЕ образуются осадок, газ и вода, то реакции являются обратимыми (слайд 6):
Обратимые реакции – это реакции, которые при одних и тех же условиях протекают в двух противоположных направлениях
а) 2NaNO3 + CaCl2 
б) K3PO4 + 3NaCl 
в) CuCl2 + Na2SO4 
Ионные уравнения (слайды 7, 8, 9):
Для реакций ионного обмена составляют полные и сокращенные ионные уравнения. При этом на ионы никогда не раскладывают :
- нерастворимые вещества (см. таблицу растворимости);
- оксиды;
- воду;
- газы
1) Запишем молекулярное уравнение и уравняем его:
CuSO4 + 2NaOH 
2) Разложим на ионы все, что возможно и затем сократим одинаковые ионы в обоих частях уравнения:
Cu +2 + SO4 -2 + 2Na +1 + 2OH -1 

3) Запишем то, что получилось:
Cu +2 + 2OH -1 

Другие примеры составления ионных уравнений (разбираются с пояснениями):
CaCO3 + 2HNO3 

CaCO3 + 2H +1 + 2NO3 -1 
CaCO3 + 2H +1 
CuS + 2HCl 
CuS + 2H +1 + 2Cl -1 
CuS + 2H +1 
NaOH + HNO3 
Na +1 + OH -1 + H +1 + NO3 -1 
OH -1 + H +1 
K3PO4 + 3NaCl 
3K +1 + PO4 -3 + 3Na +1 + 3Cl -1 
Вывод: сокращенного ионного уравнения нет, следовательно, у обратимых реакций нет сокращенных ионных уравнений
III. Закрепление изученного материала (20 мин)
Учащимся предлагается выполнить задания в парах. Каждое задание предлагается на слайде и проверяется на следующем слайде (слайдах).
Задание 1 (Слайд 10)
Саша и Алеша делали домашнее задание. Они составили уравнения реакций, но случайно на лист бумаги пролили чернила. Помогите ученикам восстановить запись. Составьте к восстановленным
Проверка задания 1 (слайды 11, 12).
1) NaOH + HCl 
Na +1 + OH -1 + H +1 + Cl -1 
OH -1 + H +1 
2) MgCl2 + Na2SO3 

Mg +2 + 2Cl -1 + 2Na +1 + SO3 -2 

Mg +2 + SO3 -2 
3) K2SO3 + 2HNO3 
2K +1 + SO3 -2 + 2H +1 + 2NO3 -1 
SO3 -2 + 2H +1 
4) ZnSO4 + 2NaOH 

Zn +2 + SO4 -2 + 2Na +1 + 2OH -1 
Zn +2 + 2OH -1 
5) Al(OH)3 + 3HNO3 
Al(OH)3 + 3H +1 + 3NO3 -1 
Al(OH)3 + 3H +1 
6) CaCO3 + 2 HCl 
CaCO3 + 2H +1 + 2Cl -1 
CaCO3 + 2H +1 
Задание 2. (слайд 13):
Полные и сокращенные ионные уравнения к заданиям 2,3,4,5 дети должны будут сделать дома)
Колдунья с вороном отравили лечебный колодец, в котором был раствор хлористого кальция, который помогал целому городу. Он использовался горожанами при отравлениях, кровотечениях, аллергиях. Они превратили раствор СaCl2 в нерастворимый известняк CaCO3. Помогите жителям “расколдовать” колодец, если в вашем распоряжении есть растворы NaCl, Na2CO3, HCl, H2SO4, Zn(NO3)2.
Проверка задания 2 (слайд 14):
СаСО3 + 2HCl 
Задание 3 (слайд 15):
Олененок спешит к друзьям. Он шел долгих 3 дня. Ему осталось только перейти реку, но река оказалась испорчена – она наполнена раствором серной кислоты. Помогите Олененку воссоединиться с друзьями, если в вашем распоряжении есть растворы NaCl, Ba(OH)2 HCl, CuSO4, Ba(NO3)2.
Проверка задания 3 (слайд 16):
H2SO4 + Ba(OH)2 

Задание 4 (слайд 17):
Тигренок и крокодил поранились, а у доктора Айболита закончились все лекарства. У него в распоряжении есть некоторые химикаты: NaNO3, CuOH)2 H2SO4, НCl, BaCl2. Он знает, что раствор сульфата меди (II) может оказывать антисептическое, вяжущее, ранозаживляющее действие. Помогите доктору приготовить раствор и вылечить тигренка и крокодила.
Проверка задания 4 (слайд 18):
Cu(OH)2 + H2SO4 
Задание 5 (слайд 19):
Однажды русалка заметила, что ее друзья рыбы перестали с ней играть и уплывают подальше от ее дома. Она не могла понять, в чем дело, ведь они не ссорились. И тогда ее мама рассказала ей, что рыбы уплывают, потому что около их дома почти нет растений, и рыбам не хватает кислорода. Русалка подумала, что можно посадить растения, но они будут расти долго. А из старых мудрых книжек она узнала, что можно насытить воду углекислым газом – повышение концентрации СО2 в воде приводит к значительному ускорению в росте растений. В распоряжении русалки оказались: NaOH, ВaCO3, K2SO4, НCl, Ba(NO3)2. помогите русалке получить углекислый газ.
Проверка задания 5 (слайд 20):
BаСО3 + 2HCl 
IV. На следующем уроке мы продолжим разбирать тему “Реакции ионного обмена” и напишем небольшую проверочную работу, а сейчас .
Домашнее задание (слайд 21):
Параграф 4 упр. 1, 2, 3 стр. 22 и . не забудьте составить полные и сокращенные ионные уравнения к заданиям 2, 3, 4, 5, решенным в классе, иначе Ваша помощь сказочным персонажам не будет полной.
Ионные уравнения
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации. Разберем историю вопроса, алгоритм составления ионных уравнений и примеры задач.
ИСТОРИЯ ВОПРОСА
Еще древние алхимики, проводя нехитрые химические реакции в поисках философского камня и записывая в толстые фолианты результаты своих исследований, использовали определенные знаки для химических веществ. У каждого ученого была своя система, что неудивительно: каждый хотел защитить свои тайные знания от происков завистников и конкурентов. И лишь в VIII веке появляются единые обозначения для некоторых элементов.
В 1615 году Жан Бегун в своей книге «Начала химии», что по праву считается одним из первых учебников в этом разделе естествознания, предложил использовать условные обозначения для записи химических уравнений. И лишь в 1814 году шведский химик Йонс Якоб Берцелиус создал систему химических символов на основе одной или двух первых букв латинского названия элемента, подобную той, с которой ученики знакомятся на уроках.
В восьмом классе (параграф 12, учебник «Химия. 8 класс» под редакцией В.В. Еремина) ребята научились составлять молекулярные уравнения реакций, где и реагенты, и продукты реакций представлены в виде молекул.
Однако это упрощенный взгляд на химические превращения. И об этом задумывались ученые уже в XVIII веке.
Аррениус в результате своих экспериментов выяснил, что растворы некоторых веществ проводят электрический ток. И доказал, что вещества, обладающие электропроводностью, в растворах находятся в виде ионов: положительно заряженных катионов и отрицательно заряженных анионов. И именно эти заряженные частицы вступают в реакции.
ЧТО ТАКОЕ ИОННЫЕ УРАВНЕНИЯ
Ионные уравнения реакций — это химические равенства, в которых вещества, вступающие в реакцию, и продукты реакций обозначены в виде диссоциированных ионов. Уравнения данного типа подходят для записи химических реакций замещения и обмена в растворах.
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации (тема подробно разбирается в параграфе 10, учебник «Химия. 9 класс» под редакцией В.В. Еремина). В виде молекул записывают газы, вещества, выпадающие в осадок, и слабые электролиты, которые практически не диссоциируют. Газы обозначаются стрелкой вверх (↑), субстанции, выпадающие в осадок, стрелкой вниз (↓).
ОСОБЕННОСТИ ИОННЫХ УРАВНЕНИЙ
1. Реакции ионного обмена, в отличие от окислительно-восстановительных реакций, протекают без нарушения валентности веществ, вступающих в химические превращения.

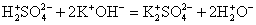
2. Реакции между ионами протекают при условии образования в ходе реакции плохорастворимого осадка, выделения летучего газа или образования слабых электролитов.
Удивительно, что реакции обмена могут проходить даже с нерастворимыми солями слабых кислот. В этом случае сильная кислота вытесняет слабую из ее солей. В качестве примера можно привести сокращенное ионное уравнение разведения карбоната кальция в сильных кислотах.
АЛГОРИТМ СОСТАВЛЕНИЯ ИОННОГО УРАВНЕНИЯ
Записываем молекулярное уравнение химического процесса.
Балансируем молекулярное уравнение с помощью коэффициентов.
Чтобы правильно сбалансировать равенство, нужно вспомнить закон сохранения массы веществ (параграф 12, «Химия. 8 класс» под редакцией В.В. Еремина), согласно которому в ходе химических превращений новые атомы не появляются, а старые не разрушаются. Т.е. число атомов в продуктах реакции равно числу атомов в исходных веществах. Помним, что водород и кислород уравниваем в последнюю очередь.
Определяем, какие вещества в химической реакции диссоциируют, т.е. распадаются на ионы.
Записываем в виде ионов:
- растворимые соли;
- сильные кислоты (H2SO4, HNO3, HCl и др.);
- растворимые в воде основания.
Записываем в виде молекул:
- нерастворимые соли;
- слабые кислоты, щелочи, вода;
- оксиды;
- газы;
- простые вещества;
- большинство органических соединений.
Если есть сомнения в растворимости реагента или продукта реакции, можно проверить по специальной таблице, которая является справочным материалом, ей можно пользоваться на различных экзаменах.
В таблице, помимо растворимости соединений, представлены также заряды катионов и анионов, участвующих в реакциях.
Определяем многоатомные ионы.
Это необходимо сделать, т.к. данные соединения не разлагаются на отдельные атомы и имеют свой заряд. Чаще всего в химических превращениях участвуют следующие многоатомные ионы:
Записываем равенство таким образом, чтобы все диссоциирующие субстанции были представлены в виде катионов и анионов.
Проверяем, чтобы уравнение было сбалансировано, т.е. количество различных атомов в частях с реагентами и продуктами реакции совпадало.
На данном этапе мы получили полное ионное уравнение.
Вычеркиваем идентичные ионы в обеих частях равенства, т.е. катионы и анионы с одинаковыми нижними индексами и зарядами, и переписываем равенство без данных ионов.
Проверяем, чтобы количество атомов элементов совпадало в правой и левой частях уравнения. Таким образом получаем краткое ионное уравнение.
ПРИМЕРЫ
Задача 1
Выясните, произойдет ли химическое взаимодействие между растворами гидроксида калия и хлорида аммония. (Записать для реакции молекулярное, полное ионное и сокращенное ионное уравнение.)
Записываем молекулярное уравнение, проверяем коэффициенты.
Помним, что гидроксид аммония — нестабильное соединение и разлагается на аммиак и воду.
Записываем окончательное уравнение:
NB! Благодаря летучести и резкому раздражающему запаху 3%-й раствор NH3 называется «нашатырный спирт» и используется в медицине.
Подсматривая в таблицу растворимости, помечаем полное ионное уравнение, не забывая о зарядах ионов.
Вычеркивая идентичные катионы и анионы в обеих частях реакции, составляем краткое ионное уравнение.
Делаем вывод: химическая реакция между гидроксидом калия и хлоридом аммония протекает с образованием воды и выделением аммиака — летучего газа с резким запахом.
Задача 2
А сейчас выполним задание из учебника «Химия. 9 класс» под редакцией В.В. Еремина.
Налейте в пробирку 1 мл раствора карбоната натрия и аккуратно прилейте к нему пару капелек соляной кислоты.
Составьте уравнение реакции, напишите полное и сокращенное ионные уравнения.
Записываем реакцию в молекулярном виде, расставляем коэффициенты, если это необходимо.
Подсматривая в таблицу растворимости, записываем полное ионное уравнение, не забывая отмечать заряды ионов.
Вычеркивая одинаковые катионы и анионы в правой и левой частях равенства, составляем краткое ионное уравнение.
Вопрос «Что происходит?» остался без ответа. К сожалению, в домашних условиях этот опыт осуществить трудновато, так как стиральной содой уже давно никто не пользуется, да и соляную кислоту в аптеке уже не продают. Но примерно такой же визуальный эффект можно наблюдать, если смешать раствор пищевой соды с раствором уксусной кислоты.
Реакции ионного обмена
Этот видеоурок доступен по абонементу
У вас уже есть абонемент? Войти
Урок посвящен изучению темы «Реакции ионного обмена». На нём вы рассмотрите сущность реакций, протекающих между растворами кислот, солей и щелочей. Для этого будут записаны уравнение реакции между двумя веществами. На уроке будет дано определение новому понятию реакции ионного обмена.
http://rosuchebnik.ru/material/ionnye-uravneniya/
http://interneturok.ru/lesson/chemistry/9-klass/bhimicheskaya-svyaz-elektroliticheskaya-dissociaciyab/reaktsii-ionnogo-obmena