S al2s3 h2s na2s nahs составьте уравнения
Вопрос по химии:
Как составить уравнение следующих реакций S-Al2S3-H2S-Na2S
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 1
2Al + 3S = Al₂S₃
Al₂S₃ + 6HCl = 2AlCl₃ + 3H₂S
H₂S + 2NaOH = Na₂S + 2H₂O
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Составьте уравнения следующих перевоплощений: S FeS H2S NaHS
Составьте уравнения последующих перевоплощений: S FeS H2S NaHS Для уравнения 1 составьте схему электрического баланса. Для уравнения 2 укажите тип реакции. Для реакции 3 напишите молекулярное и ионно-молекулярное уравнение.
- Брюшкова Мила
- Химия 2019-01-26 10:11:11 3 1
1)S+Fe=FeS
+2e= -окислитель
-2e= -восстановитель
2)FeS+2HCl=FeCl2+H2S-реакция размена
3)H2S+NaOH=H2O+NaHS
Готовые домашние задания, готовые задачи по химии и биологии
Характеристика сульфидов. Задачи 851 — 854
Свойства и получение сульфидов
Задача 851.
Почему сульфид цинка растворяется в соляной кислоте, а сульфид меди нет? В какой кислоте можно растворить сульфид меди?
Решение:
Взаимодействие сульфида цинка с соляной кислотой выражается уравнением:
ZnS(к) + 2HCl ↔ ZnCl2 + H2S(г)
ZnS + 2H + ↔ Zn 2+ + H2S
Присутствие в числе исходных веществ малорастворимого электролита ZnS, при образовании которого связываются ионы S 2- , обуславливает протекание реакции влево. С другой стороны, при образовании слабого электролита H2S также связываются ионы S 2- , способствующие протеканию реакции вправо. Таким образом, ионы S 2- участвуют в двух процессах, приводящих к установлению двух равновесий:
S 2- + Zn 2+ ↔ ZnS(к);
S 2- + 2Н + ↔ Н 2 S(г).
Протекание того или иного процесса зависит от того, какое из двух веществ – сероводород или сульфид цинка – в большей степени связывает ионы S 2- . Константа диссоциации H2S (K = K1 . K2 = 6 . 10 -22 ), произведение растворимости ZnS равно 1,3 . 10 -23 . Из чего вытекает, что связывание ионов S 2- в молекулы H2S происходит полнее, чем в ZnS. Поэтому рассматриваемая реакция протекает вправо – сульфид цинка растворяется в соляной кислоте. Аналогично два равновесия устанавливаются в системе CuS—HCl:
S 2- +Cu 2+ ↔ CuS(к);
S 2- + 2Н + ↔ Н2S(г).
Но произведение растворимости CuS равно 3,2 . 10 -38 , что меньше, чем 6 . 10 -22 . Поэтому связывание ионов S 2- в CuS происходит полнее, чем в молекулах H2S и, равновесие в системе:
сместится влево; сульфид меди не растворим в растворе соляной кислоты. Следовательно, сульфид меди растворится в растворе той кислоты, суммарная константа диссоциации которой будет иметь меньшее численное значение, чем ПР(CuS), например, ортокремниевая кислота H4SiO4 численное значение К = К1 . К2 . К3 . К4 = 8 . 10 -48 .
Задача 852.
Каковы продукты реакции взаимодействия хлорида железа (III): а) с сероводородом; б) с сульфидом аммония?
Решение:
а) Хлорид железа (III) и сероводород реагируют с образованием хлорида железа (II), серы и хлороводорода:
Данная реакция протекает по окислительно-восстановительному механизму, где роль окислителя играет FeCl3, а восстановителя – H2S.
б) Между хлоридом железа (III) и сульфидом аммония протекает реакция по обменному механизму с образованием сульфида железа (III) и хлорида аммония:
Задача 853.
Объяснить, почему ZnS и РbS можно получить обменной реакцией в водном растворе, а Al2S3 и Cr2S3 нельзя. Указать способ получения Al2S3 и Cr2S3.
Решение:
Малорастворимые сульфиды металлов можно осадить из растворов солей действием сероводорода или сульфида аммония:
Являясь солями слабой кислоты, растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих элементы в высоких степенях окисления Al2S3 и Cr2S3 и др.), часто идет до конца, он необратим. Поэтому Al2S3 и Cr2S3 нельзя получить обменной реакцией в водном растворе. Обычно для их получения используют сплавление метала с серой в отсутствие кислорода и влаги:
2Al + 3S 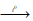
2Cr + 3S 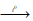
Сульфид хрома поучают:
Сплавление оксида хрома(III) с сероводородом:
2Cr2O3 + 9S 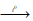
Пропускание сероводорода через нагретый оксид хрома(III):
Cr2O3 + 3H2S 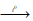
Задача 854.
Какова реакция среды в растворах: а) Na2S; 6) (NH4)2S; в) NaНS?
Решение:
а) Na2S – соль сильного основания и слабой кислоты, гидролизующаяся по аниону:
Na2S ↔ 2Na + + S 2- ;
S 2- + H2O ↔ HS — + OH — (ионно-молекулярная форма);
Na2S + H2O ↔ NaHS + NaOH (молекулярная форма).
Гидролиз преимущественно протекает по первой ступени, при этом образуется избыток ионов ОН — , которые придают раствору соли щелочную среду, рН > 7.
б) (NH4)2S – соль слабого однокислотного основания и слабой двухосновной кислоты, гидролизуется как по катиону, так и по аниону:
(NH4)2S ↔ 2NH4 + + S 2- ;
NH4 + + H2O ↔ NH4OH + H + (ионно-молекулярная форма);
S 2- + H2O ↔ HS — + NH4OH (ионно-молекулярная форма).
При гидролизе солей, образованных слабым основанием и слабой кислотой в растворе образуются в избытке как ионы Н + так и ионы ОН — , которые взаимодействуя друг с другом образуют Н2О:
Н + + ОН — ↔ Н2О
Казалось бы, реакция среды должна быть нейтральной по причине образования воды, но, на самом деле, реакция среды бывает или слабокислой, или слабощелочной, что зависит от силы кислоты и основания, образующие соль. Так, если КD основания меньше, чем KD кислоты, то гидролиз соли будет преимущественно протекать по катиону и, следовательно, в растворе будут незначительно преобладать ионы водорода Н + , что придаст раствору слабокислую среду, рН раствора будет незначительно меньше семи. Так как KD(H2S) — , что придаёт ему слабощелочную среду, рН > 7.
в) NaНS – кислая соль слабой кислоты и сильного основания, которая будет гидролизоваться по аниону:
NaHS ↔ Na + + HS — ;
HS — + H2O ↔ H2S + OH — (ионно-молекулярная форма);
NaHS + H2O ↔ H2S + NaOH (молекулярная форма).
При гидролизе гидросульфида натрия образуется избыток ионов ОН — , которые придают раствору соли щелочную среду, рН > 7.
http://obrazovalka.com/qa/ximiya/1875934-sostavte-uravnenija-sledujushhih-perevoploshhenij-s-fes-h2s-nahs.html
http://buzani.ru/2-uncategorised/1279-kharakteristika-sulfidov-zadachi-851-854