Оксид серы (VI)
Оксид серы (VI) – это кислотный оксид. При обычных условиях – бесцветная ядовитая жидкость. На воздухе «дымит», сильно поглощает влагу.
Способы получения. Оксид серы (VI) получают каталитическим окислением оксида серы (IV) кислородом.
Сернистый газ окисляют и другие окислители, например , озон или оксид азота (IV):
Еще один способ получения оксида серы (VI) – разложение сульфата железа (III):
Химические свойства оксида серы (VI)
1. Оксид серы (VI) активно поглощает влагу и реагирует с водой с образованием серной кислоты:
2. Серный ангидрид является типичным кислотным оксидом , взаимодействует с щелочами и основными оксидами.
Например , оксид серы (VI) взаимодействует с гидроксидом натрия. При этом образуются средние или кислые соли:
Еще пример : оксид серы (VI) взаимодействует с оксидом оксидом (при сплавлении):
SO3 + MgO → MgSO4
3. Серный ангидрид – очень сильный окислитель , так как сера в нем имеет максимальную степень окисления (+6). Он энергично взаимодействует с такими восстановителями, как йодид калия, сероводород или фосфор:
4. Растворяется в концентрированной серной кислоте, образуя олеум – раствор SO3 в H2SO4.
Урок №14. Серный ангидрид и серная кислота
Повторите темы уроков 9 класса:
Оксид серы (VI)
Оксид серы (VI) – это кислотный оксид. При обычных условиях – бесцветная ядовитая жидкость, «дымит» на воздухе, поглощая пары воды.
Способы получения
Оксид серы (VI) получают в реакциях окисления:
SO 2 + NO 2 = SO 3 + NO
Разложением сульфата железа (III):
Химические свойства оксида серы (VI)
1. Оксид серы (VI) активно поглощает влагу и реагирует с водой с образованием серной кислоты:
2. Серный ангидрид – типичным кислотный оксид, взаимодействует с щелочами и основными оксидами.
SO 3 + 2NaOH ( избыток) = Na 2 SO 4 + H 2 O
SO 3 + NaOH ( избыток) = NaHSO 4
SO 3 + MgO = t = MgSO 4
3. Серный ангидрид – очень сильный окислитель:
SO 3 + 2KI = I 2 + K 2 SO 3
3SO 3 + H 2 S = 4SO 2 + H 2 O
5SO 3 + 2P = P 2 O 5 + 5SO 2
4. Растворяется в концентрированной серной кислоте, образуя олеум – раствор SO 3 в H 2 SO 4
РЕАКЦИИ СЕРНОЙ КИСЛОТЫ
Химические свойства разбавленной серной кислоты
H 2 SO 4 — сильная двухосновная кислота, водный раствор изменяет окраску индикаторов (лакмус и универсальный индикатор краснеют)
1) Диссоциация протекает ступенчато:
(первая ступень, образуется гидросульфат – ион)
HSO 4 — → H + + SO 4 2-
(вторая ступень, образуется сульфат – ион)
H 2 SO 4 образует два ряда солей — средние (сульфаты) и кислые (гидросульфаты)
2) Взаимодействие с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
Zn 0 + H 2 +1 SO 4 (разб) → Zn +2 SO 4 + H 2 0 ↑
Zn 0 + 2H + → Zn 2+ + H 2 0 ↑
3) Взаимодействие с основными и амфотерными оксидами:
CuO + H 2 SO 4 → CuSO 4 + H 2 O
CuO + 2H + → Cu 2+ + H 2 O
4) Взаимодействие с основаниями:
H 2 SO 4 + 2NaOH → Na 2 SO 4 + 2H 2 O
Если кислота в избытке, то образуется кислая соль:
H 2 SO 4 + NaOH → NaНSO 4 + H 2 O
H 2 SO 4 + Cu(OH) 2 → CuSO 4 + 2H 2 O
2H + + Cu(OH) 2 → Cu 2+ + 2H 2 O
5) Обменные реакции с солями:
Серная кислота – сильная нелетучая кислота, вытесняет из солей другие менее сильные кислоты:
MgCO 3 + H 2 SO 4 → MgSO 4 + H 2 O + CO 2 ↑
MgCO 3 + 2H + → Mg 2+ + H 2 O + CO 2 ↑
Н 2 SO 4 + 2NaHCO 3 = Na 2 SO 4 + CO 2 ↑ + H 2 O
H 2 SO 4 + Na 2 SiO 3 = Na 2 SO 4 + H 2 SiO 3 ↓
Качественная реакция на сульфат-ион
BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓
Образование белого осадка BaSO 4 (нерастворимого в кислотах) используется для идентификации серной кислоты и растворимых сульфатов.
6) Реагирует с аммиаком
Химические свойства концентрированной серной кислоты
1. С водой образуются гидраты:
H 2 SO 4 + nH 2 O = H 2 SO 4 ·nH 2 O + Q
Органические вещества обугливаются!
2H 2 SO 4 + C = CO 2 + 2SO 2 + 2H 2 O
2. Серная кислота окисляет неметаллы
неМе + H 2 SO 4 (конц.) = H 2 O + SO 2 + Кислотный гидроксид
, где степень окисления неметалла – высшая
C + 2H 2 SO 4 = 2H 2 O + CO 2 + 2SO 2
S + 2H 2 SO 4 = 3SO 2 + 2H 2 O
2P + 5H 2 SO 4 = 2H 3 PO 4 + 5SO 2 + 2H 2 O
3. Взаимодействие серной кислоты с металлами
H 2 SO 4 (конц.) + Me = t = соль + H 2 O + Х
Концентрированная серная кислота является сильным окислителем. При этом она обычно восстанавливается до сернистого газа SO 2 . С активными металлами может восстанавливаться до серы S, или сероводорода Н 2 S.
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании образуется газа SO 2 :
6H 2 SO 4 (конц.) + 2Fe = t = Fe 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
6H 2 SO 4(конц.) + 2Al = t = Al 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
2H 2 SO 4 (конц.) + Cu = CuSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + Hg = HgSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + 2Ag = Ag 2 SO 4 + SO 2 ↑ + 2H 2 O
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
3Mg + 4H 2 SO 4 = 3MgSO 4 + S + 4H 2 O
При взаимодействии со щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
5H 2 SO 4 (конц.) + 4Zn = 4ZnSO 4 + H 2 S↑ + 4H 2 O
4. Взаимодействие с восстановителями
Концентрированная серная кислота окисляет галогеноводороды и сероводород при комнатной температуре:
3H 2 SO 4 (конц.) + 2KBr = Br 2 ↓ + SO 2 ↑ + 2KHSO 4 + 2H 2 O
5H 2 SO 4 (конц.) + 8KI = 4I 2 ↓ + H 2 S↑ + K 2 SO 4 + 4H 2 O
H 2 SO 4 (конц.) + 3H 2 S = 4S↓ + 4H 2 O
СОЛИ СЕРНОЙ КИСЛОТЫ
1) Разложение сульфатов
Термически устойчивые сульфаты – сульфаты щелочных металлов (в том числе лития), они плавятся не разлагаясь
Остальные сульфаты при нагревании разлагаются на оксид серы(IV), оксид металла и кислород:
2CuSO 4 = t = 2CuO + SO 2 + O 2 (SO 3 )
2Al 2 (SO 4 ) 3 = t = 2Al 2 O 3 + 6SO 2 + 3O 2
2ZnSO 4 = t = 2ZnO + SO 2 + O 2
2Cr 2 (SO 4 ) 3 = t = 2Cr 2 O 3 + 6SO 2 + 3O 2
Следует быть осторожнее с сульфатами железа (II) и хрома (II) , эти металлы при наличии окислителя склонны окисляться до степени окисления +3, а тут как раз выделяется кислород:
4FeSO 4 = t = 2Fe 2 O 3 + 4SO 2 + O 2
Так как оксиды тяжёлых и благородных металлов разлагаются сами, разложение их сульфатов следует записывать до металла:
Ag 2 SO 4 = t = 2Ag + SO 2 + O 2
HgSO 4 = t = Hg + SO 2 + O 2
2) Сульфаты проявляют окислительные свойства и могут взаимодействовать с восстановителями, восстанавливаясь до сульфидов.
CaSO 4 + 4C = CaS + 4CO
3) Многие средние сульфаты образуют устойчивые кристаллогидраты
Na 2 SO 4 ∙ 10H 2 O − глауберова соль
CaSO 4 ∙ 2H 2 O − гипс
CuSO 4 ∙ 5H 2 O − медный купорос
FeSO 4 ∙ 7H 2 O − железный купорос
ZnSO 4 ∙ 7H 2 O − цинковый купорос
Na 2 CO 3 ∙ 10H 2 O − кристаллическая сода
Оксид серы (VI) SO3, серный ангидрид
Взаимодействуя с кислородом, сера образует два оксида:
- SO2 (IV) — сернистый газ (сернистый ангидрид, диоксид серы)
- SO3 (VI) — серный ангидрид
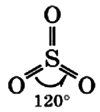
Молекула сернистого газа сильно полярна, угловой формы (угол между связями составляет 119°):
В таком виде молекула серного ангидрида может находиться только в газообразном состоянии.
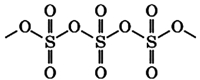
В жидком и твердом состоянии происходит полимеризация молекул:
Физические свойства серного ангидрида:
- бесцветная жидкость;
- при температуре менее 16,8°C серный ангидрид превращается в белую кристаллическую массу;
- обладает высокой гигроскопичностью.
Химические свойства серного ангидрида
Оксид серы (VI) является типичным кислотным оксидом:
- с основаниями реагирует с образованием гидросульфатов (кислых солей) и сульфатов (средних солей):
- с основными оксидами реагирует с образованием сульфатов:
- с водой реагирует бурно, при этом образуется серная кислота:
Серный ангидрид очень хорошо растворяется в серной кислоте, образуя раствор, называемый олеумом:
В кислотно-восстановительных реакциях выступает в роли сильного окислителя, восстанавливаясь до сернистого ангидрида:
Получение и применение серного ангидрида
В промышленных целях серный ангидрид получают путем окисления сернистого газа в присутствии катализатора:
Серный ангидрид используют для получения серной кислоты, а также, в качестве сульфирующего и обезвоживающего реагента.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://www.sites.google.com/site/himulacom/%D0%B7%D0%B2%D0%BE%D0%BD%D0%BE%D0%BA-%D0%BD%D0%B0-%D1%83%D1%80%D0%BE%D0%BA/11-%D0%BA%D0%BB%D0%B0%D1%81%D1%81-%D1%87%D0%B5%D1%82%D0%B2%D1%91%D1%80%D1%82%D1%8B%D0%B9-%D0%B3%D0%BE%D0%B4-%D0%BE%D0%B1%D1%83%D1%87%D0%B5%D0%BD%D0%B8%D1%8F/%D1%83%D1%80%D0%BE%D0%BA-14-%D1%81%D0%B5%D1%80%D0%BD%D1%8B%D0%B9-%D0%B0%D0%BD%D0%B3%D0%B8%D0%B4%D1%80%D0%B8%D0%B4-%D0%B8-%D1%81%D0%B5%D1%80%D0%BD%D0%B0%D1%8F-%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0
http://prosto-o-slognom.ru/chimia/503_oksid_sery_SO3.html