Сероводород
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода похожа на структуру воды — уголковая молекула. Но валентный угол H-S-H меньше, чем угол H-O-H в воде и составляет 92,1 о .
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например , при действии соляной кислоты на сульфид железа (II):
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: х лорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например , сероводород реагирует с гидроксидом натрия:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
2. Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
Например , азотная кислота окисляет сероводород до молекулярной серы:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например , оксид серы (IV) окисляет сероводород:
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например , сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Сероводород и концентрированная азотная кислота уравнение
Для выполнения задания используйте следующий перечень веществ: азотная кислота, сероводород, нитрат калия, хлорид натрия, нитрат свинца (II). Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна окислительно-восстановительная реакция, и запишите уравнение этой реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
Для выполнения задания используйте следующий перечень веществ: азотная кислота, сероводород, нитрат калия, хлорид натрия, нитрат свинца (II). Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Можно же еще вариант: нитрат свинца+хлорид натрия= хлорид свинца в осадке
Запишем уравнение реакции концентрированной азотной кислоты и сероводорода:
Составим электронный баланс:
Сера в степени окисления −2 (сероводород) является восстановителем. Азот в степени окисления +5 (азотная кислота) — окислителем.
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Ответ правильный и полный, содержит следующие элементы: — выбраны вещества, и записано уравнение окислительно-восстановительной реакции; Химия, Биология, подготовка к ГИА и ЕГЭОкислительные свойства азотной кислоты. ОВР в статье специально выделены цветом . Обратите на них особое внимание. Эти уравнения могут попасться в ЕГЭ. автор статьи — Саид Лутфуллин Азотная кислота – в любом виде (и разбавленная, и концентрированная) является сильным окислителем.
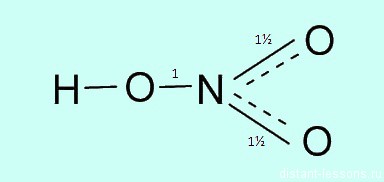
Окислительные свойства обеспечиваются азотом в высшей степени окисления +5 Какая валентность у азота в этом соединении? Вопрос очень хитрый, многие отвечают на него корректно. У азота в азотной кислоте валентность IV .
Три связи с каждым атомом кислорода, и четвертая как бы распределяется, образуется полуторная связь. Таким образом, валентность азота IV, а степень окисления +5 Первое самое интересное свойство: взаимодействие с металлами.
Схема реакции азотной кислоты (и разбавленной, и концентрированной) с металлами: HNO 3 + Ме → нитрат + H 2 O + продукт восстановленного азота
2. С платиной и золотом концентрированная азотная кислота не реагирует вообще. Чтобы понять до чего вообще может восстанавливаться азот, посмотрим на диаграмму его степеней окисления: Азот +5 – окислитель, будет восстанавливаться, то есть понижать степень окисления.
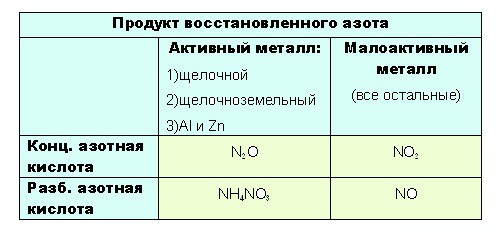
(Не все конечно, такие реакции вообще что угодно дать могут, но в ЕГЭ образуются только эти). Определить какой именно продукт будет образовываться можно чисто логически:
Остальные металлы восстанавливают азотную кислоту до +2 или +4, с образованием продуктов соответственно: NO или O 2.
(обратите внимание, что железо окисляется до высшей степени окисления) Если тяжело сразу понять всю логичность выбора, вот таблица: А зотная кислота окисляет неметаллы до высших оксидов. Так как неметаллы – не такие сильные восстановители, как активные металлы, азот может восстановиться только до +4, образовав NO 2 или NO соответственно. При окислении неметаллов концентрированной азотной кислотой образуется бурый газ ( NO 2), а если кислота разбавленная, то образуется NO . Схемы реакций следующие: неметалл + HNO 3(разб.) → соединение неметалла в высшей степени окисления + NO неметалл + HNO 3(конц.) → соединение неметалла в высшей степени окисления + NO 2 (угольная кислота не образуется, так как она не стабильна)
Образовавшийся иод окисляется дальше до иодноватой кислоты, поэтому реакцию можно записать сразу: То же самое происходит при взаимодействии с иодо- и бромоводородами: Реакции с золотом, магнием, медью и серебром источники: http://chem-ege.sdamgia.ru/problem?id=10319 http://distant-lessons.ru/okislitelnye-svojstva-azotnoj-kisloty.html |