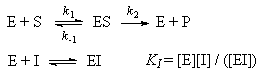Широко используемое в ферментативном катализе уравнение
Во многих случаях скорость реакции резко изменяется в присутствии специальных веществ — катализаторов. Катализаторы участвуют в реакции, но в результате ее не расходуются. Катализаторы биологических процессов, протекающих в живых организмах, представляют собой белковые молекулы, которые называют ферментами, или энзимами.
Простейшая схема ферментативного катализа включает обратимое образование промежуточного комплекса фермента (E) с реагирующим веществом (субстратом, S) и разрушение этого комплекса с образованием продуктов реакции (P):
Применение квазиравновесного приближения к этой схеме (при условии k2 > k1). Применение этого метода к простейшей схеме катализа дает уравнение Михаэлиса-Ментен:

где wmax = k2 . [E]0 — максимальная скорость реакции (при бесконечно большой концентрации субстрата),
— константа Михаэлиса. Эта константа равна концентрации субстрата, при которой скорость реакции равна половине максимальной скорости. Типичные значения KM — от 10 -6 до 10 -1 моль/л. Константу скорости k2 иногда называют числом оборотов фермента. Она может изменяться в пределах от 10 до 10 8 мин -1 .
Уравнение (7.2) можно записать в других координатах, более удобных для обработки экспериментальных данных:

(координаты Лайнуивера-Берка) или

Для определения параметров KM и wmax по уравнениям (7.2а) и (7.2б) проводят серию измерений начальной скорости реакции от начальной концентрации субстрата и представляют экспериментальные данные в координатах 1/w0 ё 1/[S]0 или w0 ё w0/[S]0.
Иногда течение ферментативной реакции осложняется присутствием ингибиторов — веществ, способных образовывать комплексы с ферментом или фермент-субстратным комплексом. Различают конкурентное, неконкурентное и смешанное ингибирование.
При конкурентном механизме ингибитор (I) конкурирует с субстратом за активные участки фермента. Простейшая кинетическая схема данного процесса имеет вид:
Применение квазистационарного приближения к комплексу ES и квазиравновесного приближения к комплексу EI с учетом уравнений материального баланса [E] + [ES] + [EI] = [E]0 и [I] » [I]0 дает для скорости реакции уравнение типа (7.2):

где эффективная константа Михаэлиса связана с исходной концентрацией ингибитора:

Величину KI = [E]. [I] / [EI], которая представляет собой константу диссоциации комплекса фермента с ингибитором, называют константой ингибирования. Таким образом, при конкурентном ингибировании увеличивается константа Михаэлиса, а максимальная скорость ферментативной реакции остается неизменной.
При неконкурентном механизме ингибитор обратимо связывает промежуточный комплекс фермента с субстратом. Простейшая кинетическая схема данного процесса имеет вид:

где предполагается, что константы диссоциации комплексов EI и ESI одинаковы: [E]. [I] / [EI] = [ES]. [I] / [ESI] = KI. Применение квазистационарного приближения к комплексу ES и квазиравновесного приближения к комплексам EI и ESI с учетом уравнений материального баланса [E] + [ES] + [EI] + [ESI] = [E]0 и [I] » [I]0 дает для скорости реакции уравнение типа (7.2):

где эффективная максимальная скорость связана с начальной концентрацией ингибитора выражением:
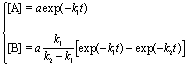
При неконкурентном ингибировании максимальная скорость реакции уменьшается, а константа Михаэлиса остается неизменной.
Смешанное ингибирование описывается более сложными кинетическими схемами. При смешанном ингибировании изменяются и константа Михаэлиса, и максимальная скорость ферментативной реакции.
Пример 7-1. Найдите константу Михаэлиса и максимальную скорость гидролиза аденозинтрифосфата, катализируемого миозином, по следующим кинетическим данным:
Решение. Уравнение Михаэлиса-Ментен в данных координатах имеет вид (7.2б), следовательно, точки пересечения с осями имеют координаты: (0;wmax) для оси ординат, (wmax/KM;0) для оси абсцисс. Первая точка пересечения дает значение wmax = 2.1 . 10 -6 моль/(л. с). Вторая точка позволяет найти константу Михаэлиса: wmax/KM = 14.6 . 10 -3 с -1 , KM = 2.1 . 10 -6 / 14.6 . 10 -3 = 1.44 . 10 -4 моль/л.
Пример 7-2. Ферментативная реакция (KM = 2.7 . 10 -3 моль/л) подавляется конкурентным ингибитором (KI = 3.1 . 10 -5 моль/л). Концентрация субстрата равна 3.6 . 10 -4 моль/л. Сколько ингибитора понадобится для подавления реакции на 65%? Во сколько раз надо повысить концентрацию субстрата, чтобы уменьшить степень подавления до 25%?
Решение. 1) Конкурентное ингибирование описывается формулами (7.3) и (7.3а). 65%-ное подавление реакции означает, что скорость ингибируемой реакции составляет 35% от скорости реакции в отсутствие ингибитора:

откуда следует, что

В этой формуле известны значения KM, KI и [S]. Концентрация ингибитора равна:

Уменьшение степени ингибирования до 25% означает, что скорость ингибируемой реакции составляет 75% от нормальной:

где в данном случае известны KM, KI и [I]0. Отсюда можно выразить искомую концентрацию субстрата:

Таким образом, для уменьшения степени ингибирования до 25% концентрацию субстрата надо увеличить в 1.4 . 10 -2 / 3.6 . 10 -4 = 40 раз.
7-1. Гидролиз ацетилхолина катализируется ферментом ацетилхолинэстеразой, число оборотов которой составляет 25000 с -1 . Сколько времени потребуется ферменту для расщепления одной молекулы ацетилхолина? (ответ)
7-2. Для некоторой ферментативной реакции константа Михаэлиса равна 0.035 моль/л. Скорость реакции при концентрации субстрата 0.110 моль/л равна 1.15 . 10 -3 моль/(л. с). Найдите максимальную скорость этой реакции.(ответ)
7-3. Начальная скорость окисления сукцината натрия в фумарат натрия под действием фермента сукциноксидазы была измерена для ряда концентраций субстрата:
0.0005
0.00033
Определите константу Михаэлиса данной реакции.(ответ)
7-4. Начальная скорость выделения O2 при действии фермента на субстрат была измерена для ряда концентраций субстрата:
0.002
Определите константу Михаэлиса данной реакции.(ответ)
7-5. Найдите константу Михаэлиса и максимальную скорость каталитического разложения гидроперекиси тетралина по следующим кинетическим данным:
7-6. Найдите константу Михаэлиса и максимальную скорость каталитического окисления циклогексена трет-бутилпероксидом по следующим кинетическим данным:
7-7. Найдите константу Михаэлиса и максимальную скорость гидролиза карбобензилоксиглицилфенилаланина под действием карбоксипептидазы по следующим кинетическим данным:
7-8. Рассчитайте концентрацию неконкурентного ингибитора I (KI = 2.9 . 10 -4 моль/л), необходимую для 90%-ного подавления ферментативной реакции.(ответ)
7-9. В некоторых случаях кинетические исследования ферментативных реакций проводят в условиях избытка фермента. Выведите уравнение Михаэлиса-Ментен, описывающее зависимость начальной скорости ферментативной реакции от начальных концентраций фермента и субстрата в системе
при условии, что концентрация фермента намного больше концентрации субстрата.(ответ)
*7-10. Рассмотрите механизм ферментативного катализа с двумя промежуточными комплексами:
Используя метод квазистационарных концентраций и уравнение материального баланса, покажите, что скорость реакции описывается уравнением типа Михаэлиса-Ментен (7.2). Найдите выражения для эффективной максимальной скорости и эффективной константы Михаэлиса через константы скорости отдельных стадий.(ответ)
7-11. Запишите уравнения конкурентного и неконкурентного ингибирования в координатах Лайнуивера-Берка. Представьте эти уравнения в графическом виде для трех разных начальных концентраций ингибитора (включая [I]0 = 0). Объясните, как можно определить константу ингибирования.(ответ)
7-12. Запишите уравнения конкурентного и неконкурентного ингибирования в координатах w0 
*7-13. Рассмотрите схему неконкурентного ингибирования с разными константами диссоциации комлпексов:
Используя квазистационарное приближение для ES и квазиравновесное приближение для EI и ESI, найдите начальную скорость реакции. Как связаны максимальная скорость реакции и константа Михаэлиса с соответствующими величинами для неингибируемой реакции?(ответ)


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Ферментативный катализ. Уравнение Михаэлиса-Ментена
Ферментами (энзимами) называются вещества белковой природы, которые ускоряют химические реакции, протекающие в клетках и тканях живого организма. Поэтому их еще называют биокатализаторами, а словами академика Павлова «возбудителями жизни».
Молекула фермента имеет чередующиеся полярные группы СООН, NH2, NH, OH, SH и др. и неполярные гидрофобные группы (первичная структура). Макромолекула фермента может изгибаться и свертываться в клубки с образованием внутримолекулярных водородных связей (вторичная структура белка). Сложные ферменты содержат ионы металлов с переменной степенью окисления (Fe, Cu), которые участвуют в окислительно-восстановительных реакциях. Ферменты классифицируют по типу катализируемой реакции: гидролазы (реакции гидролиза), изомеразы (изомерные превращения), оксиредуктазы (окислительно-восстановительные реакции). Активные центры фермента способны избирательно связывать молекулу реагирующего вещества (субстрата), образую с ней единый фермент-субстратный комплекс. Большое значение имеет геометрическое соответствие структур активного центра фермента и самого субстрата – «ключ-замок».
Активность ферментов в миллионы раз выше химических катализаторов.
Ферментативный катализ занимает промежуточное положение между гомогенным и гетерогенным катализом. Его отличительные черты: высокая каталитическая активность (малые количества фермента и высокие скорости), специфичность или селективность действия (один фермент ускоряет определенную реакцию), низкие температуры и сильное влияние рН среды и присутствия других веществ. Ингибиторами (I) называют вещества, осложняющие течение ферментативной реакции вследствие образования комплексов с ферментом или фермент-субстратным комплексом.
В фармацевтической продукции ферментные препараты занимают большую часть ассортимента. При инфекционных заболеваниях используются препараты, разрушающие оболочку болезнетворных бактерий. Широко известны препараты, применяемые при нарушениях функций желудочно-кишечного тракта, ферменты для рассасывания гнойных скоплений и тромбов, например, стрептокиназа.
Кинетика ферментативных реакций.
Скорость ферментативной (энзимной) реакции Vферм зависит от концентрации фермента СE и концентрации ресубстрата CS. Наблюдается прямо пропорциональная зависимость Vферм от от начальной концентрации С0,Е (первый порядок по ферменту). Зависимость Vферм от концентрации субстрата имеет нелинейный вид (рис.1), однако, при низких концентрациях субстрата порядок по субстрату первый, а при высоких – нулевой.
Зависимость скорости ферментативной реакции от концентрации субстрата
Определение константы Михаэлиса — Ментана графическим методом
Простейшая схема ферментативного катализа /1/ включает обратимое образование фермент-субстратного комплекса (ES), который необратимо превращается в продукт (Р)

Константа равновесия первой стадии выражена через константы скорости прямо (k1) и обратной реакции (k-1), а константа скорости второй стадии k2
Ферментативный катализ в биологических системах
Зачастую говоря о витаминах, минералах и других полезных для человеческого организма элементах упоминаются вещества, которые называются ферментами. Что такое ферментативный катализ и как он происходит в организме человека вы узнаете, дочитав эту статью до конца.
Строение атома и химические связи
Вспомним некоторые сведения о строении атомов и природе химических связей, удерживающих атомы в молекуле. Основу строения атома составляют центральное положительно заряженное ядро и вращающиеся вокруг него по орбитам отрицательно заряженные электроны. Самый простой атом (водорода) имеет один электрон, самый тяжелый из встречающихся в природе атомов — атом урана — 92 электрона. Способность атомов различных элементов вступать в реакцию между собой объясняется тем, что они, так сказать, «делятся» электронами своих внешних орбит: возникает пара электронов, общих для «объединяющихся» атомов — через эти общие электроны образуется химическая связь между ними.
Существуют и другие типы связей между атомами, но описанная, так называемая ковалентная связь, является наиболее прочной. Какое действие оказывают вещества, «атакующие» химические связи? Они нарушают распределение внешних электронов, увеличивая силы отталкивания или притяжения. Следствием этого является ослабление или разрыв связей. Электроны перераспределяются, и возникают новые связи.
Взаимодействие молекул
Чтобы молекулы вступили во взаимодействие и перераспределились внешние электроны составляющих их атомов, разорвались одни связи и замкнулись другие, этим им необходимо находиться в достаточно активном состоянии. Известно, что повышение температуры ускоряет химические реакции. Это объясняется тем, что тепловая энергия увеличивает число молекул, находящихся в активированном состоянии. Количество энергии, которое вещества должны получить дополнительно для того, чтобы между ними пошел процесс, называется энергией активизации. Это количество энергии, достаточное для того, чтобы большинство молекул преодолело так называемый энергетический барьер. Когда взаимодействие заканчивается, ее продукты находятся на более низком энергетическом уровне, чем исходные вещества, то есть в более устойчивом состоянии.
Как работают катализаторы?
Сущность действия катализаторов состоит в том, что они понижают энергетический барьер реакции, направляют ее как бы в обход этого барьера.
Представьте себе лыжника, стоящего перед лестницей к трамплину, с которого ему предстоит прыгнуть. Чтобы начать спуск, ему необходимо предварительно затратить некоторое количество энергии, для попадания на площадку перед трамплином. И тогда ему хватит небольшого толчка, для полета.
Теперь допустим, что перед нашим лыжником имеется ровная тропинка, ведущая на спуск с трамплина в обход лестницы. Чтобы начать спуск, пройдя этой тропинкой, ему требуется гораздо меньшая затрата энергии, чем для подъема на площадку по лестнице; стоящий перед ним энергетический барьер окажется менее высоким. Но при этом величина свободной энергии спуска будет такой же, как при спуске с площадки.
Для чего нужны ферменты и что такое ферментативный катализ
Ферментативный катализ отличается от катализа неферментативного тремя важными особенностями.
Первая — это большая специфичность ферментов (катализаторов). Если катализатор-нефермент, так сказать, облегчает осуществление множества различных хим. реакций, убыстряя их, то фермент катализирует химические превращения веществ, имеющих строго специфическое строение и не оказывает воздействие на остальные субстраты (вещества, химические превращения которых катализируются определенным ферментом).
Вторая – заключается в том, что ферменты действуют при мягких условиях внешней среды. Они не требуют высоких температур, резко кислой или очень щелочной реакции среды, повышенного во много раз давления — условий, при которых невозможна жизнь.
Третья – чрезвычайно высокая молекулярная активность ферментов; 1 молекула фермента катализирует за 1 минуту превращения множество молекул субстрата. Под действием биологических катализаторов — ферментов реакции идут в десятки тысяч, подчас в миллионы раз быстрей, чем под влиянием неорганических-катализаторов.
Ферментативный катализ по эффективности более высок по сравнению с неорганическими. Это объясняется тем, что он сильней уменьшает энергию активации. Также эффективней облегчается преодоление энергетического барьера реакции, увеличивает число активированных, способных к реакции молекул, и потому ее ускоряет.
Ферментативный катализ на первое его стадии заключается в том, что фермент соединяется с субстратом и образуется фермент-субстратный комплекс.
Формирование и последующее превращения фермент-субстратного комплекса разделяют на несколько стадий:
- соединение молекул фермента и субстрата;
- преобразование первичного фермент-субстратного комплекса в один или несколько последовательных комплексов, находящихся в активированном состоянии — химические связи легче могут разорваться;
- отделение конечных продуктов реакции от фермента.
Освободившаяся молекула фермента способна вновь вступать в оборот — соединяться с новой порцией субстрата.
Непосредственное участие в каталитическом действии принимает не вся молекула фермента, а лишь часть ее, которая называется активным центром фермента. Важнейшая составная часть активного центра — его каталитически активный участок, непосредственно взаимодействующий с субстратом. Наряду с этим принято выделять в составе активного центра так называемый контактный, или якорный участок (площадку), который обеспечивает связывание фермента с субстратом. Для многих ферментов уже выяснено, какие аминокислоты входят в состав их активных центров.
Как происходит ферментативный катализ на химическом уровне
Как протекает ферментативный катализ изучен еще не до конца, в частности не совсем ясно, каким образом активируется субстрат, какой вид приобретает его молекула в том активированном, переходном состоянии, при котором облегчен разрыв и замыкание связей в молекуле. Одни из объяснений дает так называемая теория деформации субстрата.
Возьмем соединение А—В. Связь между A и В разорвана с присоединением к А—В молекулы воды. При этом вода присоединяется таким образом, что за счет освободившейся валентности к А присоединяется одна часть молекулы воды — группа ОН (гидроксильная группа), а к молекуле В — второй атом водорода, входивший в молекулу воды. Такой тип химических реакций называется реакциями гидролиза — распад молекулы с присоединением к продуктам распада остатков молекулы воды. Ферменты, катализирующие такой тип реакции, называют гидролитическими ферментами. К такому типу реакций относятся реакции расщепления белков, углеводов и жиров в органах пищеварения. Например, молекула обычного сахара состоит из двух простых сахаров: глюкозы и фруктозы, соединенных между собой.
Если связь между ними с присоединением воды разорвется, молекула сахарозы расщепится на молекулу глюкозы и молекулу фруктозы. Таким образом, под соединением А—В мы можем подразумевать сахарозу, под А — глюкозу и под В — фруктозу. Реакция гидролиза сахарозы катализируется ферментом сахаразой, который является каталитически активным белком.
При соединении субстрата (сахарозы) с ферментом он располагается в соответствующих участках молекулы последнего таким образом, что связь между частями А и В (остатками глюкозы и фруктозы) в молекуле (сахарозы) растягивается наподобие того, как растягивали тело пытаемого человека на дыбе средневековые палачи (отсюда название «теория дыбы»); связь эта становится рыхлой. В силу происходящей при этом деформации, изменения конфигурации (как принято говорить, конформации) молекулы субстрата (сахарозы), в ней перераспределяются электроны, и это приводит к изменению расположения электрических зарядов. В итоге этого связь между А и В разрывается и при этом по освободившимся связям к обломку А присоединяется ОН, а к обломку В — водород. Источником гидроксила и водорода служит молекула воды. Сахароза распалась на глюкозу и фруктозу.
Ферментативный катализ хорошо объясняется теорией «дыбы». Для других типов подобных реакций механизм активирующего влияния фермента на субстрат менее ясен.
Как происходит ферментативный катализ в организме человека
По местам освободившихся связей к молекуле субстрата или ее остатку могут присоединяться другие атомы или группа атомов — синтезируются новые соединения. Такие реакции катализируются особым классом ферментов — синтетазами. Отщепившиеся от молекулы атомы и их группы за счет действия ферментов, именуемых трансферазами, могут быть перенесены на молекулы других соединений с образованием при этом новых молекул.
За счет действия ферментов, называемых оксидоредуктазами, продукты расщепления белков, углеводов, жиров подвергаются глубокому распаду путем их окисления. В результате такого процесса углерод пищевых веществ окисляется до углекислоты, водород — до воды, азот восстанавливается до аммиака. Те продукты обмена веществ (метаболиты), которые в организме подвергаются далее тем или иным превращениям, называются промежуточными продуктами, а те что дальнейшим превращениям не подвергаются, а удаляются из организма являются конечными.
Например: крахмал пищи под действием пищеварительных ферментов подвергается гидролизу, расщепляясь при этом на большое число молекул глюкозы. Глюкоза поступает в клетки тела. В них она подвергается многочисленным превращениям, в ходе которых она преобразуется в различные необходимые организму продукты: холестерин, гормоны и многие другие. Основная же масса продуктов распада глюкозы в итоге многоэтапных превращений, на разных стадиях катализируемых различными ферментами, вступает в конце концов в окислительно-восстановительные реакции и полностью окисляются до углекислоты и воды. В ходе этого окисления глюкозы освобождается необходимая для жизнедеятельности энергия.
Вообще процессы распада пищевых веществ идут с освобождением энергии. Такие реакции называются экзэргоническими. Процессы биологического синтеза протекают с потреблением энергии и называются эндэргоническими. Наиболее эффективный способ освобождения энергии пищевых веществ — глубокий их распад путем окисления. Энергия для этих процессов используется организмом как для производства различных видов работы (сокращение мышц и др.), так и для процессов биосинтеза.
Вывод
Таким образом, превращение того или иного вещества в организме является многоступенчатым процессом, требующим для каждого этапа действия соответствующих ферментов. По современным данным, в одной клетке нашего тела содержится в среднем 100 000 молекул ферментов, при помощи которых осуществляется 1—2 тысячи различных химических реакций. Следовательно, на одну реакцию приходится 50—100 молекул ферментов. Синтез или распад того или иного продукта обеспечивается своего рода ферментной системой. Продукт предшествующей ферментативной реакции служит субстратом для действия следующего фермента этого конвейера. Многоступенчатым, «поточным» является и синтез того или иного вещества в организме.
На это мы закончим. В этой статье по подробно разобрали что такое ферментативный катализ и как он происходит. Если вам статья понравилась и стала полезной, поделитесь ей со своими знакомыми и друзьями в соц сетях.
http://pandia.ru/text/80/238/10682.php
http://mnogovoprosov.ru/fermentativnyj-kataliz/