По ионным схемам составьте молекулярные уравнения реакций: а) Fe (2+) + S (2-) → FeS↓ б) Fe(OH)3 + . → Fe (3+) + .
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,211
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Сокращенное ионное уравнение Fe2 + + S2 — = FeS↓ соответствует взаимодействию 1) Fe(OH)2 и Na2S 2) Fe(NO3)2 и K2S 3) FeSO4 и ZnS 4) Fe(OH)3 и H2S?
Химия | 5 — 9 классы
Сокращенное ионное уравнение Fe2 + + S2 — = FeS↓ соответствует взаимодействию 1) Fe(OH)2 и Na2S 2) Fe(NO3)2 и K2S 3) FeSO4 и ZnS 4) Fe(OH)3 и H2S.
Fe + 2(OH)2 — 1 + Na2 + 1S — 2равно 2NaOH + FeS.
1. 2NaOH + Fes = Na2S + Fe(OH)2↓, 2Na( + ) + 2OH( — ) + FeS = 2Na( + ) + S(2 — ) + Fe(OH)2↓, 2OH( — ) + FeS = S(2 — ) + Fe(OH)2↓, 2.
Определите степени окисления : Железа в соединениях : Fe₂O₃, (FeOH)⁺, (FeO₄)²⁻?
Определите степени окисления : Железа в соединениях : Fe₂O₃, (FeOH)⁺, (FeO₄)²⁻.
Как называются эти веществаZnHPO4FeOH(NO3)2?
Как называются эти вещества
Какое правильное название у формулы : [FeOH ]2SO 4 ?
Какое правильное название у формулы : [FeOH ]2SO 4 ?
Исходя из сокращенного ионного уравнения реакции : Zn2 + + S2 — — — — — ZnS составьте полное ионное и молекулярное уравнения реакций?
Исходя из сокращенного ионного уравнения реакции : Zn2 + + S2 — — — — — ZnS составьте полное ионное и молекулярное уравнения реакций.
Взаимодействию каких веществ соответствуют сокращенное ионное уравнение : 2H + CO3 = H2O + CO2?
Взаимодействию каких веществ соответствуют сокращенное ионное уравнение : 2H + CO3 = H2O + CO2.
В уравнении электролитической диссоциации соли K2Mg(FeOH)(SO4)3 общее число ионов составляет 1) 5 ; 2) 6 ; 3) 7 ; 4) 4?
В уравнении электролитической диссоциации соли K2Mg(FeOH)(SO4)3 общее число ионов составляет 1) 5 ; 2) 6 ; 3) 7 ; 4) 4.
Определите степень окисления атомов в соединениях : Fe2O3, (FeOH) + , (FeO4)2 -?
Определите степень окисления атомов в соединениях : Fe2O3, (FeOH) + , (FeO4)2 -.
Уравняйте уравнение реакцииFeCl3 + KOH — FeOH + KCl?
Уравняйте уравнение реакции
FeCl3 + KOH — FeOH + KCl.
Назвать соединения : Ni(OH)2 ; K2S ; HF ; SO2 ; (FeOH)2SO4?
Назвать соединения : Ni(OH)2 ; K2S ; HF ; SO2 ; (FeOH)2SO4.
Составьте ионное уравнение NaS + HNO3?
Составьте ионное уравнение NaS + HNO3.
Вы находитесь на странице вопроса Сокращенное ионное уравнение Fe2 + + S2 — = FeS↓ соответствует взаимодействию 1) Fe(OH)2 и Na2S 2) Fe(NO3)2 и K2S 3) FeSO4 и ZnS 4) Fe(OH)3 и H2S? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 — 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
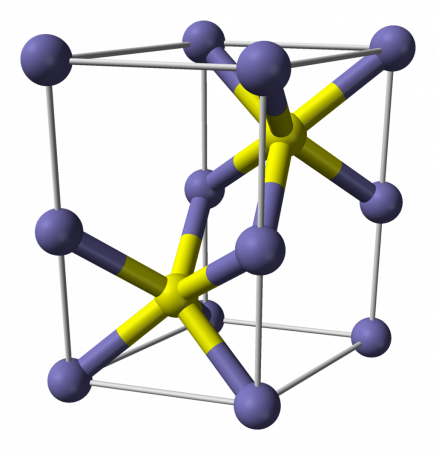
Сульфид железа (II)
| Сульфид железа (II) | |
|---|---|
 | |
| Систематическое наименование | Сульфид железа (II) |
| Хим. формула | FeS |
| Состояние | твёрдое |
| Молярная масса | 87,910 г/моль |
| Плотность | 4,84 г/см³ |
| Температура | |
| • плавления | 1194 °C |
| Рег. номер CAS | 1317-37-9 |
| PubChem | 14828 |
| Рег. номер EINECS | 215-268-6 |
| SMILES | |
| ChemSpider | 8466211 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфид железа (II) — сложное неорганическое вещество с химической формулой FeS класса неорганических сульфидов .
Содержание
- 1 Описание и структура
- 2 Получение
- 3 Химические свойства
- 4 Применение
Описание и структура
Сульфид железа (II) — бескислородная соль. Кристаллы чёрного цвета с металлическим блеском и гексагональной кристаллической решёткой, тугоплавкий, разлагается при нагревании в вакууме. Во влажном состоянии чувствителен к кислороду воздуха. Нерастворим в воде. Не выпадает в осадок при насыщении растворов солей железа (II) сероводородом. Разлагается кислотами. Применяется как сырье в производстве чугуна, твердый источник сероводорода. Не притягивается магнитом.
Получение
1. Взаимодействие железа с серой:
Реакция начинается при нагревании смеси железа с серой в пламени горелки, далее может протекать и без подогрева, с выделением теплоты.
2. Взаимодействие оксида железа (III) с водородом и сероводородом:
Химические свойства
1. Взаимодействие с концентрированной HCl:
2. Взаимодействие с концентрированной HNO3:
Применение
Сульфид железа (II) служит обычным исходным продуктом при получении сероводорода в лабораторных условиях. Гидросульфид железа [Fe(SH)2] и/или отвечающая ему основная соль [Fe(SH)OH] является важнейшей составной частью некоторых лечебных грязей.
http://himia.my-dict.ru/q/5286835_sokrasennoe-ionnoe-uravnenie-fe2-s2-fes/
http://chem.ru/sulfid-zheleza-ii.html









