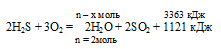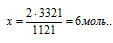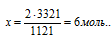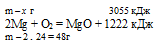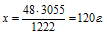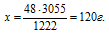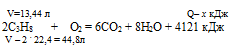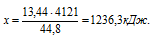Составьте термохимическое уравнение горения магния в кислороде, если при сжигании 120 г магния выделилось 3000 кДж энергии. В ответе
Ваш ответ
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,203
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Составьте термохимическое уравнение, если известно, что при сгорании 1 грамма магния выделяется 25, 6 Кдж теплоты?
Химия | 5 — 9 классы
Составьте термохимическое уравнение, если известно, что при сгорании 1 грамма магния выделяется 25, 6 Кдж теплоты.
Значение теплового эффекта горения магния (из уравнения реакции) запишите с точностью до целых (без единиц измерения) :
Термохимическое уравнение составляется на 1 моль вещества.
А у нас 1 г магний найдем сколько молей в этом одном грамме и составим пропорцию.
При сгорании 48 г магния в кислороде выделяется 980 КДЖ теплоты ?
При сгорании 48 г магния в кислороде выделяется 980 КДЖ теплоты .
Составьте термохимические уравнения.
При сжигании магния массой 3г выделяется 75, 15кДж теплоты?
При сжигании магния массой 3г выделяется 75, 15кДж теплоты.
Составьте термохимическое уравнение реакции горения магния.
При сжигании 10 г магния в кислороде выделяется 255 кдж энергии составьте термохимическое уравнение горения магния?
При сжигании 10 г магния в кислороде выделяется 255 кдж энергии составьте термохимическое уравнение горения магния.
При сжигании 1, 2 грамм магния в кислороде выделилось 30, 1 килоджоули теплоты Вычислите тепловой эффект и напишите термохимическое уравнение горения магния в кислороде?
При сжигании 1, 2 грамм магния в кислороде выделилось 30, 1 килоджоули теплоты Вычислите тепловой эффект и напишите термохимическое уравнение горения магния в кислороде.
Составьте термохимическое уравнение реакции горения углерода, если известно, что при сгорании 1, 2 углерода выделяется 40, 2 кДж теплоты ПОМОГИТЕ?
Составьте термохимическое уравнение реакции горения углерода, если известно, что при сгорании 1, 2 углерода выделяется 40, 2 кДж теплоты ПОМОГИТЕ!
Запишите термохимическое уравнение реакции горения метана, если известно, что при сгорании 5, 6 л этого газа (и?
Запишите термохимическое уравнение реакции горения метана, если известно, что при сгорании 5, 6 л этого газа (и.
У. ) выделяется 225 кДж теплоты.
Запишите термохимическое уравнение реакции горения метана если известно что при сгорании 5?
Запишите термохимическое уравнение реакции горения метана если известно что при сгорании 5.
6 литра этого газа выделяется 225 кДж теплоты.
При сжигании 6?
08 гр магния выделяется 152.
Составьте термохимическое уравнение этой реакции.
Составьте термохимическое уравнение реакции горение ацетилена , если известно , что при сгорании 1, 12 л(н?
Составьте термохимическое уравнение реакции горение ацетилена , если известно , что при сгорании 1, 12 л(н.
У) ацетилена выделяется 65, 25 кДж теплоты.
Составьте термохимическое уравнение реакции горения этилена, если известно, что тепловой эффект этой реакции 1410, 97 кДж / моль?
Составьте термохимическое уравнение реакции горения этилена, если известно, что тепловой эффект этой реакции 1410, 97 кДж / моль.
Вычислите объем сгоревшего этилена (н.
У. ), если при этом выделилось 7054, 8 кДж теплоты.
На странице вопроса Составьте термохимическое уравнение, если известно, что при сгорании 1 грамма магния выделяется 25, 6 Кдж теплоты? из категории Химия вы найдете ответ для уровня учащихся 5 — 9 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
HCl + NaOH = NaCl + H₂O по уравнению реакции m(HCl) / M(HCl) = m(NaCl) / M(NaCl) масса хлороводорода m(HCl) = M(HCl)m(NaCl) / M(NaCl) массовая доля хлороводорода в растворе w = m(HCl) / m(p) w = M(HCl)m(NaCl) / [M(NaCl) * m(p)] w = 36, 5г / моль * 11..
80кг — 100% 0. 8кг — 1% m(п) = 0. 8×80 = 64кг m(ц)80 — 64 = 16кг.
Zn(OH)₂ + 2KOH = K₂[Zn(OH)₄] тетрагидроксоцинкат калия.
У метиламина. Амины сами по себе являются слабыми основаниями (могут реагировать, например, с кислотами). Этанол — спирт. Он обладает кислотными свойствами.
2СН3СООН + Mg = (CH3COO)2Mg + Н2. Ацетат магния. 2СН3 — СН2 — СООН + CaO = (CH3 — CH2 — COO)2Ca + Н2О пропионат кальция. СН3СООН + СН3 — СН2 — ОН = СН3СООС2Н5 + Н2О этилацетат. Два первых вещества соли, последнее вещество, сложный эфир.
Так, можна. Якщо вскипьятити воду, то вона пiдiйметься вверх, а вугiльний пил осяде на низ посудини.
Железный купорос пирит.
BaCl2 Взаємодія металевого барію з хлором : Ba + Cl2 = BaCl2.
Оксиды : CaO, CO2, N2O5, Al2O3, N2O, FeO, SO3, ZnO, Mn2O7, CuO, , CO, Na2OSiO2, , NO, MnO, Cr2O3, CrO3 кислоты : H2SO3, HCl Основания : Zn(OH)2, Ca(OH)2, , KOH, F3(OH)3, Ba(OH)2, Al(OH)3, соли : CaCl2, FeCl3, Na2SO4, CaCO3.
Вычисление количества теплоты, количества и массы веществ реакций горения сероводорода, пропена и магния
Задача 1.8.
При полном сгорании сероводорода в избытке кислорода выделилось 3363 кДж теплоты. Согласно термохимическому уравнению:
2Н2S + 3О2 = 2Н2O + 2SO2 + 1121 кДж
количество вещества образовавшейся воды составляет:
1) 1 моль; 2) 2 моль; 3) 4 моль; 4) 6 моль.
Дано: Количество выделившейся теплоты: Q = 3363 кДж.
Найти: количество вещества образовавшейся воды: n(H2O) = ?
Р е ш е н и е:
I способ
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
Для вычисления количества вещества образовавшейся воды составляем пропорцию:
х моль сероводорода дают 3363 кДж (по условию)
2 моль сероводорода дают 1121 кДж (по уравнению)
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 4.
При решении данной задачи в условиях ЕГЭ можно было не составлять термохимическое уравнение. Рассмотрим этот способ.
II способ
Согласно определению теплоты образования 1121 кДж выделяется при полном сгорании 2 моль H2S, следовательно, можно составить пропорцию:
1211 кДж выделяется при сгорании 2 моль H2S
3363 кДж выделяется при сгорании х моль H2S
Подходит ответ № 4.
Ответ: n(H2O) = 6 моль.
Задача 1.9
При горении магния в кислороде выделилось 3055 кДж теплоты. Согласно термохимическому уравнению:
2Мg + О2 = МgО + 1222 кДж
масса сгоревшего магния равна:
1) 24 г; 2) 60 г; 3) 120 г; 4) 240 г.
Дано: Количество выделившейся теплоты: Q = 3055 кДж.
Найти: масса сгоревшего магния: m(Mg) = ?
Решение:
I способ
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
Для вычисления количества вещества образовавшейся воды составляем пропорцию:
х г магния дают 3055 кДж (по условию)
48г магния дают 1222 кДж (по уравнению)
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 3.
При решении данной задачи в условиях ЕГЭ можно было не составлять термохимическое уравнение. Рассмотрим этот способ.
II способ
Согласно определению теплоты образования 1222 кДж выделяется при полном сгорании 48 г Mg, следовательно, можно составить пропорцию:
1222 кДж выделяется при сгорании 48 г Mg
3055 кДж выделяется при сгорании х г Mg
Видим, что подходит ответ № 3.
Ответ: m(Mg) = 120 г.
Задача 1.10.
При сгорании 2 моль пропена выделяется 4121 кДж теплоты. При сгорании 13,44 л пропена (н.у.) выделяется:1) 2472,6 кДж; 2) 1236,ЗкДж; 3) 8242кДж; 4) 1373 кДж.
Дано: Количество выделившейся теплоты: Q = 4121 кДж.
Найти: количество теплоты Q= х кДж = ?
Решение:
I способ
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
Для вычисления количества вещества образовавшейся воды составляем пропорцию:
44,8 л пропена дают 4121 кДж (по условию)
13,44 л пропена дают х кДж (по уравнению)
Сравнивая полученный ответ с предложенными вариантами, видим, что подходит ответ № 2.
При решении данной задачи в условиях ЕГЭ можно было не составлять термохимическое уравнение. Рассмотрим этот способ.
Согласно определению теплоты образования 4121 кДж выделяется при полном сгорании 44,8 л пропена, следовательно, можно составить пропорцию:
4121 кДж выделяется при сгорании 44,8 л пропена
х кДж выделяется при сгорании 13,44 л пропена
http://himia.my-dict.ru/q/2019608_sostavte-termohimiceskoe-uravnenie-esli-izvestno-cto/
http://buzani.ru/zadachi/ege-khimiya/950-termokhimicheskie-uravneniya-zadacha-1-8-1-10