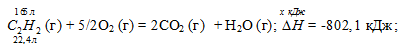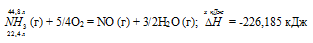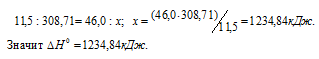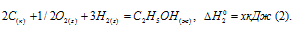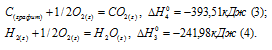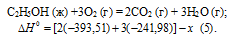Метанол: химические свойства и получение
Метанол CH3OH, метиловый спирт – это органическое вещество, предельный одноатомный спирт .
Общая формула предельных нециклических одноатомных спиртов: CnH2n+2O.
Строение метанола
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства метанола
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому метанол – жидкость с относительно высокой температурой кипения (температура кипения метанола +64,5 о С).
Водородные связи образуются не только между молекулами метанола, но и между молекулами метанола и воды. Поэтому метанол очень хорошо растворимы в воде. Молекулы метанола в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Метанол смешивается с водой в любых соотношениях.
Изомерия метанола
Для метанола не характерно наличие структурных изомеров – ни изомеров углеродного скелета, ни изомеров положения гидроксильной группы, ни межклассовых изомеров.
Химические свойства метанола
Метанол – органическое вещество, молекула которого содержит, помимо углеводородной цепи, одну группу ОН.
1. Кислотные свойства метанола
| Метанол – неэлектролит, в водном растворе не диссоциирует на ионы; кислотные свойства у него выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
Метанол с растворами щелочей практически не реагирует, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому метанол не взаимодействуют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Метанол взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
| Например, метанол взаимодействует с калием с образованием метилата калия и водорода . |
Метилаты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, метилат калия разлагается водой: |
CH3OK + H2O → CH3-OH + KOH
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии метанола с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, метанол реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии метанола с аммиаком образуется метиламин. |
2.3. Этерификация (образование сложных эфиров)
Метанол вступает в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, метанол реагирует с уксусной кислотой с образованием метилацетата (метилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, метанол взаимодействует с азотной кислотой : |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от метанола отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140 о С) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации метанола при температуре до 140 о С образуется диметиловый эфир: |
4. Окисление метанола
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| Метанол окисляется сначала в формальдегид, затем в углекислый газ: Метанол → формальдегид → углекислый газ |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол
4.1. Окисление оксидом меди (II)
Метанол можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Метанол окисляется до метаналя.
| Например, метанол окисляется оксидом меди до муравьиного альдегида |
4.2. Окисление кислородом в присутствии катализатора
Метанол можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Метанол окисляется до метаналя.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) метанол окисляется до углекислого газа.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ |
4.4. Горение метанола
При сгорании спиртов образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания метанола: |
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола образуется альдегид.
Получение метанола
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании хлорметана с водным раствором гидроксида натрия образуется метанол |
2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
Однако получить метанол гидратацией алкенов нельзя.
3. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
| Например, при гидрировании формальдегида образуется метанол |
CH2=O + H2 → CH3-OH
4. Промышленное получение метанола из «синтез-газа»
Каталитический синтез метанола из монооксида углерода и водорода при 300-400°С и давления 500 атм в присутствии смеси оксидов цинка, хрома и др.
Сырьем для синтеза метанола служит «синтез-газ» (смесь CO и H2), обогащенный водородом:
Составление термохимического уравнения реакции и вычисление теплот образования веществ
Теплота образования веществ
Задание 88.
Тепловой эффект какой реакции равен теплоте образования метана? Вычислите теплоту образования метана, исходя из следующих термохимических уравнений:
а) Н2 (г) + 1/2О2 (г) = Н2О (ж); 
б) С (к) + О2 (г) = СО2 (г); 
в) СН4 (г) + 2О2 (г) = 2Н2О (ж) + СО2 (г); 
Ответ: -74,88 кДж.
Решение:
Стандартная теплота образования равна теплоте реакции образования 1 моль этого вещества из простых веществ при стандартных условиях (Т = 298 К; р = 1,0325 . 105 Па). Образование метана из водорода и углерода можно представить так:
С (графит) + 2Н2 (г) = СН4 (г); 
Исходя из данных уравнений по условию задачи, учитывая, что водород сгорает до воды, углерод — до углекислого газа, метан – до углекислого газа и воды и, на основании закона Гесса, с термохимическими уравнениями можно оперировать также как и с алгебраическими. Для получения искомого результата нужно уравнение горения водорода (а) умножить на 2, а затем, сумму уравнений горения водорода (а) и углерода (б) вычесть из уравнения горения метана (в):
СН4 (г) + 2О2 (г) — 2 Н2 (г) + О2 (г) — С (к) + О2 (г) =
= 2Н2О (ж) + СО2 — 2Н2О — СО2;

СН4 (г) = С (к) + 2Н2 (к); 
Так как теплота образования равна теплоте разложения с обратным знаком, то

Ответ: -74,88 кДж.
Задание 89.
Тепловой эффект какой реакции равен теплоте образования гидроксида кальция? Вычислите теплоту образования гидроксида кальция, исходя из следующих термохимических уравнений:
Са (к) + 1/2О (г) = СаО (к); 
Н2 (г) + 1/2О2 (г) = Н2О (ж); 
СаО (к) + Н2О (ж) = Са(ОН)2 (к); 
Ответ: —986,50 кДж.
Решение:
Стандартная теплота образования равна теплоте реакции образования 1 моль этого вещества из простых веществ при стандартных условиях (Т = 298 К; р = 1,0325 . 105 Па). Образование гидроксида кальция из простых веществ можно представить так:
Са (к) + О2 (г) + Н2 (г) = Са(ОН)2 (к); 
Исходя из уравнений, которые даны по условию задачи и, учитывая, что водород сгорает до воды, а кальций, реагируя с кислородом, образует СаО, то на основании закона Гесса с термохимическими уравнениями можно оперировать также как с алгебраическими. Для получения искомого результата нужно все три уравнения сложить между собой:
СаО (к) + Н2О (ж) + Са (к) + 1/2О (г) + Н2 (г) + 1/2О2 (г = (ОН)2 (к) + СаО (к) + Н2О (ж); 
Так как стандартные теплоты образования простых веществ условно принята равными нулю, то теплота образования гидроксида кальция будет равна тепловому эффекту реакции образования его из простых веществ (кальция, водорода и кислорода):


Ответ: -986,50 кДж.
Задание 90.
Тепловой эффект реакции сгорания жидкого бензина с образованием паров воды и диоксида углерода равен -3135,58 кДж. Составьте термохимическое уравнение этой реакции и вычислите теплоту образования С6Н6 (ж). Ответ: +49,03 кДж.
Решение:
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном давлении Qp равные изменению энтальпии системы 

Термохимическое уравнение реакции имеет вид:
С6Н6 (ж) + 7/2O2 = 6CO2 (г) + 3Н2О (г); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:









Ответ: +49,03 кДж.
Теплота образования
Задание 91.
Вычислите, сколько теплоты выделится при сгорании 165 л (н.у.) ацетилена С2Н2, если продуктами сгорания являются диоксид углерода и пары воды? Ответ: 924,88 кДж.
Решение:
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном давлении Qp равные изменению энтальпии системы 

Уравнение реакции имеет вид:
С2Н2 (г) + 5/2O2 (г) = 2CO2 (г) + Н2О (г); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Термохимическое уравнение будет иметь вид:
Теплоту, выделившуюся при сгорании 165 л ацетилена по этой реакции, определим из пропорции:
22,4 : -802,1 = 165 : х; х = 165 (-802,1)/22,4 = -5908,35 кДж; Q = 5908,35 кДж.
Ответ: 5908,35 кДж.
Задание 92.
При сгорании газообразного аммиака образуются пары воды и оксид азота. Сколько теплоты выделится при этой реакции, если было получено 44,8 л NO в пересчете на нормальные условия? Ответ: 452,37 кДж.
Решение:
Уравнение реакции имеет вид:
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Термохимическое уравнение будет иметь вид:
Теплоту, выделившуюся при сгорании 44,8 л аммиака, вычислим из пропорции:
22,4 : -226,185 = 44,8 : х; х = 44,8 (-226,185)/22,4 = -452,37 кДж; Q = 452,37 кДж.
Ответ: 452,37 кДж
Тепловой эффект реакции
Задание 93.
Реакция горения метилового спирта выражается термохимическим уравнением:
СН3ОН (ж) +3/2О2 (г) = СО2 (г) + 2Н2О (ж); 
Вычислите тепловой эффект этой реакции, если известно, что молярная теплота парообразования СН3ОН (ж) равна +37,4 кДж. Ответ: -726,62 кДж.
Решение:
(СН3ОН (ж)) = (СН3ОН (г)); 
+37,4 кДж = -201,17 — 

Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Ответ: -726,62 кДж.
Термохимическое уравнение реакции
Задание 94.
При сгорании 11,5 г жидкого этилового спирта выделилось 308,71 кДж теплоты. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксид углерода. Вычислите теплоту образования С2Н5ОН(ж). Ответ: —277,67 кДж.
Решение:
Мольная масса С2Н5ОН равна 46,0г/моль.
Находим тепловой эффект реакции горения этилового спирта из пропорции:
Следовательно, термохимическое уравнение реакции будет иметь вид:
С2Н5ОН (ж) +3О2 (г) = 2СО2 (г) + 3Н2О (г); 
Обозначим искомую величину через х, запишем термохимическое уравнение образования С2Н5ОН из простых веществ:
Запишем также термохимические уравнения образования СО2(г) и Н2О(ж):
Из уравнений (2), (3) и (4) можно получить уравнение (5). Для этого умножим уравнение (4) на три, уравнение (2) — на два, а затем из суммы уравнений (3) и (4) вычтем уравнение (2), получим:
Сравнивая уравнения (1) и (5), находим:
Ответ: 
Расчеты по термохимическим уравнениям
Расчеты по термохимическим уравнениям
1. По термохимическому уравнению реакции СО2 + 2Н2 = СНзОН + 109 кДж вычислите количество выделившейся теплоты при образовании 6,4 г метанола.
2. По термохимическому уравнению реакции С2Н4 + Н2О = С2Н5ОН + 46 кДж вычислите объем взятого этилена (н. у.), если известно, что выделенная в этом процессе теплота составила 184 кДж.
3. Термохимическое уравнение реакции горения фосфора: 4Р + 5О2 = 2Р2О5 + 3010 кДж. Сколько теплоты выделится при сгорании 62 г фосфора?
4. По термохимическому уравнению реакции горения этилена С2Н4 + 3О2 = 2СО2 + 2Н2О + 1400 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило 5,6 л этилена (н. у.).
5. По термохимическому уравнению реакции горения ацетилена 2С2Н2 + 5О2 = 4СО2 + 2Н2О + 2610 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило: а) 1 моль ацетилена; б) 5,2 г ацетилена; в) 67,2 л ацетилена (н. у.).
6. По термохимическому уравнению реакции горения спирта С2Н5ОН + 3О2 = 2СО2 + ЗН2О + 1374 кДж вычислите, сколько выделится теплоты и какое количество вещества кислорода вступило в реакцию, если сгорело 3 моль спирта.
7. По термохимическому уравнению реакции горения метана СН4 + 2О2 = СО2 + 2Н2О + 803кДж рассчитайте, какое количество теплоты выделится при сгорании 5 м3 метана (н. у.) и какое количество вещества кислорода потребуется на это горение.
8. По термохимическому уравнению 2Н2О = 2Н2+ ОкДж рассчитайте количество теплоты, поглощенной при образовании 2,24 л водорода (н. у.).
9. Возобновление кислорода в атмосфере осуществляется реакцией фотосинтеза:
9.6СО2 + 6Н2О = С6Н12О6 + 6О2 – 2915,8 кДж. Рассчитайте количество вещества оксида углерода (IV) и количество поглощенной теплоты при образовании 7,2 кг глюкозы.
10. Одним из основных источников энергии в живом организме является окисление глюкозы:
10. С6Н12О6 + 6О2 = 6СО2 + 6Н2О + 2915,8 кДж. Рассчитайте количество теплоты, выделяющейся при окислении 3 моль глюкозы. Какой объем углекислого газа (н. у.) при этом выделится?
11. По термохимическому уравнению горения водорода 2Н2 + О2 = 2Н2О + 484 кДж
11.рассчитайте объем водорода (н. у.) и количество вещества воды, если в результате реакции выделилось 24,2 кДж теплоты.
12. Используя термохимическое уравнение реакции CuO + Н2 = Cu + Н2О + 80 кДж, рассчитайте количество теплоты, выделяющейся при восстановлении: а) 5 моль оксида меди (II); б) 1,6 г оксида меди (П).
13. В промышленности водород получают по уравнению: СН4 + 2Н2О = СО2 + 4НкДж. Каков расход воды (в г), метана (в л) и теплоты при получении 250 м3 водорода (н. у.)?
14. Используя термохимическое уравнение СаСОз = СаО + СО,650 кДж, рассчитайте количество теплоты, которое потребуется для разложения 10 кг известняка, содержащего 2% примеси.
15. Используя термохимическое уравнение N2 + О2 = 2NO — 180 кДж, рассчитайте объемы кислорода и азота (н. у.), вступивших в реакцию, если при этом поглотилось 3600 кДж энергии.
16. По термохимическому уравнению реакции 2Al + Fе2О3 = А12О3 + 2Fe + 848 кДж рассчитайте, сколько выделится теплоты при вступлении в реакцию: а) 10,8 г алюминия; б) 0,2 моль оксида железа (III).
17. По термохимическому уравнению реакции 2 Н2S + 3О2 = 2SО2 + 2Н2О + 857,3 кДж вычислите, какое количество теплоты образуется при сжигании: а) 3 моль Н2S; б) 17 г Н2S; в) 2,24 л Н2S.
18. По термохимическому уравнению реакции 2Al + 3C12 = 2АIСl3 + 1394,8 кДж вычислите, какое количество теплоты выделилось при взаимодействии с алюминием: а) 1 моль C12; б) 4,48 л C12; в) 7,1 г C12.
19. По термохимическому уравнению реакции 4Al + 3О2 = 2 А12О3 + 3350,4 кДж вычислите, какое количество теплоты выделилось при взаимодействии с алюминием: а) 1 моль О2; б) 4,48 О2; в) 3,2 г О2
20. По термохимическому уравнению реакции Si + О2= SiО2 + 850,6 кДж вычислите, какое количество теплоты может выделиться, если сжечь в кислороде: а) 5,6 кг кремния; б) 4 моль кремния.
21. Используя термохимическое уравнение горения серы S + О2= SО2 + 297 кДж, вычислите количество теплоты, образуемое при сгорании: а) 7,2 моль серы; б) 6,4 г серы.
22. По термохимическому уравнению реакции 2Na + C12 = 2NaCl + 819 кДж
22.вычислите объем (н. у.) и количество вещества хлора, вступившего в реакцию, если известно, что выделилось 81,90 кДж теплоты.
23. По термохимическому уравнению реакции Fe + S = FeS + 95,4 кДж вычислите количество теплоты, образуемое при окислении 11,2 г железа, и количество вещества сульфида железа (П), полученного при этом.
24. По термохимическому уравнению реакции 3Fe + 2О2 = Fe3О4 + 1116 кДж вычислите количество теплоты, выделившееся при сжигании 1 кг железа, содержащего 6% примеси.
25. При соединении 4,2 г железа с серой выделилось 7,15 кДж теплоты. Составьте термохимическое уравнение этой реакции.
26. При взаимодействии 1,8 г алюминия с кислородом выделилось 54,7 кДж теплоты. Вычислите теплоту образования оксида алюминия. Составьте термохимическое уравнение этой реакции.
27. При полном сжигании 42 л метана (н. у.) выделилось 1674 кДж теплоты. Составьте термохимическое уравнение реакции горения метана.
28. При гидратации 6,72 л этилена (н. у.) выделилось 13,8 кДж теплоты. Составьте термохимическое уравнение этой реакции.
29. Тепловой эффект реакции горения бутадиена равен 2310 кДж/моль. Составьте термохимическое уравнение реакции горения бутадиена и вычислите массу сгоревшего бутадиена, если при этом выделилось 924 кДж теплоты.
30. Составьте термохимическое уравнение реакции горения метилового спирта, при сжигании 0,8 г которого выделилось 18,2 кДж теплоты.
31. Составьте термохимическое уравнение реакции горения этилена, если известно, что тепловой эффект этой реакции 1410,97 кДж/моль. Вычислите объем сгоревшего этилена (н. у.), если при этом выделилось 7054,8 кДж теплоты.
32. При полном окислении 0,5 моль этана выделилось 711,5 кДж теплоты. Составьте термохимическое уравнение этой реакции.
33. При сжигании 2 моль фосфора выделяется 1504 кДж теплоты. Составьте термохимическое уравнение реакции горения фосфора.
34. При сгорании 5,6 л этилена (н. у.) выделилось 330,75 кДж теплоты. Составьте термохимическое уравнение этой реакции.
35. Составьте термохимическое уравнение окисления аммиака до свободного азота, если при окислении 4,48 л аммиака (н. у.) выделилось 76,5 кДж теплоты.
36. В результате сгорания ацетилена объемом 1,12 л (н. у.) выделилось 65,25 кДж теплоты. Составьте термохимическое уравнение реакции.
37. Составьте термохимическое уравнение реакции горения оксида углерода (11) в кислороде, если при горении 1,2 моль оксида углерода (П) выделилось 346,2 кДж теплоты.
38. Составьте термохимическое уравнение реакции, если известно; что при сгорании 6 г водорода в кислороде выделяется 858 кДж теплоты. Вычислите, какое количество вещества воды выделилось при этом.
39. Составьте термохимическое уравнение реакции, если известно, что при взаимодействии 14 г железа с серой выделилось 24,3 кДж теплоты.
40. При окислении фосфина (РНЗ) массой 14 г выделилось 486 кДж теплоты. Составьте термохимическое уравнение этой реакции.
http://buzani.ru/zadachi/khiniga-shimanovich/913-termokbimicheskie-uravnenia-teplota-obrazovanie-88-94
http://pandia.ru/text/80/049/1014.php