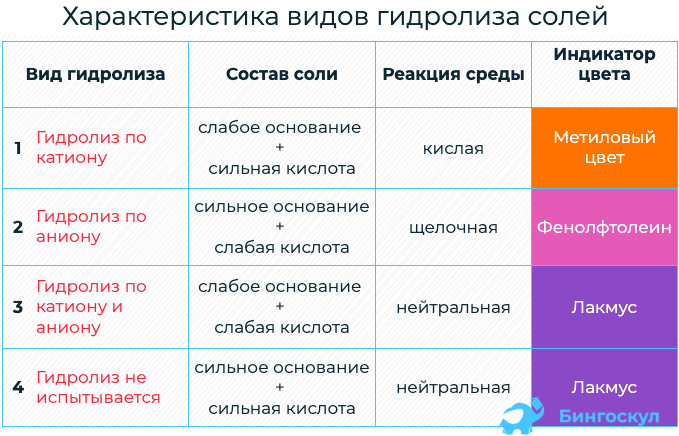
составьте уравнения гидролиза солей определите среду раствора. а) NH4Br б) K2CO3 в) MgS г) BaCl2 д) Fe(NO3)3
1) NH4Br + H2O —> NH4OH + HBr среда кислая
NH4Br —> NH4(+) + Br(-)
H2O H(+) + OH(-)
2) K2CO3 + H2O —> KHCO3 + KOH среда щелочная
K2CO3 —> KCO3(-) + K(+)
H2O H(+) + OH(-)
3) 3MgS + 2H2O —> (MgH)2S3 + Mg(OH)2 среда щелочная (не уверена в правильном составлении формулы кислой соли магния)
MgS —> Mg(2+) + S(2-)
H2O H(+) + OH(-)
4) BaCl2 + H2O —> BaOHCl + HCl среда кислая
BaCl2 —> BaCl(+) + Cl(-)
H2O H(+) + OH(-)
5) Fe(NO3)3 + H2O —> FeOH(NO3)2 + HNO3 среда кислая
Fe(NO3)3 —> Fe(NO3)2(+) + NO3(-)
H2O H(+) + OH(-)
3 и 4 абсолютно не верно! 3 — сульфид магния образован двумя слабыми частицами, плюс в таблице растворимости четкое указание на разложение в водной среде, т. е. можно предположить полный гидролиз! 4 — обе частицы сильные и гидролиз протекать не может!
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Содержание:
Гидролиз – самый распространенный химический процесс на нашей Земле, определяющий наличие жизни на нашей планете. В результате гидролиза образуются вещества, которые определяют основной химический состав жидкостей во всех живых системах: крови, плазме, тканевой жидкости. Благодаря гидролизу между мембранами клеток функционирует натрий – калиевый насос и регулируется количество основных ионов Na + и K + .
Самый известный на Земле растворитель – вода. Почти все органические и неорганические соединения готовы растворяться в водном растворе.
По химическим свойствам H2O слабый электролит, плохо разлагающийся на ионы. Для водного раствора свойственна нейтральная среда. В данной среде концентрация ионов водорода и гидроксид-ионов равны.
Растворяя всевозможные вещества в воде, возможно получить различные концентрации ионов H + и OH — . Это будет находиться в зависимости от природы вещества и степени его диссоциации.
В зависимости от этого различают слабые и сильные электролиты. К сильным электролитам относятся растворимые соли, кислоты и щелочи.
Соли в водных растворах не просто растворяются, а разлагаются на ионы. Подобный процесс получил название гидролиза.
Состав солей определяется кислотой и основанием, их степенью диссоциации и химическими свойствами. Кислоты и основания могут быть сильными и слабыми.
В зависимости от состава органические вещества относятся к разной степени гидролизуемых веществ: чем выше ионизация в молекуле, тем большему гидролизу подвергается вещество.
Сила электролита
Основание
Кислота
Растворимые основания или щелочи, например:
- гидрооксид натрия – NaOH,
- гидрооксид калия – КОН,
- гидрооксид бария – Ba(OH)2
- и т.д.
- соляная – HCl
- бромоводородная – HBr
- йодоводородная – HI
- азотная — HNO3
- серная – H2SO4
Нерастворимые основания и гидрооксид аммония NH4OH. Hапример:
- гидрооксид алюминия – Al(OH), гидрооксид калия – КОН,
- гидрооксид бария – Ba(OH)2
- и т.д.
- фтороводородная – HF
- сероводородная – H2S
- азотистая – HNO2
- сернистая – H2SO3
- угольная – H2CO3
- ортофосфорная – H3PO4
- кремниевая – H2SiO3
- уксусная – CH3COOH
В зависимости от состава соли определяется тип гидролиза, свойственный для данного вида.
Типы гидролиза солей
- Для солей, которые включают слабое основание и сильную кислоту, свойственен гидролиз по катиону.
К примеру CuCl2, — это средняя соль. Состав представлен слабым основанием Cu(OH)2 (нерастворимым в воде) и сильной кислотой HCl.
Все растворимые соли считаются сильными электролитами, вследствие этого при растворении в воде всецело диссоциируют на ионы.
Раствор представляет собой частичную диссоциацию молекулы воды и абсолютное разложение на ионы хлорида меди (II). OH — анионы объединяются с катионом Cu 2+ и образуют нерастворимое соединение, которое не диссоциирует на ионы. Ионы H + и Cl — связываются в молекулу сильного электролита – соляную кислоту. В итоге получается накопление в растворе ионов H + , которые обеспечивают, кислую реакцию среды раствора и изменение цвета индикаторов. Индикатор может быть метиловым оранжевым. В нейтральной среде имеет оранжевый цвет, в кислой окрашивается в красный.
Представляем процесс в виде уравнений реакции:
1) Cu 2+ + H2O = Cu(OH)2 ↓ + 2H + — сокращенное ионное уравнение
2) Cu 2+ + 2Cl — + 2H2O = Cu(OH)2 ↓ + 2H + + 2Cl — — полное ионное уравнение
3) CuCl2 + 2H2O = Cu(OH)2 ↓ + 2HCl— молекулярное уравнение реакции
Для солей, которые включают сильное основание и слабую кислоту, характерен гидролиз по аниону.
К примеру, Na2CO3 представляет собой соль, образованную сильным основанием NaOH (водорастворимым) и слабой кислотой H2CO3.
Когда карбонат натрия растворяется в воде, он полностью распадается на ионы, а молекулы воды отчасти диссоциируют на ионы. В итоге процесса гидролиза ионы Na + и OH — объединяются и получается сильный электролит гидроксид натрия. В растворе накапливается избыточное общее количество гидроксильных анионов OH — , которые свойственны для щелочной реакции среды. Катионы H + и анионы CO3 2- образуют слабую углекислоту, которая в растворе распадается на воду и углекислый газ.
Составляем уравнение гидролиза:
1) CO3 2- + H2O = 2OH — + H2O + CO2 ↑ — сокращенное ионное уравнение
2) 2Na + + CO3 2- + 2H2O = 2Na + + 2OH — + CO2 ↑ — полное ионное уравнение
3) Na2CO3+ 2H2O = 2NaOH + H2CO3 — молекулярное уравнение реакции
Углекислота очень слабая, в растворе распадается на H2O и CO2.
Уравнение будет выглядеть так:
Гидролиз по катиону и аниону характерен для солей, которые состоят из слабого основания и слабой кислоты.
Например, (NH4)2S представляет собой среднюю соль, образованную слабым основанием NH4OH и слабой кислотой H2S.
При растворении сульфида аммония в водном растворе происходит образование малодиссоциирующих веществ-гидроксида аммония и сероводорода. В растворе остаются лишь только молекулы воды, растворная среда станет нейтральной.
Составляем уравнение гидролиза:
1) (NH4)2S + H2O = 2NH3 ↑ + H2O +H2S↑ — молекулярное уравнение реакции
2) Полное и сокращенное ионные уравнения отсутствуют
Гидролизу не подвергается соль, состоящая из сильного основания и сильной кислоты.
Например, BaCl2 представляет собой соль, образованную сильным основанием Ba(OH)2 (водорастворимым) и сильной кислотой HCl.
Представленный тип солей не содержит кислотных остатков и катионов металлов, реагирующих с водой, т. е. способных влиять на РН водного раствора. Консистенции таких солей имеют нейтральную реакционную среду. В процессе растворения в воде образуются сильные электролиты, полностью распадающиеся на ионы.
Процессы диссоциации и гидролиза считаются обратимыми и подчиняются совокупным закономерностям смещения химического равновесия. Данные процессы возможно усиливать и замедлять, добавляя в раствор одноименный ион, разбавляя раствор или же нагревая его.
Для составления уравнений гидролиза солей существует конкретный алгоритм:
- Запишите формулу соли и определите ее растворимость в воде, применяя таблицу растворимости солей, кислот и оснований в воде.
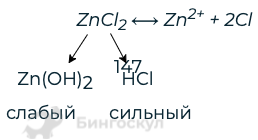
- ZnCl2 растворимый в воде
- В случае если соль растворима, составьте уравнение диссоциации
- ZnCl2⟷ Zn 2+ + 2Cl —
- Определите состав соли
- Сделайте вывод, какой из ионов соли подвергается гидролизу:
- Zn 2+ — ион, образующий слабый электролит, поэтому он подвергается гидролизу.
В данном случае гидролиз проходит по катиону.
- Zn 2+ + 2H2O = Zn(OH)2↓ +2H +
- В данном случае среда является кислой.
- Zn 2+ + 2Cl — + 2H2O = Zn(OH)2↓ +2H + + 2Cl-
- ZnCl2 + 2H2O = Zn(OH)2↓ + 2HCl
Какие из солей Fe2(SO4)3, BaCl2, CaSO4 – подвержены гидролизу, составьте ионный и молекулярные уравнения гидролиза соответствующих солей по первой ступени. Укажите реакцию их растворов.






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Какие из солей Fe 2 ( SO 4 )3, BaCl 2 , CaSO 4 – подвержены гидролизу, составьте ионный и молекулярные уравнения гидролиза соответствующих солей по первой ступени. Укажите реакцию их растворов. Как усилить гидролиз соли Fe 2 ( SO 4 )3?
Решение :
Fe 2 ( SO 4 )3 – сульфат железа, соль сильной кислоты и слабого основания, в водном растворе гидрлизуется по катиону:
2Fe 3+ + 3SO4 2- + 2H2O ↔ 2FeOH 2+ + 2SO4 2- + 2H + + SO4 2-
| Изучите химию на странице ➔ решение заданий и задач по химии. |
| Похожие готовые решения: |
- ЭДС гальванического элемента, образованного никелем, погруженным в раствор соли никеля с концентрацией ионов никеля равной 10-4 моль/л, и серебром, погруженным в раствор соли серебра, равная 1,108В.
- Чему равна сила тока, если при электролизе раствора MgCl2 в течение 45 минут на катоде выделилось 12 л водорода? Составьте схему электролиза и рассчитайте объем вещества, выделившегося на аноде
- Скорость некоторой реакции при охлаждении от 120 до 70 оС уменьшилась в 32 раза. Определите температурный коэффициент данной реакции.
- При каких изменениях температуры, давления и концентраций начальных и конечных веществ можно увеличить выход оксида азота в реакции N2 + O2 = 2NO Если известно, что ∆Н>0? Напишите уравнение константы
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
http://bingoschool.ru/manual/gidroliz-solej.-vodnyij-rastvor-sreda-kislotnaya-nejtralnaya-shhelochnaya/
http://natalibrilenova.ru/kakie-iz-solej-fe2so43-bacl2-caso4—podverzhenyi-gidrolizu-sostavte-ionnyij-i-molekulyarnyie-uravneniya-gidroliza-sootvetstvuyuschih-solej-po-pervoj-stupeni-ukazhite-reaktsiyu-ih-rastvorov-/