Гидроксид аммония: строение, свойства и применение
Гидроксид аммония: строение, свойства и применение — Наука
Содержание:
В гидроксид аммония представляет собой соединение с молекулярной формулой NH4ой ой5NO образуется при растворении газообразного аммиака (NH3) в воде. По этой причине ее называют аммиачной водой или жидким аммиаком.
Это бесцветная жидкость с очень интенсивным и резким запахом, который невозможно изолировать. Эти характеристики напрямую связаны с концентрацией NH.3 растворяется в воде; концентрация, которая на самом деле, будучи газом, может содержать огромное количество его, растворенного в небольшом объеме воды.
Достаточно небольшая часть этих водных растворов состоит из катионов NH.4 + и анионы ОН – . С другой стороны, в очень разбавленных растворах или в замороженных твердых веществах при очень низких температурах аммиак может быть найден в форме гидратов, таких как: NH3∙ H2Или, 2NH3∙ H2O и NH3∙ 2H2ИЛИ.
Любопытный факт: облака Юпитера состоят из разбавленных растворов гидроксида аммония. Однако космический зонд «Галилео» не смог найти воду в облаках планеты, чего можно было ожидать, учитывая имеющиеся у нас знания об образовании гидроксида аммония; то есть это кристаллы NH4ОН полностью безводный.
Ион аммония (NH4 + ) образуется в просвете почечных канальцев путем объединения аммиака и водорода, секретируемого клетками почечных канальцев. Аналогичным образом аммиак вырабатывается в клетках почечных канальцев в процессе превращения глутамина в глутамат и, в свою очередь, в превращении глутамата в α-кетоглутарат.
Аммиак производят в промышленных масштабах по методу Габера-Боша, при котором газы азота и водорода вступают в реакцию; с использованием иона трехвалентного железа, оксида алюминия и оксида калия в качестве катализаторов. Реакция проводится при высоком давлении (150-300 атмосфер) и высокой температуре (400-500 ºC) с выходом 10-20%.
Аммиак образуется в реакции, которая при окислении дает нитриты и нитраты. Они необходимы для получения азотной кислоты и удобрений, таких как нитрат аммония.
Химическая структура
Как указывает его определение, гидроксид аммония состоит из водного раствора газообразного аммиака. Следовательно, внутри жидкости нет никакой определенной структуры, кроме структуры случайного расположения ионов NH.4 + и ОН – сольватируется молекулами воды.
Ионы аммония и гидроксила являются продуктами равновесия гидролиза в аммиаке, поэтому эти растворы обычно имеют резкий запах:
Согласно химическому уравнению, сильное снижение концентрации воды сместило бы равновесие в сторону образования большего количества аммиака; то есть, когда гидроксид аммония нагревается, пары аммиака будут выделяться.
По этой причине ионы NH4 + и ОН – не образуют кристалл в земных условиях, что приводит к твердому основанию NH4ОН не существует.
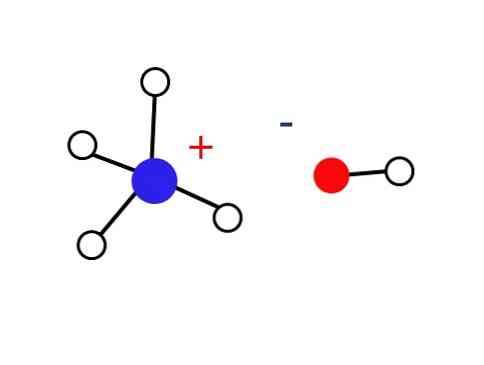
Указанное твердое вещество должно состоять только из электростатически взаимодействующих ионов (как показано на изображении).
Аммиачный лед
Однако при температурах значительно ниже 0ºC и в окружении огромных давлений, таких как те, что преобладают в ядрах замороженных лун, аммиак и вода замерзают. При этом они кристаллизуются в твердую смесь с различными стехиометрическими пропорциями, самой простой из которых является NH3∙ H2O: моногидрат аммиака.
NH3∙ H2O и NH3∙ 2H2Или это аммиачный лед, поскольку твердое вещество состоит из кристаллической структуры молекул воды и аммиака, связанных водородными связями.
При изменении T и P, согласно компьютерным исследованиям, моделирующим все физические переменные и их влияние на эти льды, происходит переход фазы NH3∙ нГн2Или к фазе NH4ОЙ.
Следовательно, только в этих экстремальных условиях NH4ОН может существовать как продукт протонирования во льду между NH3 а H2ИЛИ:
Обратите внимание, что на этот раз, в отличие от гидролиза аммиака, вовлеченные частицы находятся в твердой фазе. Аммиачный лед, который становится соленым без выделения аммиака.
Физические и химические свойства
Молекулярная формула
Молекулярный вес
вид
Это бесцветная жидкость.
Концентрация
Примерно до 30% (для ионов NH4 + и ОН – ).
Запах
Очень сильный и резкий.
Вкус
Пороговое значение
34 ppm для неспецифического обнаружения.
Точка кипения
Растворимость
Он существует только в водном растворе.
Растворимость воды
Смешивается в неограниченных пропорциях.
Плотность
0,90 г / см 3 при 25 ° С.
Плотность паров
Относительно воздуха, взятого за единицу: 0,6. То есть он менее плотный, чем воздух. Однако логически указанное значение относится к аммиаку как к газу, а не к его водным растворам или NH.4ОЙ.
Давление газа
2160 мм рт. Ст. При 25 ° C.
Коррозионное действие
Он способен растворять цинк и медь.
pH
11,6 (1 н. Раствор); 11,1 (раствор 0,1 N) и 10,6 (0,01 н. раствор).
Константа диссоциации
pKb = 4,767; Кб = 1,71 х 10 -5 при 20 ºC
pKb = 4,751; Кб = 1,774 х 10 -5 при 25 ºС.
Повышение температуры практически незаметно увеличивает основность гидроксида аммония.
Номенклатура
Какие общепринятые и официальные имена получает NH?4ОЙ? Согласно тому, что установлено IUPAC, его название — гидроксид аммония, потому что он содержит гидроксильный анион.
Аммоний, из-за его заряда +1, является одновалентным, поэтому, используя номенклатуру акций, он называется: гидроксид аммония (I).
Хотя использование термина гидроксид аммония технически некорректно, поскольку это соединение невозможно выделить (по крайней мере, не на Земле, как подробно объясняется в первом разделе).
Также гидроксид аммония называется аммиачной водой и жидким аммиаком.
Растворимость
NH4ОН не существует в виде соли в земных условиях, невозможно оценить, насколько он растворим в различных растворителях.
Однако ожидается, что он будет чрезвычайно растворим в воде, поскольку при его растворении высвобождаются огромные количества NH.3. Теоретически это был бы отличный способ хранения и транспортировки аммиака.
В других растворителях, способных принимать водородные связи, таких как спирты и амины, можно было ожидать, что он также будет в них хорошо растворим. Здесь катион NH4 + является донором водородной связи, а OH – служит обоими.
Примеры этих взаимодействий с метанолом: H3N + -H — OHCH3 и HO – — HOCH3 (УВКН3 указывает на то, что кислород получает водородную связь, а не то, что метильная группа связана с H).
Риски
-При попадании в глаза вызывает раздражение, которое может привести к повреждению глаз.
-Это въедливо. Поэтому при попадании на кожу он может вызвать раздражение, а при высоких концентрациях реагента — ожоги кожи. Повторяющийся контакт гидроксида аммония с кожей может вызвать ее сухость, зуд и покраснение (дерматит).
— Вдыхание спрея гидроксида аммония может вызвать острое раздражение дыхательных путей, характеризующееся удушьем, кашлем или одышкой. Продолжительное или повторяющееся воздействие вещества может привести к рецидивирующим инфекциям бронхов. Также вдыхание гидроксида аммония может вызвать раздражение легких.
— Воздействие высоких концентраций гидроксида аммония может потребовать неотложной медицинской помощи, поскольку может произойти скопление жидкости в легких (отек легких).
-Концентрация 25 ppm была принята как предел воздействия при 8-часовой рабочей смене в среде, где рабочий подвергается вредному воздействию гидроксида аммония.
Реактивность
-Помимо потенциального вреда для здоровья от воздействия гидроксида аммония, существуют другие меры предосторожности, которые необходимо учитывать при работе с веществом.
-Гидроксид аммония может реагировать со многими металлами, такими как: серебро, медь, свинец и цинк. Он также реагирует с солями этих металлов с образованием взрывоопасных соединений и выделением газообразного водорода; который, в свою очередь, является легковоспламеняющимся и взрывоопасным.
-Он может бурно реагировать с сильными кислотами, например: соляной кислотой, серной кислотой и азотной кислотой. Аналогичным образом он реагирует с диметилсульфатом и галогенами.
-Реагирует с сильными основаниями, такими как гидроксид натрия и гидроксид калия, с образованием газообразного аммиака. В этом можно убедиться, наблюдая равновесие в растворе, в котором добавка ионов ОН – сдвигает равновесие к образованию NH3.
-Медь и алюминий, а также другие оцинкованные металлы не должны использоваться при работе с гидроксидом аммония из-за его коррозионного воздействия на них.
Приложения
В еде
-Он используется в качестве добавки во многие пищевые продукты, в которых он действует как разрыхлитель, регулятор pH и отделочный агент для поверхности пищи.
— Список продуктов, в которых используется гидроксид аммония, обширен и включает выпечку, сыры, шоколадные конфеты, конфеты и пудинги.
-Гидроксид аммония классифицируется FDA как безвредное вещество для пищевой промышленности, если соблюдаются установленные стандарты.
-В мясных продуктах он используется в качестве противомикробного агента, способного уничтожать бактерии, такие как кишечная палочка, снижая его до неопределяемого уровня. Бактерии обнаруживаются в кишечнике крупного рогатого скота, адаптируясь к кислой среде. Регулируя pH, гидроксид аммония препятствует росту бактерий.
Терапия
-Гидроксид аммония имеет несколько терапевтических применений, в том числе:
-10% раствор применяется как стимулятор дыхательного рефлекса.
-Наружно он используется на коже для лечения укусов и укусов насекомых.-Он действует на пищеварительную систему как антацидное и ветрогонное средство, то есть помогает выводить газы.
Кроме того, он используется в качестве местного рубифицирующего средства при острой и хронической скелетно-мышечной боли. Вследствие омолаживающего действия гидроксида аммония наблюдается местное усиление кровотока, покраснение и раздражение.
Промышленное и разное
— Действует по снижению NOx (высокореактивных газов, таких как оксид азота (NO) и диоксид азота (NO2)) для выбросов аккумуляторных батарей и снижения выбросов NOx в дымовых газах.
-Используется как пластификатор; добавка для красок и для обработки поверхностей.
-Увеличивает пористость волос, позволяя пигментам краски проникать лучше, что обеспечивает лучший результат.
-Гидроксид аммония используется как противомикробное средство при очистке сточных вод. Кроме того, он участвует в синтезе хлорамина. Это вещество выполняет ту же функцию, что и хлор, при очистке воды в бассейне, но имеет то преимущество, что оно менее токсично.
-Используется как ингибитор коррозии в процессе нефтепереработки.
-Он используется в качестве чистящего средства в различных промышленных и коммерческих продуктах, используется на различных поверхностях, включая нержавеющую сталь, фарфор, стекло и духовку.
-Кроме того, он используется в производстве моющих средств, мыла, фармацевтических препаратов и чернил.
В сельском хозяйстве
Хотя гидроксид аммония не вводится непосредственно в качестве удобрения, он выполняет эту функцию. Аммиак производится из атмосферного азота по методу Габера-Боша и транспортируется охлажденным до температуры ниже точки кипения (-33 ºC) к местам его использования.
Аммиак под давлением вводится в виде пара в почву, где он немедленно вступает в реакцию с почвенной водой и переходит в форму аммония (NH4 + ), который удерживается в катионообменных центрах почвы. Кроме того, производится гидроксид аммония. Эти соединения являются источником азота.
Наряду с фосфором и калием азот составляет триаду основных питательных веществ растений, необходимых для их роста.
Структура гидроксида аммония, свойства, номенклатура, применение
гидроксид аммония представляет собой соединение NH молекулярной формулы4ОН или Н5НЕ производится растворением газообразного аммиака (NH3в воде. По этой причине он получает названия аммиачной воды или жидкого аммиака.
Это бесцветная жидкость с очень интенсивным и острым запахом, которая не изолирует. Эти характеристики имеют прямую связь с концентрацией NH3 растворяется в воде; концентрация, которая на самом деле, будучи газом, может покрывать его огромное количество, растворенное в небольшом объеме воды.
Значительно небольшая часть этих водных растворов состоит из катионов NH.4 + и ОН-анионы — . С другой стороны, в очень разбавленных растворах или в замороженных твердых веществах при очень низких температурах аммиак можно найти в форме гидратов, таких как: NH3∙ H2О, 2НХ3∙ H2O и NH3H 2H2О.
Любопытно, что облака Юпитера образованы разбавленными растворами гидроксида аммония. Однако космическому зонду Galileo не удалось обнаружить воду в облаках планеты, что можно было бы ожидать из знания того, что известно образование гидроксида аммония; то есть они кристаллы NH4ОН абсолютно безводный.
Ион аммония (NH4 + ) вырабатывается в просвете почечных канальцев путем соединения аммиака и водорода, секретируемых клетками почечных канальцев. Аналогичным образом, аммоний вырабатывается в клетках почечных канальцев в процессе превращения глютамина в глутамат и, в свою очередь, при превращении глутамата в α-кетоглутарат..
Аммиак производится промышленным способом по методу Хабера-Боша, в котором газы азота и водорода вступают в реакцию; с использованием иона трехвалентного железа, оксида алюминия и оксида калия в качестве катализаторов. Реакцию проводят при высоких давлениях (150-300 атмосфер) и высоких температурах (400-500 ºC) с выходом 10-20%..
В реакции образуется аммиак, который при окислении производит нитриты и нитраты. Они необходимы при получении азотной кислоты и удобрений, таких как аммиачная селитра.
- 1 Химическая структура
- 1.1 Аммиачный лед
- 2 Физические и химические свойства
- 2.1 Молекулярная формула
- 2.2 Молекулярный вес
- 2.3 Внешний вид
- 2.4 Концентрация
- 2.5 Запах
- 2.6 Вкус
- 2.7 Пороговое значение
- 2.8 Точка кипения
- 2.9 Растворимость
- 2.10 Растворимость в воде
- 2.11 Плотность
- 2.12 Плотность пара
- 2.13 Давление пара
- 2.14 Коррозионное действие
- 2,15 рН
- 2.16 Константа диссоциации
- 3 Номенклатура
- 4 Растворимость
- 5 рисков
- 5.1 Реакционная способность
- 6 использует
- 6.1 В еду
- 6.2 Терапия
- 6.3 Промышленное и разное
- 6.4 В сельском хозяйстве
- 7 ссылок
Химическая структура
Как указано в его определении, гидроксид аммония состоит из водного раствора газообразного аммиака. Следовательно, внутри жидкости нет определенной структуры, кроме структуры случайного расположения ионов NH.4 + и ОН — сольватированные молекулами воды.
Ионы аммония и гидроксила являются продуктами равновесного гидролиза аммиака, поэтому для этих растворов характерен резкий запах:
Согласно химическому уравнению, высокое снижение концентрации воды приведет к смещению равновесия с образованием большего количества аммиака; то есть при нагревании гидроксида аммония пары аммиака будут выделяться.
По этой причине ионы NH4 + и ОН — им не удается сформировать кристалл в земных условиях, что приводит к тому, что твердое основание NH4ОН не существует.
Это твердое вещество должно состоять только из ионов, взаимодействующих электростатически (как показано на рисунке).
Аммиачный лед
Однако при температурах значительно ниже 0ºC и в окружении огромных давлений, таких как те, что преобладают в ядрах ледяных лун, аммиак и вода замерзают. При этом они кристаллизуются в твердой смеси с различными стехиометрическими пропорциями, являясь самым простым NH3∙ H2O: моногидрат аммиака.
NH3∙ H2O и NH3H 2H2Или это аммиачный лед, потому что твердое тело состоит из кристаллического расположения молекул воды и аммиака, соединенных водородными связями.
Учитывая изменение T и P, согласно вычислительным исследованиям, которые моделируют все физические переменные и их влияние на этот лед, происходит переход фазы NH3∙ нН2Или в фазу NH4Огайо.
Поэтому только в этих экстремальных условиях NH4ОН может существовать как продукт протонирования во льду между NH3 и Н2O:
Обратите внимание, что на этот раз, в отличие от гидролиза аммиака, участвующие виды находятся в твердой фазе. Аммиачный лед, который становится соленым без выделения аммиака.
Соли аммония: получение и химические свойства
Соли аммония
Соли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка .
Способы получения солей аммония
1. Соли аммония можно получить взаимодействием аммиака с кислотами . Реакции подробно описаны выше.
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Например , хлорид аммония реагирует с нитратом серебра:
3. Средние соли аммония можно получить из кислых солей аммония . При добавлении аммиака кислая соль переходит в среднюю.
Например , гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония:
Химические свойства солей аммония
1. Все соли аммония – сильные электролиты , почти полностью диссоциируют на ионы в водных растворах:
NH4Cl ⇄ NH4 + + Cl –
2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями , если в продуктах образуется газ, осадок или образуется слабый электролит.
Например , карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ:
Соли аммония реагируют с щелочами с образованием аммиака.
Например , хлорид аммония реагирует с гидроксидом калия:
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
3. Соли аммония подвергаются гидролизу по катиону , т.к. гидроксид аммония — слабое основание:
4. При нагревании соли аммония разлагаются . При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония:
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
При температуре 250 – 300°C:
При температуре выше 300°C:
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
http://ru.thpanorama.com/articles/qumica/hidrxido-de-amonio-estructura-propiedades-nomenclatura-usos.html
http://chemege.ru/soli-ammoniya/