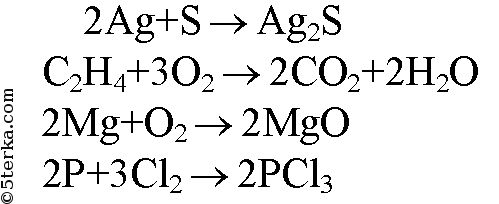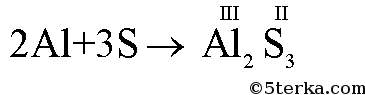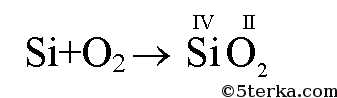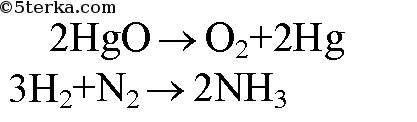Расстановка коэффициентов в уравнении онлайн
Рекомендации по пользованию сервисом
1) Для того,чтобы расставить расставить коэффициенты в уравнении химической реакции онлайн вставьте уравнение и нажмите «Уравнять»
2) Символы химических элементов следует записывать строго в том виде, в котором они фигурируют в таблице Менделеева. Т.е. первая буква в обозначении символа любого химического элемента должна быть заглавной, а вторая строчной. Например, символ химического элемента марганца следует записать как Mn, но не ни в коем случае как mn и mN;
3) Изредка возникают ситуации, когда формулы реагентов и продуктов записаны абсолютно верно, но коэффициенты все равно не расставляются. Такое может возникать в тех случаях, если коэффициенты в уравнении могут быть расставлены двумя или более способами. Наиболее вероятно возникновение такой проблемы с реакциями окисления органических веществ при которых рвется углеродный скелет. В таком случае попробуйте заменить неизменяемые фрагменты органических молекул на какой-нибудь произвольный символ, например радикал фенил C6H5 можно обозначить как Ph или X. Например, следующее уравнение:
не будет сбалансировано, так как возможна разная расстановка коэффициентов. Однако, введя обозначение C6H5 = Ph, расстановка коэффициентов происходит корректно:
Примечание
В уравнении допускается для разделения формул реагентов от формул продуктов использовать как знак равенства (=), так и стрелку (→), а также случайная запись отдельных букв символов химических элементов не латиницей, а кириллицей в случае их идентичного написания, как, например, символов C, H, O, P.
В случае, если программа оказалась полезной для Вас вы можете поделиться ссылкой на нее с друзьями в социальных сетях (кнопка внизу).
Составить уравнения следующих реакций расставить коэффициенты
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
Определите окислитель и восстановитель.
1) Составлен электронный баланс:
2) Расставлены коэффициенты в уравнении реакции:
3) Указано, что сера в степени окисления +6 является окислителем, а иод в степени окисления −1 — восстановителем.
Но кислород — тоже меняет свой заряд, можно его вместо йода выписать? Это ошибка?
Кислород остается в степени окисления -2
Почему там — 2 электрона?
потому что два йода.
Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
1) Составим электронный баланс:
2) Определены коэффициенты, и составлено уравнение реакции:
3) Указаны окислитель и восстановитель:
окислитель — восстановитель —
Тема I. Работа 4. Химические уравнения. Вариант 3
Вопросы:
1. Расставьте коэффициенты в схемах реакций. а) Ag + S → Ag2S в) Mg + O2 → MgO б) С2H4 + O2 → СO2 + H2O г) Р + С12 → РС13
2. Составьте формулы веществ, образующихся в результате реакций, и расставьте в схемах реакций коэффициенты.
а) Al + S II → AlS б) Si + O2 → SiO
3. Перепишите приведенные схемы реакций, вместо знаков вопроса напишите формулы соответствующих веществ и расставьте коэффициенты. а) HgO → O2 + ? б) ? + N2 → NH3
Решения и ответы:

задача №3
к главе «Тема I. Первоначальные химические понятия. Работа 4. Химические уравнения».
http://chem-oge.sdamgia.ru/test?theme=20
http://5terka.com/node/11250