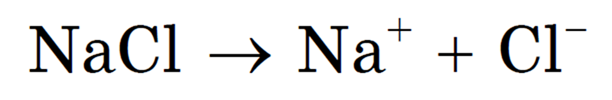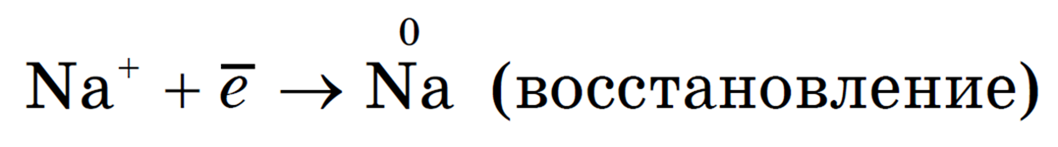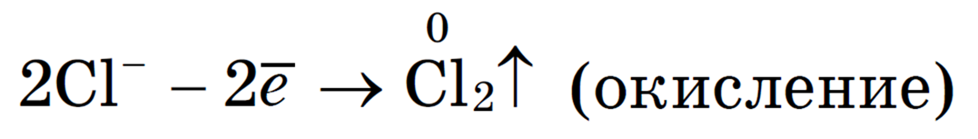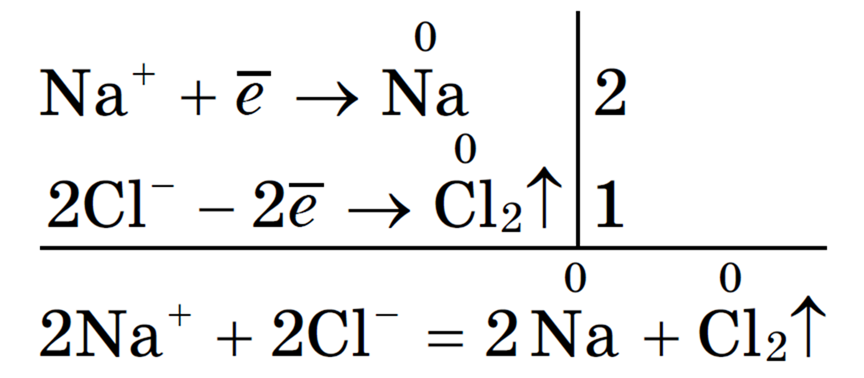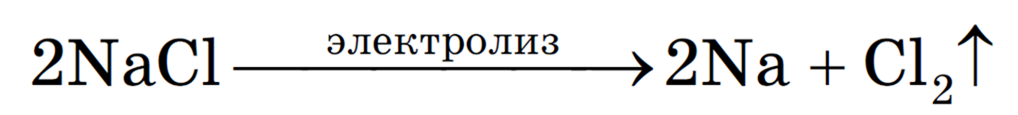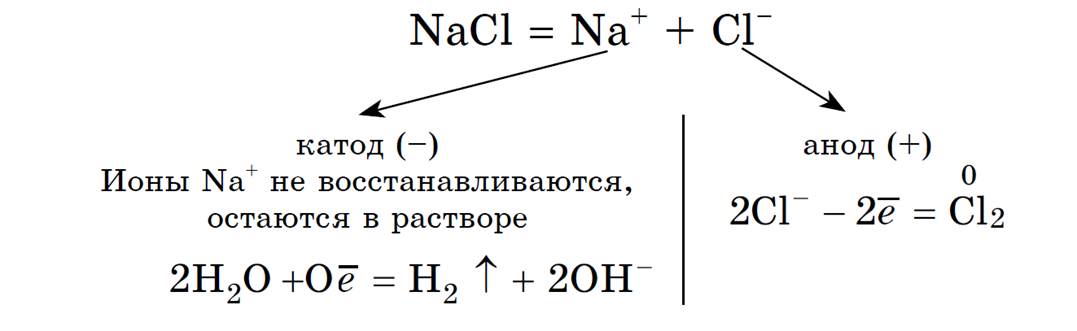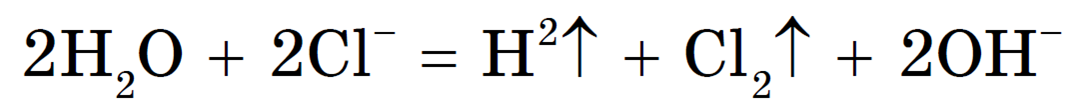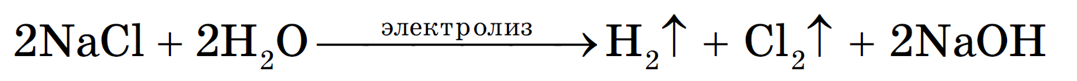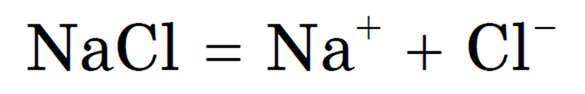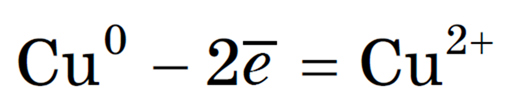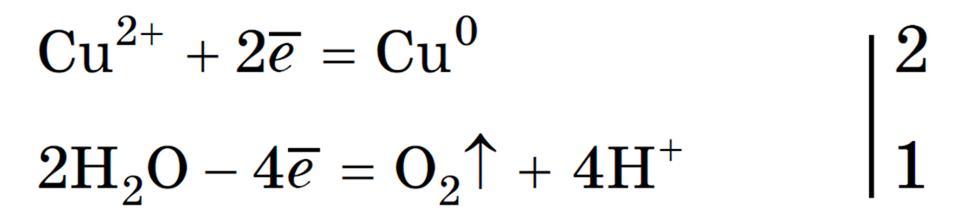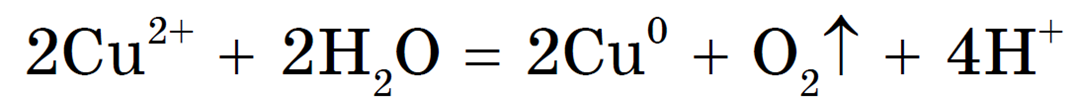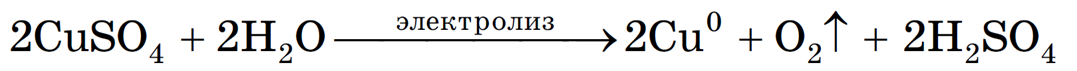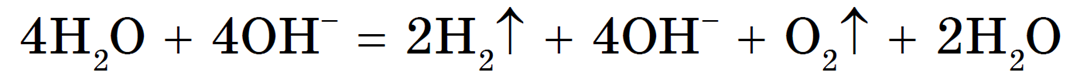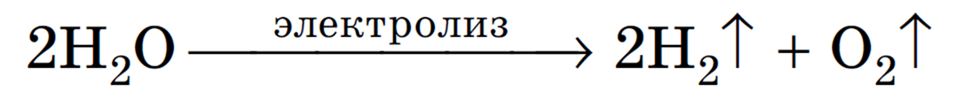Тема №34 «Электролиз расплавов и растворов»
Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита.
Электролиз расплавов и растворов
Оглавление
Электролиз расплавленных солей
Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита.
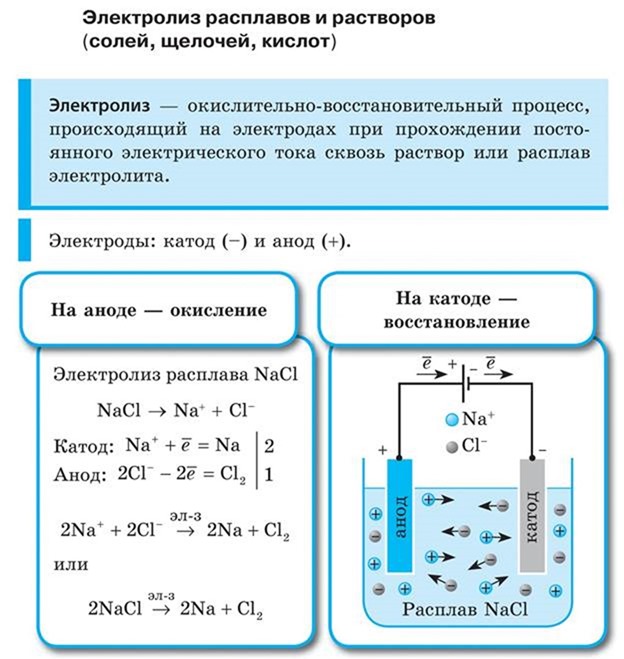
Рассмотрим процесс электролиза расплава хлорида натрия. В расплаве идет процесс термической диссоциации:
Под действием электрического тока катионы Na + движутся к катоду и принимают от него электроны:
Анионы Cl — движутся к аноду и отдают электроны:
Суммарное уравнение процессов:
На катоде образуется металлический натрий, на аноде — газообразный хлор.
Главное, что вы должны помнить: в процессе электролиза за счет электрической энергии осуществляется химическая реакция, которая самопроизвольно идти не может.
Электролитические диссоциация и ассоциация
Более сложный случай — электролиз растворов электролитов. В растворе соли кроме ионов металла и кислотного остатка присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие в электролизе.
Для определения продуктов электролиза водных растворов электролитов существуют следующие правила.
1. Процесс на катоде зависит не от материала катода, из которого он сделан, а от положения металла (катиона электролита) в электрохимическом ряду напряжений, при этом, если:
1) катион электролита расположен в ряду напряжений в начале ряда по Al включительно, то на катоде идет процесс восстановления воды (выделяется водород H2↑). Катионы металла не восстанавливаются, они остаются в растворе;
2) катион электролита находится в ряду напряжений между алюминием и водородом, то на катоде восстанавливаются одновременно и ионы металла, и молекулы воды;
3) катион электролита находится в ряду напряжений после водорода, то на катоде восстанавливаются катионы металла;
4) в растворе содержатся катионы разных металлов, то сначала восстанавливается катион металла, стоящий в ряду напряжений правее.
2. Процесс на аноде зависит от материала анода и от природы аниона:
1) если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются в процессе электролиза), то окисляется металл анода, несмотря на природу аниона;
2) если анод не растворяется (его называют инертным — графит, золото, платина), то:
• при электролизе растворов солей бескислородных кислот (кроме фторидов) на аноде идет процесс окисления аниона;
• при электролизе растворов солей кислородсодержащих кислот и фторидов на аноде идет процесс окисления воды (выделяется 02↑). Анионы не окисляются, они остаются в растворе;
• анионы по их способности окисляться располагаются в следующем порядке:
Попробуем применить эти правила в конкретных ситуациях.
Рассмотрим электролиз раствора хлорида натрия в случае, если анод нерастворимый и если анод растворимый.
1. Анод нерастворимый (например, графитовый).
В растворе идет процесс электролитической диссоциации:
Учитывая присутствие ионов Na + в растворе, составляем молекулярное уравнение:
(гидроксид натрия образуется в катодном пространстве)
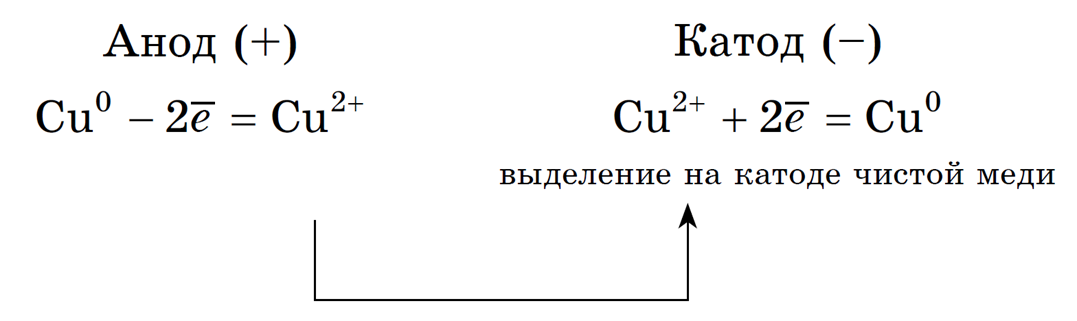
2. Анод растворимый (например, медный):
Если анод растворимый, то металл анода будет окисляться:
Катионы Cu 2+ в ряду напряжений стоят после (Н + ), поэтому они и будут восстанавливаться на катоде.
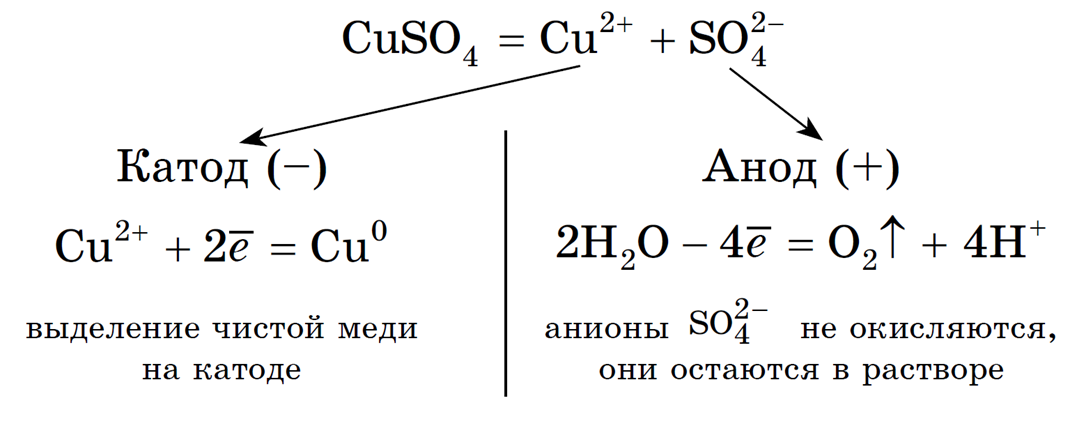
Концентрация NaCl в растворе не меняется. Рассмотрим электролиз раствора сульфата меди (II) на нерастворимом аноде:
Суммарное ионное уравнение:
Суммарное молекулярное уравнение с учетом присутствия анионов SO4 2- в растворе:
(серная кислота образуется в анодном пространстве)
Рассмотрим электролиз раствора гидроксида калия на нерастворимом аноде:
Суммарное ионное уравнение:
Суммарное молекулярное уравнение:
В данном случае, оказывается, идет только электролиз воды. Аналогичный результат получим и в случае электролиза растворов H2SO4, NaNO3, K2SO4 и др.
Электролиз расплавов и растворов веществ широко используется в промышленности.
Шпаргалка
Справочный материал для прохождения тестирования:
Составьте схему электролиза расплавов: а) гидроксида калия; б) сульфата натрия.
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,300
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,282
- разное 16,837
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Химия, Биология, подготовка к ГИА и ЕГЭ
Мы уже рассматривали электролиз растворов солей, теперь давайте разберем электролиз расплавов веществ.
В этой лекции мы рассмотрим электролиз расплавов трех видов веществ:
- электролиз расплавов оксидов;
- электролиз расплавов оснований;
- электролиз расплавов солей.
Для запоминания катодных и анодных процессов в электрохимии существует следующее мнемоническое правило:
- У анода анионыокисляются.
- На катоде катионы восстанавливаются.
В первой строке все слова начинаются с гласной буквы, во второй — с согласной.
КАТ од — КАТ ионы (ионы у кат ода)
АН од — АН ионы (ионы у ан ода)
Электролиз расплавов оксидов
На катоде идет восстановление: Me n+ + ne — = Me 0 , т.е. на катоде выделяется металл.
На аноде окисляется кислород: O -2 -2e — = O2
Возьмем для примера электролиз расплава оксида калия: 2K2O -> 4K + O2
Электролиз расплавов оснований
На катоде традиционно восстанавливается металл:
На аноде будет окисляться кислород в составе гидроксид-группы:
Электролиз расплавов солей
1. Электролиз расплава бескислородной соли:
На катоде всегда восстанавливается металл: Me n+ +ne — = Me 0
На аноде окисляется бескислородный анион: A n- — ne — = A 0
Электролиз расплава NaCl: 2NaCl = 2Na + Cl2
2. Электролиз расплава кислородсодержащей соли (элемент аниона не в высшей степени окисления):
На катоде всегда восстанавливается металл: Me n+ +ne — = Me 0
На аноде будет окисляться элемент аниона: SO3 2- — 2e — = SO3
Например, электролиз расплава сульфита натрия:
S в сульфите имеет степень окисления +4, при электролизе она окисляется до +6 — SO3
3. Электролиз расплава кислородсодержащей соли (элемент аниона в высшей степени окисления):
На катоде все без изменений 🙂
На аноде — т.к. элемент уже в высшей степени окисления, то окисляться будет кислород:
Например, электролиз расплава карбоната натрия:
Важно понимать, что эти реакции не идут сами по себе. Их протекание возможно только при действии электрического тока.
http://www.soloby.ru/787591/%D1%81%D0%BE%D1%81%D1%82%D0%B0%D0%B2%D1%8C%D1%82%D0%B5-%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D0%B7%D0%B0-%D1%80%D0%B0%D1%81%D0%BF%D0%BB%D0%B0%D0%B2%D0%BE%D0%B2-%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%BA%D1%81%D0%B8%D0%B4%D0%B0-%D1%81%D1%83%D0%BB%D1%8C%D1%84%D0%B0%D1%82%D0%B0-%D0%BD%D0%B0%D1%82%D1%80%D0%B8%D1%8F
http://distant-lessons.ru/elektroliz-rasplavov.html