Электролиз раствора сульфата натрия
Сульфат натрия в водном растворе диссоциирует
Na2SO4 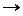
Так как натрий относится к первой группе металлов, то на катоде будет восстанавливаться водород из молекулы воды. На катоде выделяется водород, в прикатодном пространстве образуется гидроксид натрия.
На катоде (-): 4Н2О + 4е 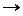
SO4 2- — анион кислородсодержащий, следовательно на аноде будет окисляться кислород из молекулы воды. На аноде выделяется кислород, в прианодном пространстве образуется серная кислота.
На аноде (+): 2Н2О – 4е 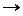
Таким образом, электролиз водного раствора сульфата натрия сводится к разложению воды на водород и кислород. В приведённых примерах используется инертный нерастворимый анод. В этом случае он выполняет единственную функцию – является передатчиком электронов.
Однако металлические аноды могут быть растворимыми. Растворимые аноды в растворах соответствующих солей под влиянием внешнего источника тока отдают свои собственные электроны и превращаются в положительно заряженные ионы, которые переходят в раствор
Кристаллическая решётка при этом разрушается. Такой процесс называется анодным растворением металла
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e32d3a3a89395fd • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Опыт 3. Электролиз сульфата натрия с нерастворимыми электродами
Модуль 2. Основные процессы химии и свойства веществ
Лабораторная работа № 7
Тема: Электролиз водных растворов солей
Электролизомназывается окислительно-восстановительный процесс, протекающий на электродах при прохождении, электрического тока через раствор или расплав электролита.
При пропускании постоянного электрического тока через раствор электролита или расплав катионы движутся к катоду, а анионы — к аноду. На электродах протекают окислительнo- восстановительные процессы;. Катод, является восстановителем, так как он отдает электроны катионам, а анод — окислителем, так как ой принимает электроны у анионов. Реакции, протекающие на электродах, зависят от состава электролита, природы растворителя, материала электродов, режима работы электролизера.
Химизм процесса электролиза расплава хлорида кальция:
на катоде Са 2+ + 2e→ Са°
на аноде 2Сl — — 2е→ 2С1° → С12
Электролиз раствора сульфата калия на нерастворимом аноде схематически выглядит так:
на катоде 2Н + + 2е→2Н°→ Н2 2
на аноде 4ОН — 4е→ О2 + 4Н + 1
K2SO4+ 4Н2О 
Цель работы:ознакомление с электролизом растворов солей.
Приборы и оборудование:выпрямитель электрического тока, электролизер, угольные электроды, наждачная бумага, стаканчики, промывалка.
Рис. 1. Прибор для проведения
3-токопроводящие проволоки; источник постоянного тока.
Реактивы и растворы:5% растворы хлорида меди СuС12, иодида калия КI, гидросульфата калия KHSO4, сульфата натрия Na2SO4, сульфата меди CuSO4, сульфата цинка ZnSO4, 20% раствор 
Опыт 1. Электролиз хлорида меди с нерастворимыми электродами
Электролизер наполните до половины объема 5% раствором хлорида меди. Опустите в оба колена электролизера по графитовому стержню, закрепите их неплотно отрезкам и каучуковой трубки. Концы электродов соедините проводниками с источниками постоянного тока. При незначительном запахе хлора электролизер немедленно отключите от источника тока. Что происходит на катоде ? Составьте уравнения электродных реакций.
Опыт 2. Электролиз иодида калия с нерастворимыми электродами
Наполните электролизер 5% раствором иодида калия, . прибавьте в каждое колено по 2 капли фенолфталеина. Вставьте вкаждое колено электролизера графитовые электроды и соедините их с источником постоянного тока.
В каком колене и почему окрасился раствор? В каждое колено добавьте по 1 капле крахмального клейстера. Где и почему выделяется иод? Составьте уравнения электродных реакций. Что образовалось в катодном пространстве?
Опыт 3. Электролиз сульфата натрия с нерастворимыми электродами
Половину объема электролизера наполните 5% раствором сульфата натрия и добавьте в каждое колено по 2 капли метилоранжа.или лакмуса. Вставьте в оба колена электроды и соедините их с источником постоянного тока. Запишите ваши наблюдения. Почему растворы электролита у разных электродов окрасились в разные цвета? Составьте уравнения электродных реакций. Какие газы и почему выделяются на электродах? В чем заключается сущность процесса электролиза водного раствора сульфата натрия
http://gomolog.ru/reshebniki/9-klass/zadachnik-kuznecova-2020/8-24.html
http://poisk-ru.ru/s4268t8.html

