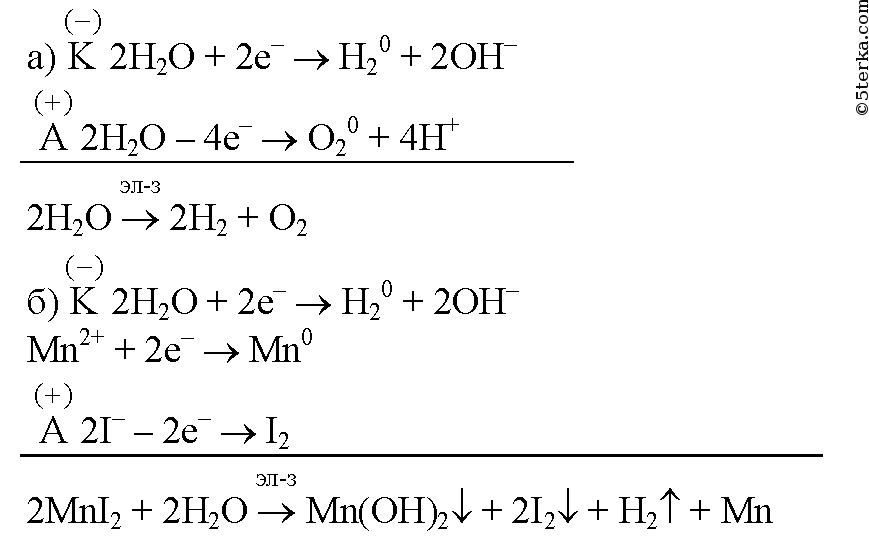24*. Составьте уравнения электролиза водных растворов солей: a) K3PO4, б) MnI2. Электроды графитовые.

задача №24
к главе «Глава 4. Вещества и их свойства. §18. Металлы».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Составьте уравнения электролиза водных растворов солей K3PO4 и MnI2?
Химия | 10 — 11 классы
Составьте уравнения электролиза водных растворов солей K3PO4 и MnI2.
1катод ( — ) 2Н2О + 2е — > ; H2 + 2OH
анод ( + ) 2H2O — 4e — > ; O2 + 4H
2катод ( — ) 2H2O + 2e — > ; H2 + 2OH
анод ( + ) 2I — 2e — > ; I2
2MnI2 + 2H2O — > ; Mn(OH)2(стрелка вниз) + 2I2(стрелка вниз) + H2(стрелка вверх) + Mn.
Составьте уравнение электролиза водного раствора карбоната калия?
Составьте уравнение электролиза водного раствора карбоната калия.
Назовите продукты электролиза : раствора MnI₂?
Назовите продукты электролиза : раствора MnI₂.
Составьте уравнения электролиза водных растворов следующих солей (электроды графитовые) :а) K3PO4б) Zn(NO3)2в) MnI2г) PtSO4д) SnPr2?
Составьте уравнения электролиза водных растворов следующих солей (электроды графитовые) :
ПОМОГИТЕ ПОЖАЛУЙСТААА))))?
Почему калий нельзя получить электролизом водных растворов солей?
Ответ поясните с помощью уравнений реакций.
Как можно получит калий с помощью электролиза ?
Уравнение электролиза раствора соли, нитрата магния?
Уравнение электролиза раствора соли, нитрата магния?
Напишите уравнения реакций, которые протекают при электролизе расплава и водного раствора хлорида кальция?
Напишите уравнения реакций, которые протекают при электролизе расплава и водного раствора хлорида кальция.
Можно ли получить металлический кальций электролизом водных растворов его солей?
При электролизе водного раствора соли на аноде выделился хлор, а в растворе образовался гидроксид бария?
При электролизе водного раствора соли на аноде выделился хлор, а в растворе образовался гидроксид бария.
Запишите формулу соли.
Составить уравнения анодного и катодного процессов при электролизе водного раствора соли NaI с инертными электродами?
Составить уравнения анодного и катодного процессов при электролизе водного раствора соли NaI с инертными электродами.
Какой процесс протекает на катоде при электролизе водного раствора смеси солей CuSO4 и NaCl?
Какой процесс протекает на катоде при электролизе водного раствора смеси солей CuSO4 и NaCl.
2. При электролизе на инертных электродах водного раствора хлорида бария не получится : а) H2 ; б) Ba ; в) Cl2 ; г) Ba(OH)2?
2. При электролизе на инертных электродах водного раствора хлорида бария не получится : а) H2 ; б) Ba ; в) Cl2 ; г) Ba(OH)2.
Составьте схему электролиза раствора этой соли.
На этой странице находится вопрос Составьте уравнения электролиза водных растворов солей K3PO4 и MnI2?. Здесь же – ответы на него, и похожие вопросы в категории Химия, которые можно найти с помощью простой в использовании поисковой системы. Уровень сложности вопроса соответствует уровню подготовки учащихся 10 — 11 классов. В комментариях, оставленных ниже, ознакомьтесь с вариантами ответов посетителей страницы. С ними можно обсудить тему вопроса в режиме on-line. Если ни один из предложенных ответов не устраивает, сформулируйте новый вопрос в поисковой строке, расположенной вверху, и нажмите кнопку.
1. а) 4 метил пропин — 2 б) 2, 3 диметил бутен — 1 в) бутин — 1 г) 1, 4 дихлор бутен — 2 д) тетраметилметан е) 1, 2, 3, 4 тетрабром бутан 2. Дано W(C) = 90% = 0. 9 D(N2) = 1. 25 — — — — — — — — — — — — — — — — — — — — — — — — — M(CxHy) — ? M(CxHy..
Это лёгкая задача : ).
А). 3 — метил пентан б). Бутен — 2 в). Гексин — 2 г). 3, 4 — диметилгептанол — 4 д). 2 — метилуксусная кислота(или 2 — метилбутановая кислота).
Формула 1 моль железа является Fe, в ней 1 атом. Вычислим число атомов на 1 моль . Число Авагадро = 6. 02•10 ^ 23 N = 1•Na = 1•6, 02•10 ^ 23 = 6, 02•10 ^ 23 Значит в 1 моль 6, 02•10 ^ 23 атомов А в 5 моль получится х Составим пропорцию Получим х =..
Для того чтобы была ионная связь разница межде электроотрицательносями дожна быть 2. 1 и более мы можем частично сказать что это ионная связь но правильней если ковалентная N берет у Li 3 электрона.
Ответ есть на фотографии.
(140 — 110) / 10 = 3 Значит берем кубический корень из 27 и получаем 3 — коэффициент Вант — Гоффа.
Na2O, MgO, Al2O3, SiO2, P2O5, SO2, Cl2O7, Na3N, Mg3N2, AlN, Si3N4, P4N5, N2S3, NCL3.
2NaOH + H2SO4 = Na2SO4 + 2H2O 80г щелочи — 142г соли 20г щелочи — х г соли х = 35. 5 г.
20 х2NaOH + H2SO4 = 2H2O + Na2SO4 80 142х = 35. 5 граммов.
Химия, Биология, подготовка к ГИА и ЕГЭ
Электролиз водных растворов солей
Тема электролиза довольна большая, формул в ней много и, как мне кажется, больше ее изучают на уроках физики… Я хочу рассмотреть ту часть, которая касается химии, и при этом только формат ЕГЭ — электролиз водных растворов солей.
Электролиз водных растворов солей
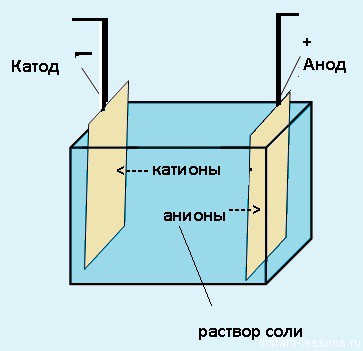
Для начала давайте представим себе систему, в которой происходит электролиз.
Электролиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, который возникает при прохождении электрического тока через раствор либо расплав электролита.
Электроды — это такие пластинки или стержни, опущенные в раствор, они подключены к источнику тока.
- Анод — положительно заряженный электрод
- Катод — отрицательно заряженный электрод
Мы будем рассматривать случай инертных электродов — т.е. они не будут вступать ни в какие химические реакции.
При пропускании электрического тока, вещество раствора будет претерпевать химические изменения, т.е. буду образовываться новые химические вещества. Они будут притягиваться к электродам следующим образом:
- Неметаллы и их производны, анионы — к аноду
- Металлы и их производный, катионы — к катоду
Теперь рассмотрим электролиз водных растворов различных солей
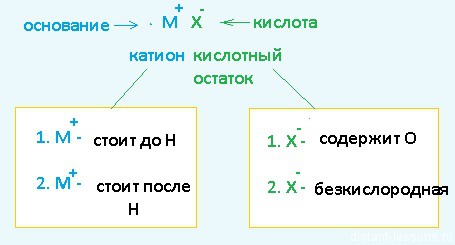
Разберем сначала катионы :
- Если металл стоит до Н, то вместо него электролизу подвергается вода:
2H2O + 2е = H2 + 2OH – Образовавшийся водород H2 идет к катоду - Если металл стоит после Н, то он сам восстанавливается:
Cu 2+ + 2е = Cu 0 Медь осаждается на катоде - Катионы металлов, стоящие в ряду напряжений после алюминия до водорода, могут восстанавливаться вместе с молекулами воды :
2Н2О + 2е = Н2+ 2ОН — Zn 2+ + 2e = Zn 0
Теперь анионы-кислотные остатки :
- Кислородсодержащие кислотные остатки — вместо них электролизу подвергается вода:
2H2O — 4e = O2 + 4H + Образовавшийся O2 выделяется на аноде - Бескислородные кислотные остатки — окисляются до простого вещества:
Cl − — 1e = Cl2 0 Хлор выделяется на аноде - Исключение: F − — вместо него будет выделяться кислород.
Примеры:
1 .1. Катион стоит в ряду до Н, кислотный остаток содержит кислород О:
1.2. Катион стоит в ряду до Н, кислотный остаток беcкислородный:
анод (+): Cl − — 1e = Cl 0 ; Cl 0 +Cl 0 =Cl2
2.1. Катион стоит в ряду после Н, кислотный остаток содержит кислород О:
K(-): Cu 2+ + 2e = Cu 0
2.2. Катион стоит в ряду после Н, кислотный остаток беcкислородный:
катод (-): Cu 2+ + 2e = Cu 0
анод (+): 2Cl − — 2e = 2Cl 0
Электролиз водных растворов солей отличается от электролиза расплавов.
Отличие — в наличии растворителя. При электролизе водных растворов солей кроме ионов самого вещества в процессе участвуют ионы растворителя. При электролизе расплавов — только ионы самого вещества.
- ЕГЭ это вопрос Части B № 3
Обсуждение: «Электролиз водных растворов солей»
Здравствуйте. Очень благодарна вам за такое понятное объяснение темы.
У меня к Вам вопрос. В одном из заданий В3, где нужно было определить продукт на катоде, я столкнулась с такой проблемой. В одной из формул веществ был написан AlCl3. Продуктом на катоде я написала водород. Но в ответ к заданию был алюминий. Скажите в чём моя ошибка или это ошибка в тесте?
Водород — правильный ответ. В ответах к тренировочным тестам ЕГЭ очень часто бывают ошибки. Да и не только в ответах. В этом году, например, в заданиях пробных ЕГЭ быди ошибки!
1. Запишите все возможные процессы на аноде, установите потенциалы процессов.
2. Сравните потенциалы анодных процессов и определите, какой из них протекает в первую очередь?
3. Выясните, меняется ли среда около анода, если да, то как и почему?
4. Запишите все возможные процессы на катоде, установите потенциалы процессов.
5. Сравните потенциалы катодных процессов и определите, какой из них протекает в первую очередь.
6. Установите, меняется ли среда около катода, если да, то как и почему?
7. Запишите итоговую схему процесса электролиза.
0,1 M раствор CuSO4
pH = 5, катод – Al, анод – Сu
здесь решают задачи школьного уровня. Не сможем вам помочь
http://himia.my-dict.ru/q/1096601_sostavte-uravnenia-elektroliza-vodnyh-rastvorov-solej/
http://distant-lessons.ru/ximiya/elektroliz