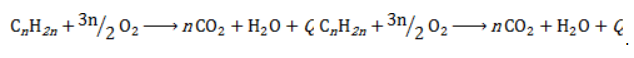Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
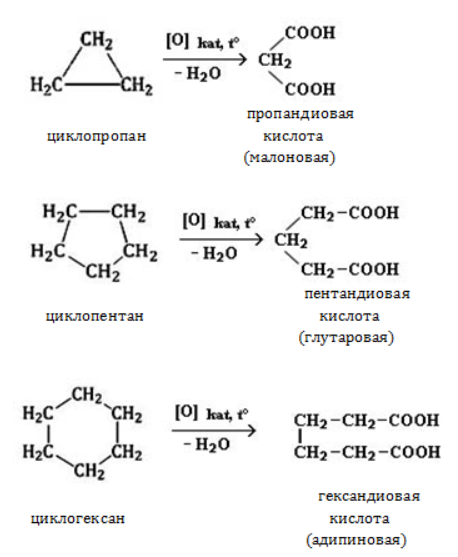
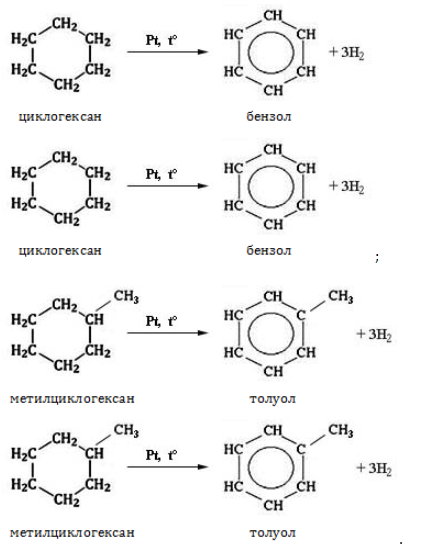
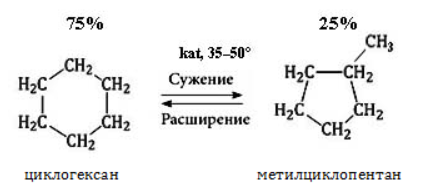
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Химические свойства циклоалкановКоличество углеродных атомов в цикле, образующем молекулу, влияет на свойства циклоалканов, проявляемые в различных видах химических взаимодействий. Соединения с малыми циклами, в которых существенную роль играет угловое напряжение, отличаются неустойчивостью и близки по свойствам к непредельным углеводородам. Чем больше звеньев в цикле, тем сильнее проявляются свойства, присущие алканам. Реакции присоединенияУчастие в процессах этого типа, связанных с разрывом замкнутого участка молекулы, свойственно циклопропану ГидрированиеУсловиями реакции являются нагревание и присутствие катализатора. Цикл размыкается с образованием алкана: Для вступления в реакцию циклопентана требуются более жесткие условия: Это единственная реакция присоединения, в которую способен вступать циклопентан. Сходство химических свойств циклоалканов с более высоким углеродным числом обусловливает их неучастие в реакциях присоединения. ГалогенированиеПродуктом этой реакции становится дигалогеналкан: ГидрогалогенированиеЦиклопропан реагирует в водном растворе с галогенводородами: Присоединять галогенводород способны и гомологи циклопропана с углеводородным радикалом и трехчленным циклом. В процессах гидрогалогенирования циклоалканов соблюдается правило Марковникова, согласно которому водород присоединяется к максимально гидрогенизированному атому углерода: Реакции замещенияДля циклоалканов со слабо напряженным или ненапряженным циклом ( ГалогенированиеВ результате реакции образуется галогенциклоалкан: Хлорирование малого цикла также может происходить без его разрыва, если температура реакции не превысит 100° C: НитрованиеАзотная кислота должна быть разбавленной. Продукт взаимодействия – нитроциклоалкан: Окисление циклоалкановРеакции окисления одинаково свойственны всем циклоалканам. Аналогично предельным незамкнутым углеводородам, они не реагируют с водным раствором Мягкое окислениеПри мягком окислении воздухом на хлориде кобальта получают алициклические кислородсодержащие соединения (кетон и спирт): Жесткое окислениеС использованием катализатора воздействие сильного окислителя (например, разбавленной азотной кислоты) на циклоалкан приводит к образованию двухосновных кислот. Реакция протекает в жестких условиях: Полное окисление (горение)В общем виде уравнение горения циклоалканов записывается: Инициирует реакцию контакт с открытым пламенем. Реакция отщепленияНагревание в присутствии металлического катализатора приводит к дегидрированию циклоалканов – отщеплению водорода и образованию ароматического соединения бензольного ряда: ИзомеризацияЦиклоалканы способны изомеризоваться с перегруппировкой атомов в углеродном скелете. Процесс протекает на платине, хлориде или бромиде алюминия и сопровождается сужением либо расширением цикла. Образование средних циклов происходит легче, и они отличаются большей устойчивостью: Реакция идет в обоих направлениях до установления равновесия. Для низших циклоалканов предпочтительной оказывается изомеризация с расширением цикла, так как она ведет к ослаблению углового напряжения в молекуле. Так, метилциклобутан переходит в циклопентан необратимо: ЗаключениеЦиклоалканы, находящиеся в начале гомологического ряда, сочетают в своих химических взаимодействиях свойства предельных и непредельных углеводородов линейного строения. Комбинация свойств вызвана, с одной стороны, особыми условиями образования непрочных изогнутых связей в простейших циклах, и, с другой стороны, насыщенностью соединений. Высшие циклоалканы практически не отличаются по химическим свойствам от алканов, так как их макроциклы не оказывают деформирующего влияния на строение химических связей. Какой продукт образуется при гидрировании циклобутана?Химия | 5 — 9 классы Какой продукт образуется при гидрировании циклобутана? Рассчитывайте массу этого продукта, если для реакции взяли 6, 72 г циклобутана. И, если не составит труда, обьясните неучу по химии ход решения этой задачи Заранее спасибо за ответ ( : C4H8 + H2 = C4H10(продукт бутан) n(C4H8) / n(C4H10) = 1 / следовательноn(C4H10) = 0. Осуществить превращение и назвать продукты реакции : Ch4→c2h2→c2h2→с2h5oh заранее спасибо?Осуществить превращение и назвать продукты реакции : Ch4→c2h2→c2h2→с2h5oh заранее спасибо. ПОЖАЛУЙСТА?Продуктом реакции гидрирования этена является : бутан, пропан, метан, этан? Срочно?Какую массу продукта реакции можно получить в результате гидрирования бензола массой 78 грамм водородом объемом 44, 8 л, если выход того вещества составляет 90%? Помогите пожалуйста?Рассчитайте массу продукта реакции, образовавшегося при горении 1, 5 моль фосфора в кислороде! С ОБЬЯСНЕНИЕМ ПОЖАЛУСЙТА! Задача по химии?Задача по химии. Какой объём азота (2) можно получить из 140 г. Азота, если известно, что выход продукта реакции составляет 85%. Какие продукты образуются при реакции железа с разбавленной соляной кислотой?Какие продукты образуются при реакции железа с разбавленной соляной кислотой? 2 уравнения реакции взаимодействия кислорода с металлами?2 уравнения реакции взаимодействия кислорода с металлами. Какой продукт образуется в ходе реакции? Найдите массу продукта, реакция которой образуется при реакции 10г калия с кислородом?Найдите массу продукта, реакция которой образуется при реакции 10г калия с кислородом. Всем привет?Решить задачу по химии : Какая масса сульфата бария образуется из 200 г гидроксида бария в реакции с серой кислотой. СРОЧНО, ДАЮ 28 БАЛЛОВпри гидрировании 55гр бутаналя выход продукта реакции составил 95%?СРОЧНО, ДАЮ 28 БАЛЛОВ при гидрировании 55гр бутаналя выход продукта реакции составил 95%. Какова масса полученного продукта реакции. На этой странице сайта вы найдете ответы на вопрос Какой продукт образуется при гидрировании циклобутана?, относящийся к категории Химия. Сложность вопроса соответствует базовым знаниям учеников 5 — 9 классов. Для получения дополнительной информации найдите другие вопросы, относящимися к данной тематике, с помощью поисковой системы. Или сформулируйте новый вопрос: нажмите кнопку вверху страницы, и задайте нужный запрос с помощью ключевых слов, отвечающих вашим критериям. Общайтесь с посетителями страницы, обсуждайте тему. Возможно, их ответы помогут найти нужную информацию. Физические : превращение воды в лёд — важно, например, для обитателей водоемов, превращение в пар — круговорот воды в природе. Плавление металлов — изготовление посуды, ювелирных изделий, в конце концов оловянных солдатиков. Химические : гашение из.. 2NaNO3 + CuSO4 — Cu(NO3)2 + Na2SO4 (но на практике эта реакция неосуществима, так как не будет осадка) 2NaNO3 + CuCl2 — реакция невозможна. Ню = м / М = 108, 5 / 217(эт М) = 0, 5ню = v / vm, следовательно V = ню * вм = 0, 5 * 22, 4 = 11, 2. Оксиген, азот и натрий ковалентный неполярный, все остальные полярные. Ионная ионная металлическая ковалентная полярная ковалентная полярная ковалентная не полярная ковалентная не полярная. 1) 2Al + 6HCl — > 2AlCl3 + 3H2 / AlCl3 — соль 2) 2Li + 2HOH — > 2LiOH + H2 / LiOH — основание 2LiOH — > Li2O + H2O / Li2O — оксид ме (гидроксид лития особенный и способен к раздражению). Я невпевнений але Ba(oh)2 + H2So4 = baso4 + h2o. X1 = C2H2 X2 = C2Na2 X3 = CH3COOH. Реакции есть на фотографии. M(CO) = 50 * 56 / 100 = 28г M(CO) = 28г / моль nCO) = 28 / 28 = 1моль CuO + CO = Cu + CO2 nCuO : nCO = 1 : 1 n(CuO) = 1моль количество вещества оксида меди равно = 1моль. источники: http://allinchemistry.ru/organicheskaya-himiya/himicheskie-svojstva-tsikloalkanov http://himia.my-dict.ru/q/6440188_kakoj-produkt-obrazuetsa-pri-gidrirovanii-ciklobutana/ |

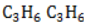 и циклобутану
и циклобутану 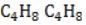 , обладающим малыми циклами.
, обладающим малыми циклами.
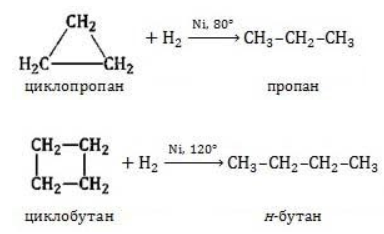
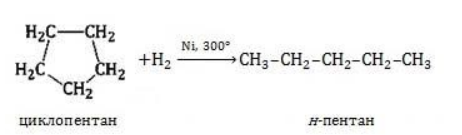

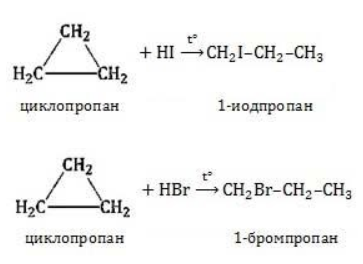

 ) характерно замещение водорода без разрушения цикла.
) характерно замещение водорода без разрушения цикла.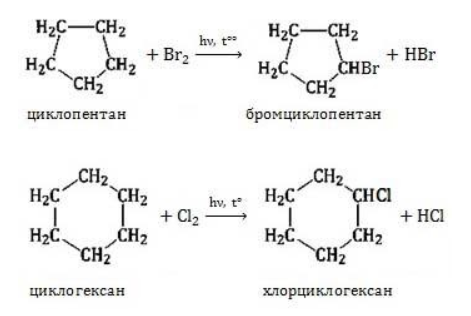
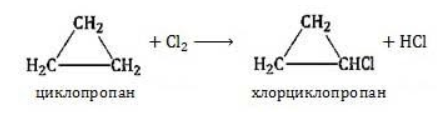
 , но подвергаются каталитическому окислению и горят, как все углеводороды.
, но подвергаются каталитическому окислению и горят, как все углеводороды.