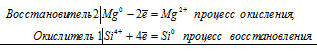1. Закончите уравнения возможных химических реакций, расставьте коэффициенты, составьте уравнения:
гидроксид калия + оксид серы (VI) = ?
оксид цинка + соляная кислота = ?
оксид фосфора (V) + оксид натрия = ?
оксид кремния (IV) + вода = ?
оксид углерода (IV) + оксид серы (VI) = ?
оксид азота (V) + гидроксид натрия = ?
серная кислота + оксид бария = ?
гидроксид лития + оксид серы (IV) = ?
2. Запишите определения для следующих понятий: основные оксиды,
Из списка оксидов выпишите только основные и укажите соответствующие им формулы оснований: Na2O; SO2; N2O3; CaO; MgО; CO2; CuО; SiO2; P2O5; FeO.
Степень окисления кремния. Применение кремниевых соединений
Решение задач на составление уравнений окислительно-восстановительных реакций кремниевых соединений
Задание 387
Какую степень окисления может проявлять кремний в своих соединениях? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
МgSi → SiH4 → SiO2 → K2SiO3 → Н2SiO3
При каком превращении происходит окислительно-восстановительная реакция?
Решение:
Для кремния в своих соединениях характерна степень окисления +4.
Уравнения реакций следующих превращений:
б) Окислительно-восстановительной реакцией является реакция силана с водой.
Здесь кремний увеличивает свою степень окисления от -4 до +4, т. е. проявляет свойство восстановителя, а водород уменьшает свою степень окисления от +1 до 0, т. е. Проявляет свойство окислителя;
Задание 388
Какое применение находит кремний? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений: SiO2 → Si → K2SiO3 → Н2SiO3
Окислительно-восстановительные реакции напишите на основании электронных уравнений.
Решение:
а) Применение кремниевых соединений
Кремний в больших количествах используется для получения динамной и трансформаторной стали, которые применяются для изготовления трансформаторов, электромоторов и генераторов. В химическом машиностроении применяют кремниевый чугун (15-17% Si), обладающий кислотоупорными свойствами. Ферросилиций служит добавкой в сталь при её выплавке, для удаления из неё кислорода (образуется SiO2, который уходит в шлак).
Особо чистый кремний применяют для изготовления полупроводниковых устройств (интегральные схемы, солнечные батареи и др.). Кварц используется для изготовления кварцевого стекла, выдерживающего нагревание до 1200 0 С и пропускающего ультрафиолетовое излучение. Изделие из кварца не растрескивается, даже если его нагреть до красного каления и, затем, опустить в холодную воду, благодаря ничтожно малому коэффициенту термического расширения.
Кристаллический кварц обладает пьезоэлектрическими свойствами. Широко используются кварцевые ультразвуковые вибраторы и эталоны частоты.
Огромное применение имеет стекло. Из него изготавливают стеклянные изделия, оконное стекло, посуду, строительные материалы, стекловолокно, стеклоткань и др. изделия.
Из кремния изготавливают ситаллы – материалы, обладающие химической стойкостью и высокой механической прочностью. Их изготавливают из металлургического шлака.
Цемент, керамика, огнеупоры, кирпичи, фаянс, фарфор, асбоцемент представляют собой материалы, содержащие оксид кремния.
Силикат натрия применяют для огнезащитного покрытия деревянных изделий, в производстве силикатных материалов. Фторокремниевую кислоту используют качестве дезинфицирующего средства.
Муллит – соединение в системе Al2O3 — SiO2, устойчивое при высоких температурах.
Цеолиты используют в качестве селективных адсорбентов при очистке и осушке газов (природный газ) и органических жидкостей (углеводороды).
SiH4 и SiCl4 используют для получения кремнийорганических соединений, из которых получают каучукоgодобные материалы, выдерживающие длительное нагревание до 250 0 С и сохраняющие эластичность даже при -60 0 С, клей, огнеупорные лаки и эмали, водоотталкивающие вещества для пропитки тканей, силиконовые смазки, протезные пластмассы, электроизоляционные материалы.
б) Уравнения реакций, которые надо провести для осуществления следующих превращений:
1) SiO2 + 2Mg = Si + 2MgO
2Mg 0 + Si 4+ = 2Mg 2+ + Si 0
SiO2 + 2Mg = Si + 2MgO
В данной реакции магний увеличивает свою степень окисления от 0 до +2, т. е. проявляет свойства восстановителя, а кремний уменьшает свою степень окисления от +4 до 0, т. е. проявляет свойства окислителя.
Si 0 + 4H + = Si 4+ + 2H2 0
В данной реакции кремний увеличивает свою степень окисления от 0 до +4, т. е. проявляет свойства восстановителя, а водород уменьшает свою степень окисления от + до 0, т. е. проявляет свойства окислителя.
В данной реакции кремний не изменяет свою степень окисления — реакция не является окислительно-восстановительной.
Составьте уравнение реакций, расставьте коэффициенты : А) азот + кислород Б)алюминий + хлор В)водород + сера Г)оксид меди + водород Пожалуйста помогите )?
Химия | 5 — 9 классы
Составьте уравнение реакций, расставьте коэффициенты : А) азот + кислород Б)алюминий + хлор В)водород + сера Г)оксид меди + водород Пожалуйста помогите ).
2)Al + 3Cl = alcl3
4)CuO + H2 = cu + h2o.
Какие неметаллы не реагируют между собой1?
Какие неметаллы не реагируют между собой
Углерод и водород.
Кислород и хлор.
Кремний и водород
Азот и кислород.
Составьте уравнения реакции, расставьте коэффициенты?
Составьте уравнения реакции, расставьте коэффициенты.
А) водород + кислород = б) углерод + водород = в) магний + фосфор = г) оксид серы (4) + кислород =.
Написать уравнения хим?
Написать уравнения хим.
Реакций и назвать : 1)водорода с азотом 2) водорода с бромом 3)серы с кислородом 4)фосфора с кислородом 5) углеродом с хлором.
Срочно?
Составьте уравнения реакций магния с : а) хлором б) серой в) соляной кислотой г) водой д) водородом е) кислородом Пожалуйста!
Записать уравнение реакции натрия и кальция с кислородом, хлором, серой , азотом, водородом и водой?
Записать уравнение реакции натрия и кальция с кислородом, хлором, серой , азотом, водородом и водой.
Рассмотреть три уравнения в свете окислительно востоновителной реакции.
Составить уравнения хим?
Составить уравнения хим.
Реакций водорода : — с кислородом и хлором (Сl2) ; — с оксидом никеля ; — с серой и азотом ; — с оксидом железа.
Если аммиак сжигать в кислороде без катализатора, то образуются азот и вода?
Если аммиак сжигать в кислороде без катализатора, то образуются азот и вода.
Составьте уравнение этой реакции и расставьте в нем коэффициенты методом электронного баланса.
Составьте уравнение окислительно — восстановительных реакций : а)алюминия и кислородом ; б)железа с хлором ; в)лития с серой?
Составьте уравнение окислительно — восстановительных реакций : а)алюминия и кислородом ; б)железа с хлором ; в)лития с серой.
Объясните пожалуйста как решить?
Объясните пожалуйста как решить.
Запишите уравнения взаимодействия простых веществ расставьте коэффициенты 1)водорода и серы, 2)магния и кислорода,
3)алюминия и кислорода,
4)алюминия и серы, 5)натрия и фосфора
Какие из элементов образуют вростые вещества, молекулы которых двухатомны : медь, водород, сера, гелий, азот, углерод, кальций, кислород?
Какие из элементов образуют вростые вещества, молекулы которых двухатомны : медь, водород, сера, гелий, азот, углерод, кальций, кислород?
А)водород, азот, сера
б) сера, гелий, углерод
в)водород, азот, кислород
г)кислород, медь, кальций.
Вопрос Составьте уравнение реакций, расставьте коэффициенты : А) азот + кислород Б)алюминий + хлор В)водород + сера Г)оксид меди + водород Пожалуйста помогите )?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 5 — 9 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
m(CaO) = 20г * 0. 13 = 2, 6г n(CaO) = = 0, 045 моль По уравнению n(CaO) = n(Ca(OH)2) = 0, 045 моль m(Ca(OH)2) = 0, 045 моль * 74г / моль = 3, 33г.
Cu + H2SO4 = не идет т. К медь стоит правее водорода, она не может вытеснить водород.
Sn + 2S (Hg / NH₄Cl / t) = SnS₂↓ сульфид олова (IV) муссивное золото m(Sn) = M(Sn)m(SnS₂) /
Проводят : вода, фольга не проводят : стекло, пластмасса, древесина, резина (наверное).
Номер 3. 2KOH + Cu(NO3)2 = 2KNO3 + Cu(OH)22K( + ) + 2OH( — ) + Cu( + 2) + 2NO3( — ) = 2K( + ) + 2NO3( — ) + Cu(OH)2Cu( + 2) + 2OH( — ) = Cu(OH)2.
Я не уверена на счёт молей , но по логике должно быть так , удачи ✋️.
А. 2Cu + O₂ = 2CuO б. 4li + O₂ = 2li₂O в. 4H + 3O₂ = 2H₂O₃.
Помогаю тобі помагаю бачиш помогаю ну як я тобі можу допомогти якшо немає завдання.
А — 6 Б — 4 В — 3 Г — 1 N — 2энерго. Уровня He — 1 энерго уровень Si — 3эн уровня Ti — 4 эн уровня Zn — 5 эн уровня.
C + 2H2 = CH4⇒CH4 + Br2 = CH3Br + HBr⇒CH3Br + CH3Br + Na = C2H6⇒C2H6 + Br2 = C2H5Br + HBr⇒C2H5Br + C2H5Br + 2Na = C4H10 + 2NaBr⇒C4H10 + O2 = 2CH3COOH 2CH4(крекинг) = С2Н2 + 3Н2 С2Н6(крекинг) = C2H4 + H2 C2H4(кркеинг) = C2H2 + H2 2C4H10 + 13O2 = 8CO2 ..
http://buzani.ru/zadachi/khimiya-shimanovich/985-kremnij-i-ego-soedineniya-zadaniya-387-388
http://himia.my-dict.ru/q/357381_sostavte-uravnenie-reakcij-rasstavte-koefficienty-a/