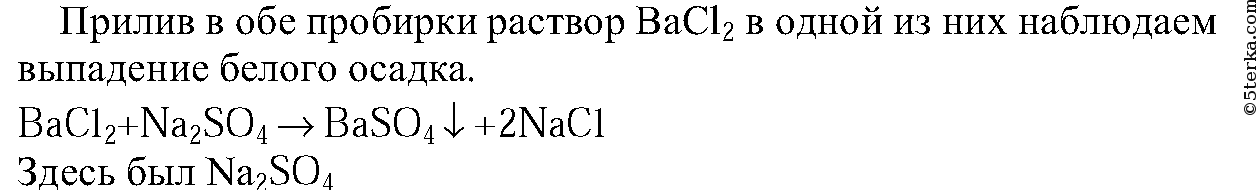Сульфид калия: способы получения и химические свойства
Сульфид калия K2S — белое вещество, плавится без разложения. Термически устойчивый. Хорошо растворяется в воде.
Относительная молекулярная масса Mr = 110,26; относительная плотность для тв. и ж. состояния d = 1,74; tпл = 912º C.
Способ получения
1. Сульфид калия можно получить путем взаимодействия калия и серы при температуре 100 — 200º C:
2K + S = K2S
2. При взаимодействии с углеродом (коксом) сульфат калия при температуре 900º C образует сульфид калия и угарный газ:
3. При температуре 600º C в присутствии оксида железа (III) сульфат калия реагирует с водородом . Взаимодействие сульфата калия с водородом приводит к образованию сульфида калия и воды:
Качественная реакция
Качественная реакция на сульфид калия — взаимодействие его с хлоридом меди, в результате реакции происходит образование черного осадка:
1. При взаимодействии с хлоридом меди , сульфид калия образует осадок сульфид меди и хлорид калия:
CuCl2 + K2S = CuS↓ + 2KCl
Химические свойства
1. Сульфид калия может реагировать с простыми веществами :
Твердый сульфид калия реагирует с кислородом при температуре выше 500º C. При этом образуется сульфат калия:
2. Сульфид калия вступает в реакцию со многими сложными веществами :
2.1. Сульфид калия способен реагировать со многими кислотами :
2.1.1. Сульфид калия реагирует с разбавленной хлороводородной кислотой . Взаимодействие сульфида калия с хлороводородной кислотой приводит к образованию хлорида калия и газа сероводорода:
K2S + 2HCl = 2KCl + H2S↑
2.1.2. Сульфид калия взаимодействует с концентрированной серной кислотой . При этом образуются гидросульфат калия, газ оксид серы, осадок сера и вода:
2.1.3. При взаимодействии сульфида калия с концентрированной азотной кислотой выделяются нитрат калия, газ оксид азота, сера и вода:
2.1.4 . Взаимодействуя с насыщенной сероводородной кислотой холодный сульфид калия образует гидросульфид калия:
Вариант 4
Вопросы:
1. Составьте уравнения реакций: а) серы с фтором (в образующемся соединении сера проявляет высшую степень окисления); б) серы с калием (укажите степени окисления атомов и расставьте коэффициенты с помощью метода электронного баланса); в) раствора серной кислоты с алюминием; г) раствора серной кислоты с оксидом меди(II); д) раствора серной кислоты с раствором гидроксида натрия (в молекулярной и ионной формах).
2. Охарактеризуйте основные области применения серной кислоты.
3. В одной пробирке находится раствор хлорида натрия, в другой — раствор сульфата натрия. Как можно распознать эти растворы? Напишите уравнения соответствующих реакций.
Ответы и решения:
2. Серная кислота используется для производства удобрений (с ее помощью получают фосфорную кислоту) и в промышленности органического синтеза.

задача №4
к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 1. Кислород. Сера. Серная кислота».
Составьте уравнение реакции серы с калием
Вопрос по химии:
Составьте уравнения и электронный баланс, определите окислитель и восстановитель в реакции серы с калием,цинком,алюминием и водородом
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 1
2K(0)+S(0)—>K(+1)2S(-2)
K(0)-1e—>K(+1) | 2 восстановитель
S(0)+2e—>S(-2) | 1 окислитель
Zn(0)+S(0)—>Zn(+2)S(-2)
Zn(0)-2e—>Zn(+2) 2 восстановитель
S(0)+2e—>S(-2) 2 окислитель
Al(0)-3e—>Al(+3) 2 восс-тель
S(0)+2e—>S(-2) 3 ок-тель
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
http://5terka.com/node/11409
http://online-otvet.ru/himia/5cea9d4c96f4e19a29531929