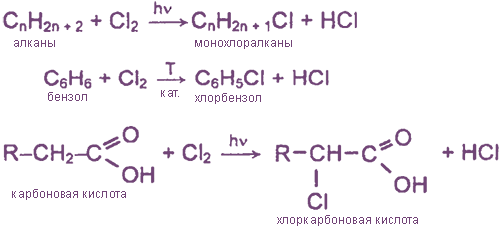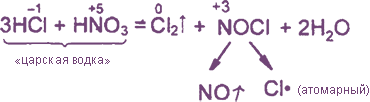Составьте уравнения реакций: а) меди с кислородом; б) железа с хлором; в) бария с водой. в уравнении реакции а укажите степени окисления
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,203
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Физические свойства
Cl2 при об. Т — газ желто-зеленого цвета с резким удушающим запахом, тяжелее воздуха — в 2,5 раза, малорастворим в воде (
6,5 г/л); х. р. в неполярных органических растворителях. В свободном виде встречается только в вулканических газах.
Способы получения
Основаны на процессе окисления анионов Cl —
2Cl — — 2e — = Cl2 0
Промышленный
Электролиз водных растворов хлоридов, чаще — NaCl:
Лабораторные
Окисление конц. HCI различными окислителями:
Химические свойства
Хлор — очень сильный окислитель. Окисляет металлы, неметаллы и сложные вещества, превращаясь при этом в очень устойчивые анионы Cl — :
Реакции с металлами
Активные металлы в атмосфере сухого газообразного хлора воспламеняются и сгорают; при этом образуются хлориды металлов.
Малоактивные металлы легче окисляются влажным хлором или его водными растворами:
Реакции с неметаллами
Хлор непосредственно не взаимодействует только с O2, N2, С. С остальными неметаллами реакции протекают при различных условиях.
Образуются галогениды неметаллов. Наиболее важной является реакция взаимодействия с водородом.
Вытеснение свободных неметаллов (Вr2, I2, N2, S) из их соединений
Диспропорционирование хлора в воде и водных растворах щелочей
В результате самоокисления-самовосстановления одни атомы хлора превращаются в анионы Cl — , а другие в положительной степени окисления входят в состав анионов ClO — или ClO3 — .
Cl2 + Н2O = HCl + НClO хлорноватистая к-та
Эти реакции имеют важное значение, поскольку приводят к получению кислородных соединений хлора:
КClO3 и Са(ClO)2 — гипохлориты; КClO3 — хлорат калия (бертолетова соль).
Взаимодействие хлора с органическими веществами
а) замещение атомов водорода в молекулах ОВ
б) присоединение молекул Cl2 по месту разрыва кратных углерод-углеродных связей
Хлороводород и соляная кислота
Газообразный хлороводород
Физические и химические свойства
HCl — хлорид водорода. При об. Т — бесцв. газ с резким запахом, достаточно легко сжижается (т. пл. -114°С, т. кип. -85°С). Безводный НСl и в газообразном, и в жидком состояниях неэлектропроводен, химически инертен по отношению к металлам, оксидам и гидроксидам металлов, а также ко многим другим веществам. Это означает, что в отсутствие воды хлороводород не проявляет кислотных свойств. Только при очень высокой Т газообразный HCl реагирует с металлами, причем даже такими малоактивными, как Сu и Аg.
Восстановительные свойства хпорид-аниона в HCl также проявляются в незначительной степени: он окисляется фтором при об. Т, а также при высокой Т (600°С) в присутствии катализаторов обратимо реагирует с кислородом:
Газообразный HCl широко используется в органическом синтезе (реакции гидрохлорирования).
Способы получения
1. Синтез из простых веществ:
2. Образуется как побочный продукт при хлорировании УВ:
R-H + Cl2 = R-Cl + HCl
3. В лаборатории получают действием конц. H2SO4 на хлориды:
H2SО4(конц.) + NaCl = 2HCl↑ + NaHSО4 (при слабом нагревании)
H2SО4(конц.) + 2NaCl = 2HCl↑ + Na2SО4 (при очень сильном нагревании)
Водный раствор HCl — сильная кислота (хлороводородная, или соляная)
HCl очень хорошо растворяется в воде: при об. Т в 1 л Н2O растворяется
450 л газа (растворение сопровождается выделением значительного количества тепла). Насыщенный раствор имеет массовую долю HCl, равную 36-37 %. Такой раствор имеет очень резкий, удушающий запах.
Молекулы HCl в воде практически полностью распадаются на ионы, т. е. водный раствор HCl является сильной кислотой.
Химические свойства соляной кислоты
1. Растворенный в воде HCl проявляет все общие свойства кислот, обусловленные присутствием ионов Н +
а) с металлами (до Н):
б) с основными и амфотерными оксидами:
в) с основаниями и амфотерными гидроксидами:
г) с солями более слабых кислот:
Реакции с сильными окислителями F2, MnO2, KMnO4, KClO3, K2Cr2O7. Анион Cl — окисляется до свободного галогена:
2Cl — — 2e — = Cl2 0
Уравнения реакция см. «Получение хлора». Особое значение имеет ОВР между соляной и азотной кислотами:
Реакции с органическими соединениями
а) с аминами (как органическими основаниями)
б) с аминокислотами (как амфотерными соедимнеиями)
Оксиды и оксокислоты хлора
Кислородсодержащие соединения хлора — чрезвычайно неустойчивые вещества, так как включают атомы Cl в нестабильных положительных с. о. Тем не менее некоторые из них имеют важное практическое значение.
Напишите уравнение реакций водорода с 1)кислородом ; 2)хлором Cl2 ; 3)оксидом железа (3)подчеркни формулу восстановителя ; 4)серой?
Химия | 5 — 9 классы
Напишите уравнение реакций водорода с 1)кислородом ; 2)хлором Cl2 ; 3)оксидом железа (3)подчеркни формулу восстановителя ; 4)серой.
Каков знак теплового эффекта этой реакции ( + Q или — Q)?
2Н2 + О2 = 2Н2ОН2 + cl2 = 2HCLH2 + 2Fe2O3 = 2FeH + 3O22H2 + S = SH4.
Напишите уравнение реакций углерода с алюминием, водородом, фтором, оксидом железа 3 ?
Напишите уравнение реакций углерода с алюминием, водородом, фтором, оксидом железа 3 .
Укажите , в каких реакциях углерод — окислитель, а в каких — восстановитель.
Напишите уравнение реакций взаимодействия водорода с ; а)неметаллами * хлором, серой, азотом) б)оксидом меди(2), оксидом железа(2) укажите тип реакций, тепловой эффект, условия возникновения и течения?
Напишите уравнение реакций взаимодействия водорода с ; а)неметаллами * хлором, серой, азотом) б)оксидом меди(2), оксидом железа(2) укажите тип реакций, тепловой эффект, условия возникновения и течения реакций.
Напишите уравнения реакций между водородом и следующими веществами : 2) кислородом ; б) хлором ; в) серой ; г) оксидом железа (II, III) Fe3O4?
Напишите уравнения реакций между водородом и следующими веществами : 2) кислородом ; б) хлором ; в) серой ; г) оксидом железа (II, III) Fe3O4.
Коэффициент перед формулой восстановителя в уравнении реакции восстановления оксида железа (III)?
Коэффициент перед формулой восстановителя в уравнении реакции восстановления оксида железа (III).
Напишите уравнения реакций калия с кислородом, серой, хлором, водородом, фосфором?
Напишите уравнения реакций калия с кислородом, серой, хлором, водородом, фосфором.
Калий запишите первым из реагентов.
Составить уравнения хим?
Составить уравнения хим.
Реакций водорода : — с кислородом и хлором (Сl2) ; — с оксидом никеля ; — с серой и азотом ; — с оксидом железа.
Напишите уравнения реакций натрия и калия с хлором , серой, водородом ?
Напишите уравнения реакций натрия и калия с хлором , серой, водородом .
Записать уравнения реакции серы с железом, кислородом, водородом , цинком?
Записать уравнения реакции серы с железом, кислородом, водородом , цинком.
Напишите уравнения реакций между : а) хлором и железом ; б)хлором и фосфором Укажите окислитель и восстановитель?
Напишите уравнения реакций между : а) хлором и железом ; б)хлором и фосфором Укажите окислитель и восстановитель.
Уравнения химических реакций взаимодействий фтор с водородом ; хлор с натрием ; сера с железом ; кислород с кальцием ; гидроген с бромом ; фтор с железом?
Уравнения химических реакций взаимодействий фтор с водородом ; хлор с натрием ; сера с железом ; кислород с кальцием ; гидроген с бромом ; фтор с железом.
На этой странице находится ответ на вопрос Напишите уравнение реакций водорода с 1)кислородом ; 2)хлором Cl2 ; 3)оксидом железа (3)подчеркни формулу восстановителя ; 4)серой?, из категории Химия, соответствующий программе для 5 — 9 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.
C2 Дано : m(Fe(OH)2) = 45 г Найти : m(FeO) — ? Fe(OH)2 = FeO + H2O 1)n(Fe(OH)2) = m / M M(Fe(OH)2) = 16 * 2 + 1 * 2 + 56 = 32 + 2 + 56 = 90 г / моль n(Fe(OH)2) = 45г / 90г / моль = 0, 5 моль n(Fe(OH)2) = 0, 5 моль 0, 5 n(FeO) = 1 1 n(FeO) = 0, 5 мол..
Кислород — 2 значит — 2 * 4 = — 8 алюминий + 3 значит Хлор + 5.
ᅠᅠ1. Реакция карбоната кальция и азотной кислоты : K₂CO₃ + 2HNO₃ ⇒ 2KNO₃ + CO₂ + H₂O (реакция протекает, так как выделяется газ и вода)2K⁺ + + 2H⁺ + 2 ⇒2K⁺ + 2 + CO₂ + H₂O + 2H⁺ ⇒ CO₂ + H₂O (сокращённое ионное)ᅠᅠРеакция карбоната кальция и азотной к..
Агрегатное состояние вещества «сахар» твердое при комнатной температуре. Плотность кристалов сахара : 1586кг / м ^ 3 Плотность рассыпного : 800 кг / м ^ 3.
Валентность золота 1.
HCl + NaOH = NaCl + H₂O по уравнению реакции m(HCl) / M(HCl) = m(NaCl) / M(NaCl) масса хлороводорода m(HCl) = M(HCl)m(NaCl) / M(NaCl) массовая доля хлороводорода в растворе w = m(HCl) / m(p) w = M(HCl)m(NaCl) / [M(NaCl) * m(p)] w = 36, 5г / моль * 11..
80кг — 100% 0. 8кг — 1% m(п) = 0. 8×80 = 64кг m(ц)80 — 64 = 16кг.
Zn(OH)₂ + 2KOH = K₂[Zn(OH)₄] тетрагидроксоцинкат калия.
У метиламина. Амины сами по себе являются слабыми основаниями (могут реагировать, например, с кислотами). Этанол — спирт. Он обладает кислотными свойствами.
2СН3СООН + Mg = (CH3COO)2Mg + Н2. Ацетат магния. 2СН3 — СН2 — СООН + CaO = (CH3 — CH2 — COO)2Ca + Н2О пропионат кальция. СН3СООН + СН3 — СН2 — ОН = СН3СООС2Н5 + Н2О этилацетат. Два первых вещества соли, последнее вещество, сложный эфир.
http://examchemistry.com/content/lesson/neorgveshestva/hlor.html
http://himia.my-dict.ru/q/1954115_napisite-uravnenie-reakcij-vodoroda-s-1kislorodom/