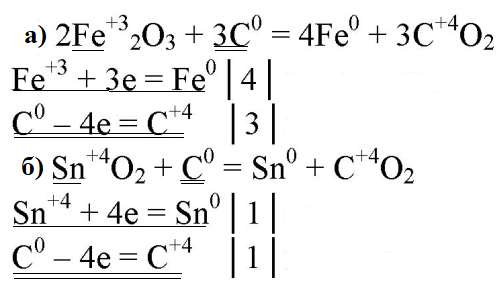Составьте уравнения реакций, протекающих без изменения степени окисления атомов элементов по схеме ?
Химия | 5 — 9 классы
Составьте уравнения реакций, протекающих без изменения степени окисления атомов элементов по схеме :
2KOH + CuCl2 = 2KCl + Cu(OH)2
Cu(OH)2 + 2NaNO3 = 2NaOH + Cu(NO3)2
2NaOH + H2SO4 = Na2SO4 + 2H2O
Na2SO4 + CaCl2 = CaSO4 + 2NaCl
CaSO4 + 2HNO3 = Ca(NO3)2 + H2SO4
Ca(NO3)2 + H2SO4(конц) = CaHSO4 + HNO3
HNO3 + AgCl = AgNO3 + HCl
HCl + BaSo4 = BaCl2 + h2SO4.
Расставьте коэффициенты в уравнении реакции протекающей по схеме : Cu + H2SO4 = CuSO4 + SO2 + H2O Охарактеризуйте данную реакцию по следующим признакам : а)изменения степени окисления ; б)обратимая ил?
Расставьте коэффициенты в уравнении реакции протекающей по схеме : Cu + H2SO4 = CuSO4 + SO2 + H2O Охарактеризуйте данную реакцию по следующим признакам : а)изменения степени окисления ; б)обратимая или необратимая ; в)каталическая или некаталическая.
Составьте уравнения реакцийнатрия а) с хлором б) с серой в) с водородом?
Составьте уравнения реакций
натрия а) с хлором б) с серой в) с водородом.
Расставьте значения степеней окисления химических элементов.
Атомы каких элементов в этих реакция выступают в качестве восстановителей и окислителей?
Составьте уравнения химической реакции , соответствующей схеме S степень окисления 0 — — > ; S в степени окисления + 4 Укажите окислитель и восстановитель?
Составьте уравнения химической реакции , соответствующей схеме S степень окисления 0 — — > ; S в степени окисления + 4 Укажите окислитель и восстановитель.
Составьте схемы строения атома серы в свободном состоянии и характерных степенях окисления?
Составьте схемы строения атома серы в свободном состоянии и характерных степенях окисления.
3. Реакция, протекающая с изменением степеней окисления элементов : 1) NH3 + H2O → … 3) N2O5 + H2O → …2) NO2 + H2O → … 4) CaO + H2O →?
3. Реакция, протекающая с изменением степеней окисления элементов : 1) NH3 + H2O → … 3) N2O5 + H2O → …
2) NO2 + H2O → … 4) CaO + H2O →.
Составьте уравнения реакции которые могут протекать при осуществлении следующих превращений : k — — — > ; SO2 — — — > ; H2SO4 — — — > ; SO2 — — — > ; Na2SO3 к обменным реакциям составьте полно?
Составьте уравнения реакции которые могут протекать при осуществлении следующих превращений : k — — — > ; SO2 — — — > ; H2SO4 — — — > ; SO2 — — — > ; Na2SO3 к обменным реакциям составьте полное и краткое ионное уравнения, а к ОВР схемы изменения степеней окисления, в какой ОВР в качестве реагента можно использовать серу?
Укажите тип реакции, всегда протекающей без изменения степени окисления : а)Соединения б)разложения в)обмена г)замещения?
Укажите тип реакции, всегда протекающей без изменения степени окисления : а)Соединения б)разложения в)обмена г)замещения.
Составьте уравнение реакций которые могут протекать при осуществлении следующих превращений : Mn)2 — MnSO4 — HMnO4 — KMnO4 — K2MnO4 К обменным реакциям составьте полное и краткое ионное уравнение, а к?
Составьте уравнение реакций которые могут протекать при осуществлении следующих превращений : Mn)2 — MnSO4 — HMnO4 — KMnO4 — K2MnO4 К обменным реакциям составьте полное и краткое ионное уравнение, а к окислительно — восстановительным схемы изменения степеней окисления элементов.
Какова окраска водного раствора тетраоксоманганата (4) калия?
Проанализируйте изменения величины зарядов ядер, радиус атомов, электроотрицательностей и степеней окисления элементов 6 А группы?
Проанализируйте изменения величины зарядов ядер, радиус атомов, электроотрицательностей и степеней окисления элементов 6 А группы.
Составить уравнения реакций указав изменения степеней окисления атомов P + ?
Составить уравнения реакций указав изменения степеней окисления атомов P + .
= P2O3 Mg + P N2 + Ca.
Вопрос Составьте уравнения реакций, протекающих без изменения степени окисления атомов элементов по схеме ?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 5 — 9 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
Составьте уравнения реакций протекающих без изменения
Вопрос по химии:
Составьте уравнения реакций, протекающих без изменения степени окисления атомов элементов по схеме:
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 1
2KOH + CuCl2 = 2KCl + Cu(OH)2
Cu(OH)2 + 2NaNO3 = 2NaOH + Cu(NO3)2
2NaOH + H2SO4= Na2SO4 + 2H2O
Na2SO4 + CaCl2 = CaSO4 + 2NaCl
CaSO4 + 2HNO3 = Ca(NO3)2 + H2SO4
Ca(NO3)2 + H2SO4(конц) = CaHSO4 + HNO3
HNO3 + AgCl = AgNO3 + HCl
HCl + BaSo4 = BaCl2 + h2SO4
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Вопросы к параграфу 32 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 32. Химические свойства углерода. Адсорбция
Вопросы и задания
1. При каких процессах образуется древесный уголь? Каково его строение, свойства и применение?
Древесный уголь — твёрдый пористый продукт, разновидность угля, образующийся при нагревании древесины без доступа воздуха. В образовавшемся древесном угле множество капилляров и пор, что делает его хорошим адсорбентом.
Применяют древесный уголь в производстве кристаллического кремния, черных и цветных металлов, сероуглерода, активированного угля, фильтрах для очистки воды, противогазах, как экологически чистое топливо.
2. С помощью каких явлений, которые вы наблюдаете в жизни, можно доказать, что хлеб, молоко, мясо содержат углерод?
Если эти продукты подгорают при жарке, то образуется уголь, значит они содержат углерод.
3. Переведите таблицу 24 в текст.
Кислород легко окисляет углерод до степени окисления +4 с образованием углекислого газа.
В реакциями с оксидами металлов углерод также проявляет свои восстановительные свойства, в результате реакции образуется углекислый газ и металл.
Реакция углерода с углекислым газом и водой приводит к образованию угарного газа.
Углерод может окислять сильные восстановители: металлы — до карбидов, водород — до метана.
4. Составьте уравнения реакций, протекающих при нагревании угля: 1) с оксидом железа(III); 2) с оксидом олова(IV). Покажите переход электронов и подчеркните одной чертой окислитель, а двумя — восстановитель.
5. Основываясь на свойствах углерода и пользуясь рисунком 32, поясните, для каких целей применяют углерод.
- При производстве органических веществ (метанол, бензин, красители);
- В медицине (активированный уголь);
- В ювелирном производстве (алмазы);
- В производстве полимеров (резина).
6. Обсудите с соседом по парте, где в повседневной жизни вы можете встретиться с веществами, в состав которых входят атомы элементов IVA-группы.
В повседневной жизни мы постоянно сталкиваемся с объектами, в составе которых присутствует углерод. Например:
— в изделия из резины и пластика – (игрушки, бытовая техника, одежда и т.д.) — в составе полимеров;
— NaHCO3 – пищевая сода; CaCO3 – мел, мрамор, известняк — в виде карбонатов;
— в еде, лекарственных средствах, красителях и т.д. — в виде органических веществ.
В форме SiO2 – песока — кремний наиболее распространён; его формы также входят в состав стекла и разнообразных минералов. Кремний применяется также в составе полупроводников в бытовой электронике.
http://online-otvet.ru/himia/5cea701796f4e19a29f0ebe9
http://gdzwow.com/answers/9-himiya-uch-rudzitis-vopr-k-par-32.html